同学们对金属模块的内容进行了归纳整理,并找了一些生活中常见的金属制品进行了探究,请你回答下列问题:
(一)图1是有关铁元素的一些信息:
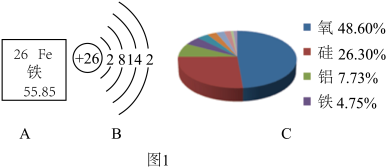
(1)铁的相对原子质量为______ ,亚铁离子的核外电子数应为 _________ ;
(2)C图应该是铁元素在________ (填“海洋中”或“地壳中”)的含量分布图,人体中若缺少铁元素易得 ________ 症.
(二)同学们选取了硬币若干(面值分别为一元、五角,一角)和书钉进行了如下探究:
【查阅资料】我国第四套人民币的硬币从1999年开始发行,一元币为钢芯镀镍(Ni),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时需要考虑的因素有________ (写一条即可).
探究实验一、第一小组同学将一枚五角币放在酒精灯火焰上灼烧片刻,发现表面变黑.
【猜想与假设】
Ⅰ.五角币加热变黑,是因为酒精不完全燃烧产生的_______ 附着在五角币的表面;
Ⅱ.五角币加热变黑,是因为五角币上的镀铜与_____ 发生了化学反应.
【实验验证】用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;请你另取一枚五角币设计实验证明猜想Ⅰ是不成立的(简述实验操作及现象):__________ .
【表达与交流】铜在空气中加热,发生反应的化学反应方程式为________ .
探究实验二、第二小组同学探究硬币与酸的反应
分别取一元硬币和一角(铝合金)硬币各一枚,放入小烧杯中,各加入5mL10%的稀盐酸,如图2所示,观察现象:B烧杯中有很少量的气泡产生;A烧杯中开始没有明显变化,过一段时间后开始有气泡产生,产生气泡的速率明显比B中快.试回答下列问题:

(1)写出 仪器的用途
仪器的用途 __________ .
(2)A烧杯中开始没有明显变化的原因可能是因为____________ .
(3)已知:镍能与稀盐酸反应,生成可溶于水的正二价镍的化合物,并放出氢气,其反应没有铁与酸反应剧烈,镍与稀盐酸反应的化学方程式为______________ .
探究实验三、第三小组同学围绕订书钉开展实验研究
【查阅资料】
订书钉主要成分为铁,其表面镀了一种金属,可能是镁、铝、锌、铜中的一种:

【实验研究】
(1)证明书钉主要成分是铁,可采用的物理方法是__________ .
(2)为探究书钉表面的金属成分做了如下实验:
①取一块订书钉(40根钉子)(如图3甲所示),浸入酒精中,一段时间后能从订书钉块上取下一层胶水薄膜
②取上述订书钉块用棉花擦去酒精,并待酒精完全挥发后称量其质量为13.4g
③将其放入图3乙所示装置,并在干燥管口用氢气传感器测量氢气质量,同时记录质量变化(如图3丙所示,ml为天平示数,mH2为传感器示数---即氢气质量,已知干燥管中装的干燥剂用于除去气体中的水分)
④5.8分钟时停止反应,取出装置中剩余订书钉,洗涤、干燥、称量,剩余订书钉质量为7.8g
【分析与结论】
(1)订书钉表面涂胶水的目的主要是_________ .
(2)请结合图丙分析:
①图丙中P点纵坐标X的值为________________ .
②参加反应的金属的总质量为_______ g.
③根据丙图可知订书钉表面镀的金属应该比铁________ (填“活泼”或“不活泼”).
④请根据实验数据分析订书钉表面镀的金属应该是镁、铝、锌、铜中的___________ .
(一)图1是有关铁元素的一些信息:

(1)铁的相对原子质量为
(2)C图应该是铁元素在
(二)同学们选取了硬币若干(面值分别为一元、五角,一角)和书钉进行了如下探究:
【查阅资料】我国第四套人民币的硬币从1999年开始发行,一元币为钢芯镀镍(Ni),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时需要考虑的因素有
探究实验一、第一小组同学将一枚五角币放在酒精灯火焰上灼烧片刻,发现表面变黑.
【猜想与假设】
Ⅰ.五角币加热变黑,是因为酒精不完全燃烧产生的
Ⅱ.五角币加热变黑,是因为五角币上的镀铜与
【实验验证】用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;请你另取一枚五角币设计实验证明猜想Ⅰ是不成立的(简述实验操作及现象):
【表达与交流】铜在空气中加热,发生反应的化学反应方程式为
探究实验二、第二小组同学探究硬币与酸的反应
分别取一元硬币和一角(铝合金)硬币各一枚,放入小烧杯中,各加入5mL10%的稀盐酸,如图2所示,观察现象:B烧杯中有很少量的气泡产生;A烧杯中开始没有明显变化,过一段时间后开始有气泡产生,产生气泡的速率明显比B中快.试回答下列问题:

(1)写出
 仪器的用途
仪器的用途 (2)A烧杯中开始没有明显变化的原因可能是因为
(3)已知:镍能与稀盐酸反应,生成可溶于水的正二价镍的化合物,并放出氢气,其反应没有铁与酸反应剧烈,镍与稀盐酸反应的化学方程式为
探究实验三、第三小组同学围绕订书钉开展实验研究
【查阅资料】
订书钉主要成分为铁,其表面镀了一种金属,可能是镁、铝、锌、铜中的一种:

【实验研究】
(1)证明书钉主要成分是铁,可采用的物理方法是
(2)为探究书钉表面的金属成分做了如下实验:
①取一块订书钉(40根钉子)(如图3甲所示),浸入酒精中,一段时间后能从订书钉块上取下一层胶水薄膜
②取上述订书钉块用棉花擦去酒精,并待酒精完全挥发后称量其质量为13.4g
③将其放入图3乙所示装置,并在干燥管口用氢气传感器测量氢气质量,同时记录质量变化(如图3丙所示,ml为天平示数,mH2为传感器示数---即氢气质量,已知干燥管中装的干燥剂用于除去气体中的水分)
④5.8分钟时停止反应,取出装置中剩余订书钉,洗涤、干燥、称量,剩余订书钉质量为7.8g
【分析与结论】
(1)订书钉表面涂胶水的目的主要是
(2)请结合图丙分析:
①图丙中P点纵坐标X的值为
②参加反应的金属的总质量为
③根据丙图可知订书钉表面镀的金属应该比铁
④请根据实验数据分析订书钉表面镀的金属应该是镁、铝、锌、铜中的
更新时间:2019-01-21 19:05:21
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图。我对它进行研究:

(1)原子序数为16的元素名称是______ ,在化学反应中,该元素的原子容易______ 电子,变成_______ (填符号);原子序数为11的元素属于__________ 填“金属”或“非金属”)元素。
(2)根据图示信息,推测一个一氧化碳分子中所含的电子总数为_____________ 。
(3)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③__________________________ ;
④__________________________ ;
(4)下图表示碘元素的_________ (填“原子”、“阳离子”或“阴离子”)结构示意图。由图 可知,碘元素应位于元素周期表中的第___________ 周期。


(1)原子序数为16的元素名称是
(2)根据图示信息,推测一个一氧化碳分子中所含的电子总数为
(3)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③
④
(4)下图表示碘元素的

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】钙元素被称为人体中的“白色钢筋混凝土”。请回答下列问题:
(1)下图是钙元素在周期表中的信息和原子结构示意图,下列说法正确的是___________ (填字母序号)。

A 图中的x=8
B 钙离子的符号为Ca+2
C 碳酸氢钙的化学式为CaHCO3
D 钙元素位于元素周期表第4周期
(2)人体缺钙会导致___________ (填字母序号)。
A 侏儒症 B 佝偻病 C 骨质疏松 D 坏血病
(3)以下是同学们对于“钙”提出的问题,请你和同学们一起探究:
【提出问题】钙的化合物这么多,为什么我们很少提起单质钙呢?
【猜想】钙的化学性质很活泼。
【查阅资料】在同一个化学反应中,若有元素化合价升高,就会有元素化合价降低。
【实验验证】从煤油中取出一小颗不规则形状的钙粒,用滤纸吸干表面的煤油,迅速放入盛有100mL冷水的烧杯中,并且滴入2滴酚酞溶液。观察到钙粒变成小圆球,四处游动,最后消失,溶液变红。
【实验结论】
①钙与水反应的化学方程式为___________ 。
②该反应___________ (选填“吸收”或“放出”)热量,理由是___________ 。
【拓展与延伸】请根据题中信息,推测出钙的密度比___________ 大。
【能力与提升】元素的化学性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。已知锶元素在元素周期表中毗邻钙元素的正下方,由此推测,锶的金属活动性比钙的金属活动性___________ (填“强”或“弱”)。
(1)下图是钙元素在周期表中的信息和原子结构示意图,下列说法正确的是

A 图中的x=8
B 钙离子的符号为Ca+2
C 碳酸氢钙的化学式为CaHCO3
D 钙元素位于元素周期表第4周期
(2)人体缺钙会导致
A 侏儒症 B 佝偻病 C 骨质疏松 D 坏血病
(3)以下是同学们对于“钙”提出的问题,请你和同学们一起探究:
【提出问题】钙的化合物这么多,为什么我们很少提起单质钙呢?
【猜想】钙的化学性质很活泼。
【查阅资料】在同一个化学反应中,若有元素化合价升高,就会有元素化合价降低。
【实验验证】从煤油中取出一小颗不规则形状的钙粒,用滤纸吸干表面的煤油,迅速放入盛有100mL冷水的烧杯中,并且滴入2滴酚酞溶液。观察到钙粒变成小圆球,四处游动,最后消失,溶液变红。
【实验结论】
①钙与水反应的化学方程式为
②该反应
【拓展与延伸】请根据题中信息,推测出钙的密度比
【能力与提升】元素的化学性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小。已知锶元素在元素周期表中毗邻钙元素的正下方,由此推测,锶的金属活动性比钙的金属活动性
您最近一年使用:0次
【推荐1】管道疏通颗粒是一种新型卫管道深层清洁产品,主要是针对厨卫管道内的堵
塞进行疏通。某小组对某种管道疏通剂(主要成分为 、铝粉、缓蚀阻垢剂)的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。
、铝粉、缓蚀阻垢剂)的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。
查阅资料: 与铝的混合遇水后发生化学反应,放大量热和气体,可加快通毛发等物质。
与铝的混合遇水后发生化学反应,放大量热和气体,可加快通毛发等物质。
【实验1】按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并过测定反应前后温度的变化比较硫通效果(温度升高值越大,疏通效果越好)。实验数据记录如下:
(1)写出 在生产、生活中的一种用途
在生产、生活中的一种用途______ 。
(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和______ (填序号)。
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是_____ 。
(4)由实验1可得知: 、铝粉、缓蚀阻垢剂的最佳质量比为
、铝粉、缓蚀阻垢剂的最佳质量比为_____ 。
【实验2】其他条件相同时,改变下水管材料,测定管道疏通颗粒对各种材料的腐蚀率。实验结果记录如下表格:
(5)管道疏通颗粒腐蚀率最低的材料是______ 。
(6)该管道疏通颗粒不宜对______ 材质的下水管道进行疏通。
(7)进行实验2时,需要控制相同的变量有____ 、____ (写2条)。
(8) 与铝粉混合遇水后发生化学反应的产物是Ca(AlO2)2和氢气,请写出该反应的化学方程式
与铝粉混合遇水后发生化学反应的产物是Ca(AlO2)2和氢气,请写出该反应的化学方程式______ 。
塞进行疏通。某小组对某种管道疏通剂(主要成分为
 、铝粉、缓蚀阻垢剂)的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。
、铝粉、缓蚀阻垢剂)的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。查阅资料:
 与铝的混合遇水后发生化学反应,放大量热和气体,可加快通毛发等物质。
与铝的混合遇水后发生化学反应,放大量热和气体,可加快通毛发等物质。【实验1】按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并过测定反应前后温度的变化比较硫通效果(温度升高值越大,疏通效果越好)。实验数据记录如下:
| 序号 |  质量/g 质量/g | 铝粉质量/g | 缓蚀阻垢剂质量/s | 混合前后温度升高值/°C |
| ① | 1.3 | 0.55 | 0.18 | 63 |
| ② | 1.3 | 0.75 | 0.18 | 78 |
| ③ | 1.3 | 0.95 | 0.18 | 89 |
| ④ | 1.3 | 1.15 | 0.18 | 83 |
| ⑤ | 1.3 | 0.95 | 0.04 | 86 |
| ⑥ | 1.3 | 0.95 | 0.09 | 87 |
| ⑦ | 1.3 | 0.95 | 0.27 | 87 |
 在生产、生活中的一种用途
在生产、生活中的一种用途(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是
(4)由实验1可得知:
 、铝粉、缓蚀阻垢剂的最佳质量比为
、铝粉、缓蚀阻垢剂的最佳质量比为【实验2】其他条件相同时,改变下水管材料,测定管道疏通颗粒对各种材料的腐蚀率。实验结果记录如下表格:
| 材料 | 塑料 | 铜 | 铁 | 钢 | 铝 | 铝合金 |
| 腐蚀率 | 0.1% | 0.4% | 0.5% | 0.3% | 100% | 80% |
(6)该管道疏通颗粒不宜对
(7)进行实验2时,需要控制相同的变量有
(8)
 与铝粉混合遇水后发生化学反应的产物是Ca(AlO2)2和氢气,请写出该反应的化学方程式
与铝粉混合遇水后发生化学反应的产物是Ca(AlO2)2和氢气,请写出该反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】金属的用途与性质密切相关。
(1)如图所示赤铁矿的主要成分是________ (填名称);

(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据信息分析,其原因是_______________ ;
(3)在空气中,铝具有很好的抗腐蚀性,其原因是______ ;
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(如图所示),说明铁比铜的金属活动性更强的实验现象是______ ,反应的化学方程式是______ ,后来,小贝选择两种药品,通过一步实验,也达到了实验目的,她选用的药品是 ____ (写出一种药品组合即可);

(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是____ (填字母)。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3﹣
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
(1)如图所示赤铁矿的主要成分是

(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据信息分析,其原因是
| 铜 | 铝 | |
| 密度/(gcm-3) | 8.92 | 2.70 |
| 地壳中含量(质量分数/%) | 0.007 | 7.73 |
| 导电性(以银的导电性为100做标准) |  | |
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(如图所示),说明铁比铜的金属活动性更强的实验现象是

(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3﹣
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小敏很好奇易拉罐的材料组成,为此展开了一系列探究。
查阅资料
(1)金属的活动性由强到弱的顺序是 K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
(2)部分金属的价格:
(3)K Ca Na遇冷水剧烈反应,且易发生爆炸: ,镁能与热水发生类似反应放出氢气,铝和水在加热时反应也很微弱,可以忽略不计。
,镁能与热水发生类似反应放出氢气,铝和水在加热时反应也很微弱,可以忽略不计。
材料分析:①.从金属的价格上看不可能是Sn、Ag、Pt、Au;
②.从易拉罐的金属颜色上看不可能是Cu;
③.从金属与水反应的剧烈程度上看不可能是K、Ca、Na、Mg;
④.从金属的毒性看不可能是Pb和Hg;
⑤.因此,易拉罐的材料可能是__________ (填元素名称)。
设计实验并进行实验
查阅资料
(1)金属的活动性由强到弱的顺序是 K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
(2)部分金属的价格:
| 金属 | 铝 | 锌 | 铁 | 锡 | 铅 | 铜 | 银 | 铂 | 金 |
| 价格(元/公斤) | 13 | 23 | 4 | 146 | 16 | 49 | 3600 | 196000 | 282000 |
 ,镁能与热水发生类似反应放出氢气,铝和水在加热时反应也很微弱,可以忽略不计。
,镁能与热水发生类似反应放出氢气,铝和水在加热时反应也很微弱,可以忽略不计。材料分析:①.从金属的价格上看不可能是Sn、Ag、Pt、Au;
②.从易拉罐的金属颜色上看不可能是Cu;
③.从金属与水反应的剧烈程度上看不可能是K、Ca、Na、Mg;
④.从金属的毒性看不可能是Pb和Hg;
⑤.因此,易拉罐的材料可能是
设计实验并进行实验
| 实验步骤 | 实验现象 | 实验结论 |
| 用磁铁吸引 | 易拉罐不能被吸引 | ① |
| 将打磨后的易拉罐样品剪碎,加入 | 样品上有细小气泡,表面覆盖一层白色金属 | 该易拉罐成分是 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】金属活动性顺序是金属化学性质的核心内容,为了更好地掌握该知识,提升科学探究能力,某实验小组同学以铝、铁、铜三种常见金属为例,对金属活动性强弱的验证展开了项目化学习。
任务一:依据金属与氧气的反应进行验证
【查阅交流】
(1)①铝常温下能与空气中的氧气反应,导致铝更耐腐蚀的原因是___ (用化学方程式表示)。
②铁在空气中不能燃烧,在纯氧中点燃铁丝,能剧烈燃烧。
③铁、铜在常温下几乎不与氧气反应,在潮湿空气中,铜比铁耐腐蚀。
【得出结论】
(2)小组同学依据______ ,得出结论:金属活泼性:Al>Fe>Cu。
任务二:利用金属与稀酸的反应进行验证
【进行实验】
(3)分别取形状、大小完全相同的三种金属片放在三支试管中,进行如下图操作并记录了实验现象。
【得出结论】金属活动性:Al>Fe>Cu。
【反思评价】
(4)小组同学仔细分析实验后,提出了质疑,认为实验不严密,理由是:______ 。
任务三:根据金属与金属盐溶液的反应进行验证
【进行实验】如图,分别取两片形状、大小完全相同的铁片放在试管中,滴加等量的氯化铝溶液和氯化铜溶液。
(5)实验①无明显现象;实验②的现象是______ ,反应的化学方程式是______ 。
【得出结论】金属活动性:Al>Fe>Cu。
【拓展延伸】
(6)小组同学通过实验,讨论后一致认为利用其他三种物质也可完成铝、铁、铜的金属活动性强弱探究,请写出其中一种组合的三种物质______ 。
任务四:对废液成分的探究
【讨论交流】
(7)若待实验②充分反应后取出铁片,晾干后发现增重0.1g,则反应掉的铁的质量______ g。
(8)实验结束,为做好废液处理,小组同学将任务三中实验①②反应后的物质全部倒入一个洁净的烧杯内,观察到红色固体明显增多,由此可推断出,烧杯中废液的溶质成分一定有______ 。为了验证烧杯中可能存在的固体,下列可以选用的试剂有______ 。
A.氢氧化钠溶液 B.氯化亚铁溶液 C.氯化铜溶液 D.稀硫酸
任务一:依据金属与氧气的反应进行验证
【查阅交流】
(1)①铝常温下能与空气中的氧气反应,导致铝更耐腐蚀的原因是
②铁在空气中不能燃烧,在纯氧中点燃铁丝,能剧烈燃烧。
③铁、铜在常温下几乎不与氧气反应,在潮湿空气中,铜比铁耐腐蚀。
【得出结论】
(2)小组同学依据
任务二:利用金属与稀酸的反应进行验证
【进行实验】
(3)分别取形状、大小完全相同的三种金属片放在三支试管中,进行如下图操作并记录了实验现象。
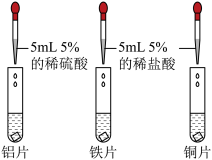
| 实验现象 | |
| 铝片 | 铝片表面产生大量气泡 |
| 铁片 | |
| 铜片 | 铜片表面无明显现象 |
【得出结论】金属活动性:Al>Fe>Cu。
【反思评价】
(4)小组同学仔细分析实验后,提出了质疑,认为实验不严密,理由是:
任务三:根据金属与金属盐溶液的反应进行验证
【进行实验】如图,分别取两片形状、大小完全相同的铁片放在试管中,滴加等量的氯化铝溶液和氯化铜溶液。

(5)实验①无明显现象;实验②的现象是
【得出结论】金属活动性:Al>Fe>Cu。
【拓展延伸】
(6)小组同学通过实验,讨论后一致认为利用其他三种物质也可完成铝、铁、铜的金属活动性强弱探究,请写出其中一种组合的三种物质
任务四:对废液成分的探究
【讨论交流】
(7)若待实验②充分反应后取出铁片,晾干后发现增重0.1g,则反应掉的铁的质量
(8)实验结束,为做好废液处理,小组同学将任务三中实验①②反应后的物质全部倒入一个洁净的烧杯内,观察到红色固体明显增多,由此可推断出,烧杯中废液的溶质成分一定有
A.氢氧化钠溶液 B.氯化亚铁溶液 C.氯化铜溶液 D.稀硫酸
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】在“质量守恒定律”的教学中,老师引导同学们进行“化学反应中反应物与生成物的质量关系”的实验探究,请你参与探究并回答有关问题:
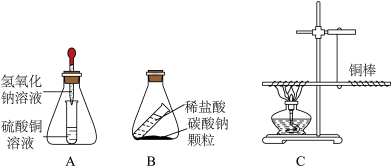
(1)如图A、图B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上。
①A瓶试管中发生反应的化学方程式为____________ ;把A瓶重新放回到天平上,天平____________ (选填“能”或“不能”)保持平衡。
②把B瓶重新放回到天平上,天平___________ (选填“能”或“不能”)保持平衡 ,理由是_________
③从原子的角度分析化学反应遵守“质量守恒定律”的原因是____________ 。
(2)如图C所示,用细线系住铜棒使之平衡,然后在铜棒一端用酒精灯加热。
①写出铜棒反应的化学方程式:____________ 。
②加热一段时间后,铜棒___________ (选填“能”或“不能”)保持平衡。
③本实验现象与质量守恒定律___________ (选填“有”或“没有”)矛盾。

(1)如图A、图B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上。
①A瓶试管中发生反应的化学方程式为
②把B瓶重新放回到天平上,天平
③从原子的角度分析化学反应遵守“质量守恒定律”的原因是
(2)如图C所示,用细线系住铜棒使之平衡,然后在铜棒一端用酒精灯加热。
①写出铜棒反应的化学方程式:
②加热一段时间后,铜棒
③本实验现象与质量守恒定律
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组将光亮铜片放在酒精灯火焰上灼烧,发现表面变黑,他们对黑色物质来源产生了兴趣,铜片表面黑色物质是什么呢?
【猜想与假设】猜想一:铜片表面的黑色固体是烟灰。
猜想二:铜片表面的黑色固体可能是空气中的氧气与铜反应生成的新物质。
猜想三:铜片表面的黑色固体既有烟灰又有氧气与铜反应生成的新物质。
【查阅资料】①酒精不充分燃烧产生炭黑(即黑烟)
②氧气的化学性质比较活泼,加热条件下能与金属铜反应生成黑色的氧化铜
【进行实验】
【反思拓展】
(1)实验一将铜片放入试管中加热,目的是排除了___________ 的干扰。
(2)实验二用注射器抽出试管内空气的目的是___________ 。
【猜想与假设】猜想一:铜片表面的黑色固体是烟灰。
猜想二:铜片表面的黑色固体可能是空气中的氧气与铜反应生成的新物质。
猜想三:铜片表面的黑色固体既有烟灰又有氧气与铜反应生成的新物质。
【查阅资料】①酒精不充分燃烧产生炭黑(即黑烟)
②氧气的化学性质比较活泼,加热条件下能与金属铜反应生成黑色的氧化铜
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 实验一:取一小段光亮铜片,放入试管内,然后用试管夹夹持试管,放在酒精灯的外焰部位加热 | 铜片变黑 | 猜想 |
| 实验二:取一试管,将一小段光亮铜片放入试管中,塞上胶塞,并用注射器抽出试管内的空气,封好胶塞,并加热,趁热取下胶塞,观察现象 | 取下胶塞前的现象 取下胶塞后的现象 | 猜想二成立 |
(1)实验一将铜片放入试管中加热,目的是排除了
(2)实验二用注射器抽出试管内空气的目的是
您最近一年使用:0次
【推荐1】某化学兴趣小组的学生,发现金属Cr不在初中学到的金属活动性顺序表中,该小组为了解Cr与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】猜想一:Al>Cu>Cr,猜想二:①___________ ,猜想三:Cr>Al>Cu,
【实验探究】为了探究哪一种猜想成立,进行了如下探究实验:(已知Cr为+2价,为亚铬)
【交流反思】你认为实验前打磨金属丝的主要目的是⑤___________ 。
【作出猜想】猜想一:Al>Cu>Cr,猜想二:①
【实验探究】为了探究哪一种猜想成立,进行了如下探究实验:(已知Cr为+2价,为亚铬)
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨Cr丝,并将其插入到硫酸铜溶液中 | Cr丝表面覆盖了一层红色的物质 | 猜想一② |
| 猜想二 | 打磨粗细相同的Cr丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①铬丝表面产生气泡缓慢 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立。 Cr与稀硫酸反应的化学方程式为③ |
| 猜想三 | ④ | 无明显现象 | 猜想三不成立 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】为探究木炭还原氧化铜的最佳条件,用适量的木炭粉和氧化铜的干燥混合物进行一系列实验。

【查阅资料】
①木炭还原氧化铜得到铜中可能含有少量的氧化亚铜;
②氧化亚铜为红色固体,能与稀硫酸发生反应: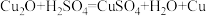
③铜不能和稀硫酸发生化学反应。
【进行实验】取一定量的混合物,用如图所示的装置进行多次实验,获得如下实验数据与现象。
【解释与结论】
(1)实验装置中,酒精灯加金属网罩的作用是_______ ;
(2)证明产生了CO2的现象是_______ ;
(3)由上述实验可以得到的结论是,木炭粉与氧化铜的质量比为_______ 时,条件最佳。
(4)为了检验生成的红色固体中是否含有Cu2O,所需试剂是________ ;
(5)下列有关该实验的说法正确的是__________ ;
A 反应开始的标志是试管b中气泡产生
B 反应后,试管a中固体减少的质量大于生成的气体中碳元素的质量
C 木炭粉发生了氧化反应
D 铜元素是地壳中含量最高的金属元素
E 氧化亚铜中,铜元素的化合价为+1价

【查阅资料】
①木炭还原氧化铜得到铜中可能含有少量的氧化亚铜;
②氧化亚铜为红色固体,能与稀硫酸发生反应:
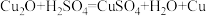
③铜不能和稀硫酸发生化学反应。
【进行实验】取一定量的混合物,用如图所示的装置进行多次实验,获得如下实验数据与现象。
| 序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色和状态 | |
| 1 | 1:9 | 有红色固体,有金属光泽。 | 混有少量黑色物质 |
| 2 | 1:10 | 混有很少量黑色物质 | |
| 3 | 1:11 | 混有极少量黑色物质 | |
| 4 | 1:12 | 无黑色物质 | |
| 5 | 1:13 | 混有较多黑色物质 | |
(1)实验装置中,酒精灯加金属网罩的作用是
(2)证明产生了CO2的现象是
(3)由上述实验可以得到的结论是,木炭粉与氧化铜的质量比为
(4)为了检验生成的红色固体中是否含有Cu2O,所需试剂是
(5)下列有关该实验的说法正确的是
A 反应开始的标志是试管b中气泡产生
B 反应后,试管a中固体减少的质量大于生成的气体中碳元素的质量
C 木炭粉发生了氧化反应
D 铜元素是地壳中含量最高的金属元素
E 氧化亚铜中,铜元素的化合价为+1价
您最近一年使用:0次
【推荐3】学习完金属的化学性质,同学们来到实验室进行锌、铜、银三种金属活动性顺序的探究活动。
老师提供的药品有:锌片、铜片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、银片、硫酸铜溶液;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液。
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白(注:表格中实验操作一栏用文字描述):
【解释与结论】根据上述实验,小华得出三种金属活动性由强到弱的顺序。
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:有同学提出,小华的实验中不用硫酸铜溶液也能得到相同的实验结论。请利用老师提供的药品,写出另一组实验②的药品________ 。
老师提供的药品有:锌片、铜片、银片、硫酸锌溶液、硫酸铜溶液、硝酸银溶液和稀硫酸。
【制定计划】在老师的指导下,经过讨论,同学们设计出了以下几种实验方案:
方案一:铜片、硫酸锌溶液、硝酸银溶液;
方案二:锌片、银片、硫酸铜溶液;
方案三:锌片、铜片、硫酸铜溶液、硝酸银溶液。
【进行实验】小华同学选用方案三进行如下探究,请你帮他完成表格中的空白(注:表格中实验操作一栏用文字描述):
| 实验操作 | 实验现象 | 分析与结论 |
① | 金属活动性:Cu | |
| ② | 锌片表面出现一层红色物质,溶液由蓝色逐渐变为无色。 | 金属活动性:Zn |
【反思与评价】探究活动结束后,同学们分享自己的收获与不足,并进行反思:有同学提出,小华的实验中不用硫酸铜溶液也能得到相同的实验结论。请利用老师提供的药品,写出另一组实验②的药品
您最近一年使用:0次



