化学研究性学习小组同学取10g石灰石样品,用足量的稀盐酸测定石灰石中碳酸钙的质量分数(假设石灰石中杂质不与盐酸反应)。测量5分钟内生成CO2质量的数据如下表:
请回答下列问题:
I.石灰石中的CaCO3完全反应时,生成二氧化碳气体的物质的量为_____mol。
II.该石灰石中CaCO3的质量分数是多少?(根据化学方程式列式计算)
Ⅲ.请根据表中数据分析,你能发现数据背后的化学反应规律是_____。
时间/分钟 | 1 | 2 | 3 | 4 | 5 |
生成 CO2 的质量/g | 1.5 | 2.5 | 3.0 | 3.3 | 3.3 |
I.石灰石中的CaCO3完全反应时,生成二氧化碳气体的物质的量为_____mol。
II.该石灰石中CaCO3的质量分数是多少?(根据化学方程式列式计算)
Ⅲ.请根据表中数据分析,你能发现数据背后的化学反应规律是_____。
更新时间:2019/04/24 22:40:37
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某物质在点燃的条件下发生反应,反应物和生成物共四种,它们的微观示意图和反应前后的质量如表所示。
(1)y=_______________ 。
(2)参加反应的甲、乙、丙、丁的实际质量比为_______________ (填最简整数比)。
(3)上述反应的化学方程式为_______________ 。
(4)根据化学方程式用相对分子质量和化学计量数表示出参加反应各物质的质量比,甲:乙:丙:丁=_______________ (列式并计算),由此可知参加反应的物质实际质量之比__________ 相对质量之比(填“=”或“≠”)。
| 物质序号 | 微观示意图 | 反应前质量/g | 反应后质量/g |
| 甲 |
| 32 | 0 |
| 乙 |
| 130 | 2 |
| 丙 |
| 10 | 98 |
| 丁 |
| 20 | y |
| |||
(1)y=
(2)参加反应的甲、乙、丙、丁的实际质量比为
(3)上述反应的化学方程式为
(4)根据化学方程式用相对分子质量和化学计量数表示出参加反应各物质的质量比,甲:乙:丙:丁=
您最近一年使用:0次
计算题
|
适中
(0.65)
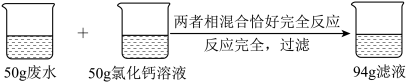
【推荐2】对废旧金属进行回收和利用,不仅有利于节约资源和能源,还能有效减少对环境的污染。化学兴趣小组的同学要对某废弃黄铜(铜锌合金)制品进行纯度分析,进行如下实验:把对表面进行清洁的部分黄铜研磨成粉末,称取32.5g黄铜样品放入烧杯,然后加入足量稀硫酸,搅拌,至不再有气泡产生,反应过程如下图所示;然后过滤、洗涤,蒸发滤液,共得到16.1g固体。请分析并完成下列问题:

(1)将黄铜研磨成粉末的目的是: ;
(2)由反应图线可知,随着反应的进行,反应速度逐渐减小,原因是: 。至反应结束所需要的时间是 S;
(3)计算黄铜样品中铜的质量分数。

(1)将黄铜研磨成粉末的目的是: ;
(2)由反应图线可知,随着反应的进行,反应速度逐渐减小,原因是: 。至反应结束所需要的时间是 S;
(3)计算黄铜样品中铜的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将硫酸钠和碳酸钠的混合物12.4g加50g水,使混合物充分溶解变成溶液,在这混合溶液中加入10%的稀硫酸49g,恰好完全反应。试计算:(结果保留至0.1%)
(1)原12.4g混合物中碳酸钠的质量为多少?
(2)反应后溶液中溶质的质量分数为多少?
(1)原12.4g混合物中碳酸钠的质量为多少?
(2)反应后溶液中溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】波尔多液是一种应用广泛的农药,由熟石灰和硫酸铜配制而成。某工厂用以下反应:2Cu+O2+2H2SO4═2CuSO4+2H2O来生产硫酸铜,若要制得80kg硫酸铜,求消耗12.25%稀硫酸溶液的质量____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】过氧化钙(CaO2)常温下稳定,在潮湿的空气及水中缓慢放出氧气,常用作鱼苗长途运输时的增氧剂,加热至350℃迅速分解,生成氧化钙和氧气(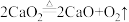 )。
)。_______ 。
(2)现称取9.0g含杂质的CaO2样品进行热分解实验(杂质不参与反应),测得反应过程中剩余固体质量与时间的关系如图所示。计算:
①生成O2的质量为_______ g;
②该样品中CaO2的质量分数_______ (写出计算过程)。
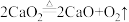 )。
)。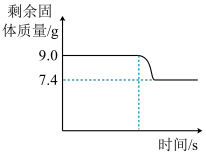
(2)现称取9.0g含杂质的CaO2样品进行热分解实验(杂质不参与反应),测得反应过程中剩余固体质量与时间的关系如图所示。计算:
①生成O2的质量为
②该样品中CaO2的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值。工业上用废铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝。现用5.6t铁屑与l00t废液恰好完全反应(已知铁屑只和废液中的硫酸反应),请你计算:
(1)可生成硫酸亚铁的质量
(2)所用废液中硫酸的溶质质量分数
(1)可生成硫酸亚铁的质量
(2)所用废液中硫酸的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。根据实验数据求反应前氯酸钾的质量分数。
| 加热时间/min | 0 | t1 | t2 | t3 | t4 |
| 固体质量/g | 50.0 | 44.4 | 35.0 | 30.8 | 30.8 |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】石灰石是我省的主要矿产之一、学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分4份进行实验,结果如下表:
(1)哪几次碳酸钙有剩余?__________ 。
(2)上表中m=___________ ,n=__________ 。
(3)试计算这种石灰石中碳酸钙的质量分数。
| 1 | 2 | 3 | 4 | |
| 加入样品质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | m | 4.4 | n |
(2)上表中m=
(3)试计算这种石灰石中碳酸钙的质量分数。
您最近一年使用:0次




 。
。 ,计算生产600t尿素,理论上能吸收CO2的质量是多少?
,计算生产600t尿素,理论上能吸收CO2的质量是多少?