在科学拓展课程中,某科学兴趣小组开展了“使带火星的木条复燃所需氧气的最低体积分数是多少”的实验探究。
(1)该兴趣小组同学利用如图所示装置制取氧气,称取一定质量的KMnO4固体放入试管中,试管内的药品放入试管底部,开始加热时,要让试管均匀受热,具体操作是_____ 。
(2)有同学认为用过氧化氢溶液和二氧化锰制取氧气更好,其理由是_____ 。
(3)为了使实验数据更加具体和准确,小组同学经讨论,他们准备用不同体积分数的氧气来进行实验。利用如图2所示装置收集氧气得到1号瓶,并利用这种方法依次得到2﹣4号瓶。分别将带火星的木条伸入集气瓶中,得到的现象如表:
某同学根据实验现象得出结论:“氧气约占36%时就是带火木条复燃的最低体积分数”,而其他同学立即反对,原因是_____ 。
(4)反思交流:综合上述探究,空气法收集氧气时,验氧气是否集满采用使带火星的木条复燃的方法,你认为是否科学?_____ 。
1号瓶 (收集34%的氧气) | 2号瓶 (收集35%的氧气) | 3号瓶 (收集36%的氧气) | 4号瓶 (收集37%的氧气) |
不复燃 | 不复燃,但很亮 | 很亮,复燃 | 立即复燃 |
(2)有同学认为用过氧化氢溶液和二氧化锰制取氧气更好,其理由是
(3)为了使实验数据更加具体和准确,小组同学经讨论,他们准备用不同体积分数的氧气来进行实验。利用如图2所示装置收集氧气得到1号瓶,并利用这种方法依次得到2﹣4号瓶。分别将带火星的木条伸入集气瓶中,得到的现象如表:
| 1号瓶(收集34%的氧气) | 2号瓶(收集35%的氧气) | 3号瓶(收集36%的氧气) | 4号瓶(收集37%的氧气) |
| 不复燃 | 不复燃,但很亮 | 很亮,复燃 | 立即复燃 |
(4)反思交流:综合上述探究,空气法收集氧气时,验氧气是否集满采用使带火星的木条复燃的方法,你认为是否科学?
更新时间:2019-05-08 17:24:12
|
相似题推荐
【推荐1】关于燃烧的研究是一项重要的课题。某小组以“探究燃烧的奥秘”为主题开展学习。
任务一:探究燃烧的条件
小明向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。他对该实验原理很感兴趣,进行了下列探究。
【实验探究及分析】
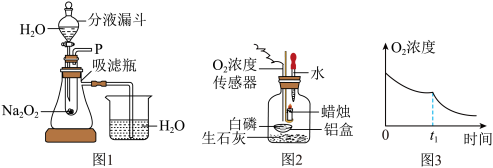
(1)如图1,打开分液漏斗活塞,以适当的速度将水滴入Na2O2中,观察到试管内有气泡产生,将带火星的木条靠近P处,当看到___________ ,说明反应生成了氧气。
(2)实验中还观察到烧杯中的导管口有气泡冒出,原因是___________ ,这一现象也为脱脂棉燃烧找到了依据。
任务二:白磷燃烧的再探究
【查阅资料】生石灰遇水反应,放出大量的热。
【实验步骤】如图2所示,点燃蜡烛后伸入广口瓶,立即塞紧橡皮塞,观察到蜡烛在瓶内燃烧,白磷不燃烧。待蜡烛自动熄灭(蜡烛未燃尽)且装置冷却到室温后,将胶头滴管中的水全部滴入广口瓶,铝盒中的足量白磷开始燃烧。图3是广口瓶内O2浓度随时间变化的图像。
【分析讨论】
(3)对比滴入水前后白磷的现象,可得出可燃物燃烧的条件之一是___________ 。
(4)白磷燃烧的化学方程式为___________ 。
(5)本实验能得出的结论是_________(填字母)。
任务三:自主设计实验
(6)利用蜡烛和烧杯,设计一个简单的实验,验证可燃物燃烧的条件之一为需要与氧气或空气接触,请写出你的实验方案及现象___________ 。

任务一:探究燃烧的条件
小明向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。他对该实验原理很感兴趣,进行了下列探究。
【实验探究及分析】
(1)如图1,打开分液漏斗活塞,以适当的速度将水滴入Na2O2中,观察到试管内有气泡产生,将带火星的木条靠近P处,当看到
(2)实验中还观察到烧杯中的导管口有气泡冒出,原因是
任务二:白磷燃烧的再探究
【查阅资料】生石灰遇水反应,放出大量的热。
【实验步骤】如图2所示,点燃蜡烛后伸入广口瓶,立即塞紧橡皮塞,观察到蜡烛在瓶内燃烧,白磷不燃烧。待蜡烛自动熄灭(蜡烛未燃尽)且装置冷却到室温后,将胶头滴管中的水全部滴入广口瓶,铝盒中的足量白磷开始燃烧。图3是广口瓶内O2浓度随时间变化的图像。
【分析讨论】
(3)对比滴入水前后白磷的现象,可得出可燃物燃烧的条件之一是
(4)白磷燃烧的化学方程式为
(5)本实验能得出的结论是_________(填字母)。
| A.可燃物燃烧O2必须充足 |
| B.白磷燃烧结束后广口瓶内没有O2存在 |
| C.蜡烛燃烧时所需O2的浓度大于白磷燃烧时所需O2的浓度 |
任务三:自主设计实验
(6)利用蜡烛和烧杯,设计一个简单的实验,验证可燃物燃烧的条件之一为需要与氧气或空气接触,请写出你的实验方案及现象
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组通过查阅资料发现在一定条件下镁可以和二氧化氮反应,发出耀眼白光,放出热量,生成氧化镁和氮化镁,小明决定利用如下实验进行探究。
【提出问题】二氧化氮是否支持燃烧?
【查阅资料】
(1)①蓝色的硝酸铜固体在加热条件下分解生成氧化铜、二氧化氮和氧气。该反应的化学方程式为:______________________ 。
②CuO是一种黑色固体;通常状况下,NO2是一种红棕色气体,相同状况下,其密度大于氧气密度,在低于室温时变成液态。
(2)【实验过程】
【反思与评价】
(3)小刚认为小明的实验不能证明NO2具有助燃性,其理由是________________ 。
小刚认为利用补充如下实验可以证明NO2具有助燃性。
(4)【实验改进】
【拓展】镁不仅在二氧化氮气体中能燃烧,在二氧化碳气体中也能燃烧生成氧化镁和一种单质,由此说明燃烧不一定有氧气参加。
【提出问题】二氧化氮是否支持燃烧?
【查阅资料】
(1)①蓝色的硝酸铜固体在加热条件下分解生成氧化铜、二氧化氮和氧气。该反应的化学方程式为:
②CuO是一种黑色固体;通常状况下,NO2是一种红棕色气体,相同状况下,其密度大于氧气密度,在低于室温时变成液态。
(2)【实验过程】
| 实验装置 | 实验现象 | 实验结论 |
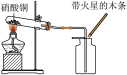 | 试管内蓝色固体逐渐变为黑色,有红棕色气体生成, | 二氧化氮能支持燃烧。 |
【反思与评价】
(3)小刚认为小明的实验不能证明NO2具有助燃性,其理由是
小刚认为利用补充如下实验可以证明NO2具有助燃性。
(4)【实验改进】
| 实验操作 | 实验现象 | 实验结论 |
步骤Ⅰ:在图2的试管和集气瓶之间连上图3所示的装置,重新进行加热硝酸铜的实验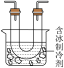 | 带火星的木条复燃 | 硝酸铜分解产物中有 |
| 步骤Ⅱ:取出图3的U型管,恢复至室温,待U型管内充满红棕色气体时,将带火星的木条伸入U型管中 | 带火星的木条复燃 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】新年联欢晚会上,老师给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和一团包有过氧化钠(Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣,请你参与同学们的讨论和探究。
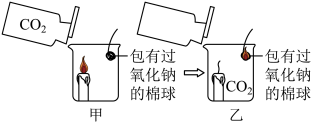
【提出问题】棉花为什么会燃烧?
【提出猜想】①可能是蜡烛燃烧引燃了棉花。
②可能是二氧化碳与过氧化钠反应生成了氧气。
③_________ 。
【实验验证】
【反思与交流】
(1)CO2与Na2O2反应生成了氧气与一种化合物,化学方程式为_______ 。
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。

【提出问题】棉花为什么会燃烧?
【提出猜想】①可能是蜡烛燃烧引燃了棉花。
②可能是二氧化碳与过氧化钠反应生成了氧气。
③
【实验验证】
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 按下图所示装置进行实验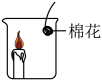 | 无现象 | 猜想① |
| ② | 向盛满二氧化碳的集气瓶中加适量的过氧化钠粉末,充分振荡,并 | 二氧化碳与过氧化钠反应生成了氧气猜想②成立 | |
| ③ | 瓶壁温度升高 | 猜想③成立 |
(1)CO2与Na2O2反应生成了氧气与一种化合物,化学方程式为
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
您最近一年使用:0次
【推荐1】某学习小组探究水泥负载二氧化锰对过氧化氢分解速率的影响。
【查阅资料】
a.水泥负载二氧化锰催化剂是将二氧化锰与水泥按照一定比例混合,加水搅拌制成的一种块状催化剂。
b.通过测定反应过程中压强变化值衡量过氧化氢分解速率,压强变化值越大,说明过氧化氢分解速率越快。
【进行实验】
每次实验时均向反应容器中加入5mL过氧化氢溶液并采集相同时间内的压强变化值,记录如下:
【解释与结论】
(1)水泥负载二氧化锰催化过氧化氢分解的文字表达式为___________ 。
(2)依据表中数据回答,⑦中压强变化值比⑧大的原因是___________ 。
(3)对比实验①②③,得出的结论是___________ 。
(4)探究等体积过氧化氢溶液中,过氧化氢溶液浓度对过氧化氢分解速率的影响的实验是_____ (填实验序号)。
【反思与评价】
(5)依据表中数据回答,不能得出“过氧化氢溶液浓度、水泥与二氧化锰的质量比相同时,水泥负载二氧化锰催化剂的质量越大,过氧化氢分解速率越快”的实验结论,其证据是_______ 。
【查阅资料】
a.水泥负载二氧化锰催化剂是将二氧化锰与水泥按照一定比例混合,加水搅拌制成的一种块状催化剂。
b.通过测定反应过程中压强变化值衡量过氧化氢分解速率,压强变化值越大,说明过氧化氢分解速率越快。
【进行实验】
每次实验时均向反应容器中加入5mL过氧化氢溶液并采集相同时间内的压强变化值,记录如下:
| 实验序号 | 过氧化氢溶液浓度/% | 水泥与二氧化锰的质量比 | 水泥负载二氧化锰催化剂的质量/g | 压强变化值/kPa |
| ① | 5 |  | 0.5 | 7.92 |
| ② | 5 |  | 0.5 | 11.98 |
| ③ | 5 |  | 0.5 | 15.82 |
| ④ | 8 |  | 0.5 | 23.26 |
| ⑤ | 11 |  | 0.5 | 31.47 |
| ⑥ | 5 |  | 0.3 | 13.22 |
| ⑦ | 5 |  | 0.1 | 10.78 |
| ⑧ | 5 |  | 0 | 0.02 |
(1)水泥负载二氧化锰催化过氧化氢分解的文字表达式为
(2)依据表中数据回答,⑦中压强变化值比⑧大的原因是
(3)对比实验①②③,得出的结论是
(4)探究等体积过氧化氢溶液中,过氧化氢溶液浓度对过氧化氢分解速率的影响的实验是
【反思与评价】
(5)依据表中数据回答,不能得出“过氧化氢溶液浓度、水泥与二氧化锰的质量比相同时,水泥负载二氧化锰催化剂的质量越大,过氧化氢分解速率越快”的实验结论,其证据是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动,请你和他们一起完成以下实验探究。
【提出问题】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【查阅资料】 CaCl2溶液显中性
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I :只有CaCl2;
猜想II:有______________________ 。
猜想Ⅲ:有CaCl2和Ca(OH)2;
猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是______________________ 。(用化学方程式解释)
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】
(1) 丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____________________ 。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑_____________________ 。
【反思交流】
(3) 某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如图所示,请回答下列问题:
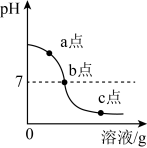
①由图可知,在c点处溶液中溶质是____________________ 。
②若要使c点对应的溶液变成b点对应的溶液,需要除去杂质,其中的一种方法是向烧杯中加入过量的____________________ ,过滤,除杂。
【提出问题】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【查阅资料】 CaCl2溶液显中性
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I :只有CaCl2;
猜想II:有
猜想Ⅲ:有CaCl2和Ca(OH)2;
猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
| 实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
| 实验操作 | 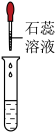 | 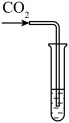 | 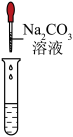 |
| 实验现象 | 产生白色沉淀 | ||
| 实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】
(1) 丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑
【反思交流】
(3) 某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如图所示,请回答下列问题:

①由图可知,在c点处溶液中溶质是
②若要使c点对应的溶液变成b点对应的溶液,需要除去杂质,其中的一种方法是向烧杯中加入过量的
您最近一年使用:0次
【推荐3】氯化铁(FeCl3)溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度氯化铁溶液的催化下,探究氯化铁对不同浓度过氧化氢溶液分解速率的影响。(资料:氯化铁溶液是氯化铁FeCl3和水的混合物,过氧化氢溶液是过氧化氢和水的混合物)
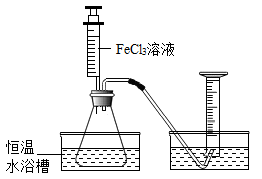
(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的氯化铁溶液,如图所示,通过观察_______________ 可以粗略判断过氧化氢的分解速率,从而得出实验结果。
写出过氧化氢在氯化铁做催化剂时发生反应的文字表达式__________________ 。
(2)为进一步判断上述实验结论的准确性,小刚同学进行了如下实验方案设计:
[方案一] 在不同过氧化氢浓度下,测定收集相同气体所需时间。
[方案二] 在不同过氧化氢浓度下,测定____________________ 。
方案二的实验测量结果
表中X=____________ ,Y= _____________ 。
实验结论:通过测量V1小于V2 ,说明_______________________ 。

(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的氯化铁溶液,如图所示,通过观察
写出过氧化氢在氯化铁做催化剂时发生反应的文字表达式
(2)为进一步判断上述实验结论的准确性,小刚同学进行了如下实验方案设计:
[方案一] 在不同过氧化氢浓度下,测定收集相同气体所需时间。
[方案二] 在不同过氧化氢浓度下,测定
方案二的实验测量结果
| 过氧化氢溶液的浓度和体积 | 2%氯化铁溶液的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) | |
| 实验1 | 8%10 mL | X | 5 | V1 |
| 实验2 | 16%10 mL | 3 | Y | V2 |
表中X=
实验结论:通过测量V1小于V2 ,说明
您最近一年使用:0次