高锰酸钾在生产、生活中有广泛应用。
实验一:实验室制取气体
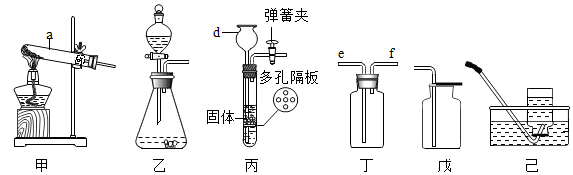
(1)实验室可以用高锰酸钾制取氧气。其反应原理______ (化学方程式表示)选用的发生装置是 ______ (填序号);仪器d的名称是 ______ 。
(2)实验室用丁装置收集二氧化碳气体,气体应从______ (填“e”或“f”端)通入;若要检验收集的气体是否为二氧化碳,需向集气瓶中加入适量澄清石灰水并振荡,该反应的化学方程式为 ______ 。
(3)梁明同学认为乙装置和丙装置类似,都可以用于液体与固体在常温下制取气体的反应。由此他认为实验室用二氧化锰和双氧水制取氧气可用丙装置进行,以便控制反应的发生和停止。刘彬同学经过认真思考后认为梁明同学的看法是错误的。刘彬同学的理由是______ 。
实验二:实验小组对高锰酸钾进行再探究
I.经硫酸酸化的高锰酸钾溶液和草酸(H2C2O4)溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:
资料1:2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。
小明经过分析,否定了假设一,理由是______ 。
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是______ 。这一实验基于的假设是 ______ 。
Ⅱ.【查阅资料】KMnO4溶液呈中性、有腐蚀性。
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表。
实验2:将铜片分别浸泡在4种溶液中进行实验,所得数据如下表。
【解释与结论】
(1)实验1的目的是______ 。
(2)实验2中,通过对比②和④,得出的结论是______ 。
(3)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比______ (填编号)。
(4)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4===5CuSO4+2MnSO4+K2SO4+______ 。
实验一:实验室制取气体

(1)实验室可以用高锰酸钾制取氧气。其反应原理
(2)实验室用丁装置收集二氧化碳气体,气体应从
(3)梁明同学认为乙装置和丙装置类似,都可以用于液体与固体在常温下制取气体的反应。由此他认为实验室用二氧化锰和双氧水制取氧气可用丙装置进行,以便控制反应的发生和停止。刘彬同学经过认真思考后认为梁明同学的看法是错误的。刘彬同学的理由是
实验二:实验小组对高锰酸钾进行再探究
I.经硫酸酸化的高锰酸钾溶液和草酸(H2C2O4)溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:
资料1:2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大,反应加快;温度升高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。
小明经过分析,否定了假设一,理由是
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是
Ⅱ.【查阅资料】KMnO4溶液呈中性、有腐蚀性。
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表。
| KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
| 鸡皮的 变化 | 无明显 变化 | 边缘部分变 为棕黄色 | 全部变 为棕色 | 全部变 为黑色 |
实验2:将铜片分别浸泡在4种溶液中进行实验,所得数据如下表。
编号 | ① | ② | ③ | ④ | |
实验 |
|
|
|
| |
铜片质量/g | 实验 | 0.54 | 0.54 | 0.54 | 0.54 |
18小 | 0.54 | 0.52 | 0.54 | 0.43 | |
【解释与结论】
(1)实验1的目的是
(2)实验2中,通过对比②和④,得出的结论是
(3)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比
(4)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4===5CuSO4+2MnSO4+K2SO4+
更新时间:2019-05-10 13:12:25
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】为探究某塑料的组成元素,设计了实验I和Ⅱ、回答下列问题:
I、制取氧气

(1)写出仪器①名称:______ 。
(2)若用一种暗紫色固体制取O2,发生反应的化学方程式为______ ,发生装置应选择上述装置______ (填标号)。
(3)欲制取干燥的O2,装置合理的连接顺序为:发生装置→C→______ (填标号)。连接装置时,发生装置的出气口应与装置C中______ (填“a”或“b”)端相连。
Ⅱ、组成探究
(4)定性检测(已知:无水CuSO4遇水变蓝色)
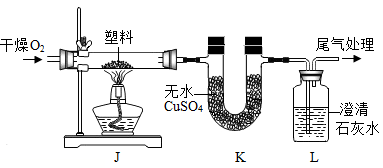
③由上述实验可知,该塑料一定含有的元素是______ (填元素符号)。
(5)定量测定
为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4gCO2和1.8gH2O,依据质量守恒定律,可判断该塑料______ (填“含有”或“不含”)除上述③中结论之外的元素。
I、制取氧气

(1)写出仪器①名称:
(2)若用一种暗紫色固体制取O2,发生反应的化学方程式为
(3)欲制取干燥的O2,装置合理的连接顺序为:发生装置→C→
Ⅱ、组成探究
(4)定性检测(已知:无水CuSO4遇水变蓝色)

| 实验操作 | 实验现象 | 结论 |
| 连接装置,检查气密性,装入试剂并按上图进行实验。通入O2,一段时间后,点燃J处酒精灯。 | 装置K中无水CuSO4变 | 塑料燃烧产物中有H2O |
| 装置L中 | 塑料燃烧产物中有CO2 |
(5)定量测定
为进一步确定组成,将1.4g该塑料在足量O2中完全燃烧,共产生了4.4gCO2和1.8gH2O,依据质量守恒定律,可判断该塑料
您最近一年使用:0次
【推荐2】为做好实验室制取氧气的实验活动和评价,某班级师生讨论并确定如下评价标准。
你是某小组成员,参与完成下列实验活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
小组讨论决定选用A方案,方案对应反应的文字表达式为_____________ 。
(2)进行实验活动。小组同学分工协作完成如下任务
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据下图所提供的仪器,选择_______ 、_______ (填仪器名称)。
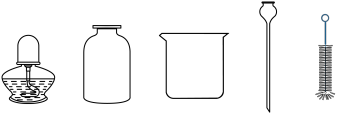
②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末送至试管_____________ (填“中部”或“底部”)后直立试管,抽出纸槽。
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略_____________ 。
④你负责排水法收集氧气。开始收集的时机是_____________ 。收集到两瓶气体,瓶底还残留少量的水,均呈红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用_____________ (填仪器名称)洗涤试管;整理实验台,报告老师后离开实验室。
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是_______ 。
(4)小组用图2装置探究MnO2、CuO对过氧化氢分解的催化效果,设计的方案和记录的数据如下表所示:

①表格中a的值为_______________ 。
②实验1中制取氧气的符号表达式为____________________ 。
③结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是_____________ 。
| 评价标准 |
| 1.是否根据实验条件选择实验方案,并进行可行性论证 |
| 2.是否积极参与实验操作活动,并善于与同学合作 |
| 3.是否规范取用药品,节约药品,保持实验台整洁 |
| 4.是否客观准确记录实验现象,并交流实验成果 |
| 5.是否体验到实验探究活动的乐趣 |
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
小组讨论决定选用A方案,方案对应反应的文字表达式为
(2)进行实验活动。小组同学分工协作完成如下任务
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据下图所提供的仪器,选择

②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末送至试管
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略
④你负责排水法收集氧气。开始收集的时机是
⑤实验结束,待试管冷却,将残余物倒入指定容器,用
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是
(4)小组用图2装置探究MnO2、CuO对过氧化氢分解的催化效果,设计的方案和记录的数据如下表所示:

| 实验序号 | 过氧化氢溶液 | 催化剂 | 收集50mLO2所用时间 |
| 实验1 | 30mL5% | 粉末状MnO2 0.2g | 21s |
| 实验2 | 30mL5% | 粉末状CuO ag | 47s |
②实验1中制取氧气的符号表达式为
③结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】松雷中学化学小组用加热高锰酸钾的方法制取氧气,收集到所需氧气之后,停止加热,同学们对实验后试管内的固体成分产生了兴趣,他们决定从反应后固体成分进行探究:
【猜想与假设】
小姗同学认为:固体可能是锰酸钾、二氧化锰
小俊同学认为:固体可能是高锰酸钾、二氧化锰
【表达与交流】
利用所学的知识分析,小姗同学猜想的理由是_____ 。
【反思与评价】
经讨论后大家一致认为_____ 的猜想不正确,理由是:_____ 。
【解释与结论】
为了证明请你对小姗同学的猜想,小元同学进行了如下实验,取少量反应后的固体于试管中继续加热,然后将_____ ,观察到_____ 现象,证明小姗的猜想不正确,则固体的成分是_____ 。
【总结与归纳】
实验结束后老师带领大家总结,根据此实验在分析反应后固体成分时,需要考虑的物质是:_____ 。
【猜想与假设】
小姗同学认为:固体可能是锰酸钾、二氧化锰
小俊同学认为:固体可能是高锰酸钾、二氧化锰
【表达与交流】
利用所学的知识分析,小姗同学猜想的理由是
【反思与评价】
经讨论后大家一致认为
【解释与结论】
为了证明请你对小姗同学的猜想,小元同学进行了如下实验,取少量反应后的固体于试管中继续加热,然后将
【总结与归纳】
实验结束后老师带领大家总结,根据此实验在分析反应后固体成分时,需要考虑的物质是:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】小丽在学习碳酸钠时做了如下2个实验:
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考分析】应先对废液中的溶质进行探究,再制定方案。
【实验探究】
小丽将所有废液倒入一洁净烧杯中,静置后得到上层清液;取少量清液加入足量的氯化钡溶液(显中性),再滴加几滴无色酚酞溶液,若出现上层清液变红,下层出现沉淀,则上层清液中含有的溶质除氯化钠外,还有____________ ,一定没有的离子有_________ (填离子符号)。
【解决问题】通过以上探究,处理上述废液的正确方法是在废液中加入_________ 直到废液呈中性。
【拓展应用】氢氧化钠溶液敞口放置在空气中会变质生成碳酸钠,请设计实验证明氢氧化钠溶液已全部变质:_____________ 。
| 实验编号 | 实验内容 | 实验现象 | 实验结论 |
| (1) | 碳酸钠溶液+盐酸 | 碳酸钠能与盐酸反应 | |
| (2) | 碳酸钠溶液+澄清石灰水 | 碳酸钠能与氢氧化钙反应 |
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考分析】应先对废液中的溶质进行探究,再制定方案。
【实验探究】
小丽将所有废液倒入一洁净烧杯中,静置后得到上层清液;取少量清液加入足量的氯化钡溶液(显中性),再滴加几滴无色酚酞溶液,若出现上层清液变红,下层出现沉淀,则上层清液中含有的溶质除氯化钠外,还有
【解决问题】通过以上探究,处理上述废液的正确方法是在废液中加入
【拓展应用】氢氧化钠溶液敞口放置在空气中会变质生成碳酸钠,请设计实验证明氢氧化钠溶液已全部变质:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】为探究盐酸的化学性质,某化学小组做了如下实验:
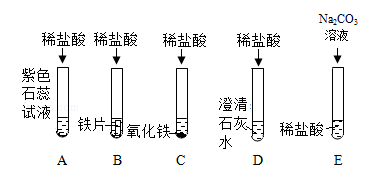
(1)上述反应中无明显现象的为_______________ (填字母序号,下同),有气泡产生的是____________ ;B 试管中所发生反应的化学方程式为____________ 。
(2)将反应后 D 和 E 试管中的废液倒入一洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行 探究。
查阅资料得知:CaCl2+Na2CO3=2NaCl+CaCO3↓;Na2CO3+2HCl=2NaCl+H2O+CO2 。
。
【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl;猜想二:NaCl 和 CaCl2 ;猜想三:NaCl、Ca(OH)2 和 HCl;猜想四:____________ 。
【讨论与交流】经讨论,同学们一致认为猜想____________ 是错误的。
【实验与结论】
【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在____________ 。

(1)上述反应中无明显现象的为
(2)将反应后 D 和 E 试管中的废液倒入一洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行 探究。
查阅资料得知:CaCl2+Na2CO3=2NaCl+CaCO3↓;Na2CO3+2HCl=2NaCl+H2O+CO2
 。
。【提出问题】滤液中溶质的成分是什么?
【假设与猜想】猜想一:NaCl;猜想二:NaCl 和 CaCl2 ;猜想三:NaCl、Ca(OH)2 和 HCl;猜想四:
【讨论与交流】经讨论,同学们一致认为猜想
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四 成立 |
| 取少量滤液于试管中,滴加适量 |
【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】以下是对露置于空气中的生石灰变质的实验探究。
【问题】生石灰用于食品干燥剂,其干燥原理是__________ (用化学方程式表示)。
【实验】该干燥剂主要成分的实验探究,实验过程如下:
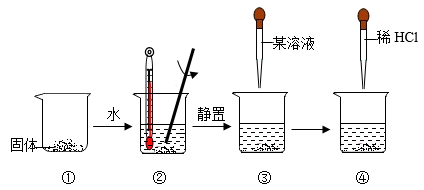
(1)烧杯②中温度计读数不变,则固体中不含__________ 。
(2)烧杯③滴入的“某溶液”可以选择的是__________ (选填序号),a.无色酚酞试液、b.Na2CO3溶液,由现象推知该固体中含有Ca(OH)2:烧杯④中__________ (填现象),固体中还含有CaCO3.
【探究】该固体变质前后组成成分的定量研究。
取一定质量的该固体粉末,滴入足量稀盐酸,将产生气体全部通入足量石灰水中,得到固体15.0g,并将所得溶液蒸干,得到22.2g无水CaCl2。
(3)变质前CaO的质量是__________ g:
(4)固体粉末中Ca(OH)2和CaCO3的质量比为__________ 。
【反思】生石灰需密封保存,目的是与空气中__________ 隔绝,以防变质。
【问题】生石灰用于食品干燥剂,其干燥原理是
【实验】该干燥剂主要成分的实验探究,实验过程如下:

(1)烧杯②中温度计读数不变,则固体中不含
(2)烧杯③滴入的“某溶液”可以选择的是
【探究】该固体变质前后组成成分的定量研究。
取一定质量的该固体粉末,滴入足量稀盐酸,将产生气体全部通入足量石灰水中,得到固体15.0g,并将所得溶液蒸干,得到22.2g无水CaCl2。
(3)变质前CaO的质量是
(4)固体粉末中Ca(OH)2和CaCO3的质量比为
【反思】生石灰需密封保存,目的是与空气中
您最近一年使用:0次