研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
【实验探究】在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH 溶液。实验装置和现象如图所示。请你一起参与。
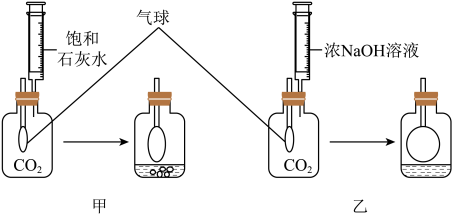
【现象结论】甲装置中产生的实验现象(用化学方程式表示)_____ ,解释通常用石灰水而不用NaOH 溶液检验CO2的原因 _____ ;乙装置中的实验现象是 _____ ,吸收CO2较多的装置是 _____ 。
【计算验证】另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2应该用饱和石灰水。
【思考评价】请你对小李同学的结论进行评价:_____ 。
【实验探究】在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH 溶液。实验装置和现象如图所示。请你一起参与。

【现象结论】甲装置中产生的实验现象(用化学方程式表示)
【计算验证】另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2应该用饱和石灰水。
【思考评价】请你对小李同学的结论进行评价:
更新时间:2019-05-25 18:44:30
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】科学佩戴口罩是预防新冠感染的最有效方法之一,熔喷布是生产一次性口罩的主要原材料。某学习小组为探究熔喷布的元素组成设计了如下实验,回答下列问题:
【提出问题】熔喷布由哪些元素组成?
【查阅资料】①无水硫酸铜为白色粉末,能吸收水分,遇水变蓝;
②熔喷布易燃,只可能由C、H、O中的两种或两种以上元素组成。
【提出猜想】猜想:①由C、H组成;②由H、O组成;③由C、O组成;④由C、H、O组成。
【设计与实验】
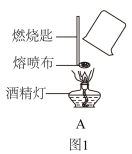
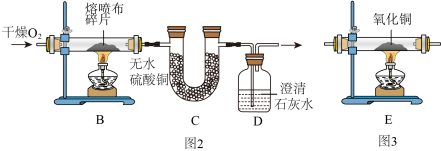
实验一:直接点燃熔喷布(如图1)
(1)甲组同学采用直接点燃熔喷布的方法进行实验,用干冷烧杯、内壁涂澄清石灰水的烧杯分别罩在火焰上方,观察到_____ 的现象,得出:“熔喷布中一定含有碳元素和氢元素”。
(2)乙组同学认为上述实验设计不严谨,理由是_____ 。
实验二:乙组同学对此实验进行改进,在氧气流中加热熔喷布(如图2)
实验步骤:步骤1:连接装置,检查装置的气密性;
步骤2:将m克某熔喷布样品碎片装入玻璃管中,先通入一段时间干燥的氧气,再点燃酒精灯;
步骤3:一段时间后,待样品完全燃烧,无灰分残留;
步骤4:熄灭酒精灯,再持续通一会儿干燥氧气;
步骤5:冷却,称量,装置C增重m1克,装置D增m2克(所加药品均足量)。
(3)“步骤4”中再持续通一会儿干燥氧气的目的是_____ 。
现象与结论:
(4)装置D中溶液变浑浊,发生反应的化学方程式为_____ 。
(5)数据处理:m=_____ (用含m1、m2的式子表示)。
得出结论:猜想①正确。
【实验反思】
(6)经过讨论:大家一致认为在装置C、D之间连接一个如图3所示的装置E会更严谨,理由是_____ 。
【提出问题】熔喷布由哪些元素组成?
【查阅资料】①无水硫酸铜为白色粉末,能吸收水分,遇水变蓝;
②熔喷布易燃,只可能由C、H、O中的两种或两种以上元素组成。
【提出猜想】猜想:①由C、H组成;②由H、O组成;③由C、O组成;④由C、H、O组成。
【设计与实验】


实验一:直接点燃熔喷布(如图1)
(1)甲组同学采用直接点燃熔喷布的方法进行实验,用干冷烧杯、内壁涂澄清石灰水的烧杯分别罩在火焰上方,观察到
(2)乙组同学认为上述实验设计不严谨,理由是
实验二:乙组同学对此实验进行改进,在氧气流中加热熔喷布(如图2)
实验步骤:步骤1:连接装置,检查装置的气密性;
步骤2:将m克某熔喷布样品碎片装入玻璃管中,先通入一段时间干燥的氧气,再点燃酒精灯;
步骤3:一段时间后,待样品完全燃烧,无灰分残留;
步骤4:熄灭酒精灯,再持续通一会儿干燥氧气;
步骤5:冷却,称量,装置C增重m1克,装置D增m2克(所加药品均足量)。
(3)“步骤4”中再持续通一会儿干燥氧气的目的是
现象与结论:
(4)装置D中溶液变浑浊,发生反应的化学方程式为
(5)数据处理:m=
得出结论:猜想①正确。
【实验反思】
(6)经过讨论:大家一致认为在装置C、D之间连接一个如图3所示的装置E会更严谨,理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】实验室有一瓶失去标签的黑色粉末,可能是二氧化锰、碳粉或铁粉其中的一种。为了探究其成分,化学兴趣小组的同学进行了以下探究:
【提出问题】这种黑色粉末是什么呢?
【实验探究】
(1)小组同学讨论发现通过一个简单的物理实验就可以排除一种猜想,他采用的方法是_____ (写出操作即可)。
(2)为了验证另外两种猜想,小组同学设计了以下实验:

提示:A中装有氢氧化钠溶液,可以吸收二氧化碳先向装置中持续通入空气,D处澄清石灰水一直不变浑浊,此操作的目的是_____ ;一段时间后点燃酒精灯,观察到D处澄清石灰水变浑浊,其中B装置的作用是检验A中的反应是否完全,B中的试剂是_____ 。
【实验结论】该黑色粉末是_____ 。
【反思交流】小组同学通过讨论发现还可以设计一个不需要加热,操作更简单的实验来确定该黑色粉末的成分
【提出问题】这种黑色粉末是什么呢?
【实验探究】
(1)小组同学讨论发现通过一个简单的物理实验就可以排除一种猜想,他采用的方法是
(2)为了验证另外两种猜想,小组同学设计了以下实验:

提示:A中装有氢氧化钠溶液,可以吸收二氧化碳先向装置中持续通入空气,D处澄清石灰水一直不变浑浊,此操作的目的是
【实验结论】该黑色粉末是
【反思交流】小组同学通过讨论发现还可以设计一个不需要加热,操作更简单的实验来确定该黑色粉末的成分
| 实验步骤 | 现象 | 结论 |
| 该粉末不是二氧化锰 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】草酸的化学式为H2C2O4,甲、乙两同学对草酸受热分解及其产物的检验做了探究:
【猜想与假设】
第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O;
第四种:草酸分解产物是CO2、CO;
以上哪种猜想不合理________ 。
【查阅资料】无水硫酸铜遇水由白色变成蓝色,碱石灰是一种常用的干燥剂。
【实验设计】(图中铁架台略去)甲同学设计了甲装置,乙同学设计了乙装置。
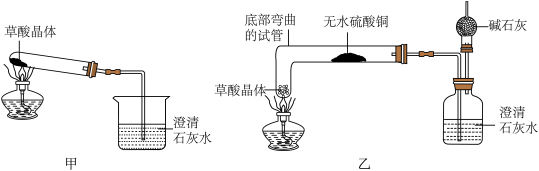
【实验过程】甲同学按甲装置实验,在给草酸晶体加热后,过一会儿观察到澄清石灰水变浑浊;乙同学按乙装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点火能燃烧,乙同学进一步通过实验验证燃烧的气体为CO,他的操作是________ ,现象是________ 。
【实验结论】第________ 种猜想是正确的,请写出草酸受热分解的化学方程式________ 。
【反思与评价】乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈乙装置优于甲装置之处________ 。(答出一点即可)
【猜想与假设】
第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O;
第四种:草酸分解产物是CO2、CO;
以上哪种猜想不合理
【查阅资料】无水硫酸铜遇水由白色变成蓝色,碱石灰是一种常用的干燥剂。
【实验设计】(图中铁架台略去)甲同学设计了甲装置,乙同学设计了乙装置。

【实验过程】甲同学按甲装置实验,在给草酸晶体加热后,过一会儿观察到澄清石灰水变浑浊;乙同学按乙装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点火能燃烧,乙同学进一步通过实验验证燃烧的气体为CO,他的操作是
【实验结论】第
【反思与评价】乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈乙装置优于甲装置之处
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】管道疏通颗粒是一种新型厨卫管道深层清洁产品,主要是针对厨卫管道内的堵塞进行疏通。某小组对某种管道疏通剂[主要成分为Ca(OH)2、铝粉、缓蚀阻垢剂]的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。
查阅资料:
Ca(OH)2与铝粉混合遇水后发生化学反应,放大量热和气体,可加快疏通毛发等物质。
【实验1】
按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
(1)写出Ca(OH)2在生产、生活中的一种用途是______ 。
(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和______ (填实验序号)。
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是______ 。
(4)由实验1可得知:Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为______ 。
【实验2】
其他条件相同时,改变下水管道材料,测定管道疏通颗粒对各种材料的腐蚀率。
实验结果记录如表格:
(5)管道疏通颗粒腐蚀率最低的材料是______ 。
(6)该管道疏通颗粒不宜对______ 材质的下水管道进行疏通。
(7)进行实验2时,需要控制相同的变量有______ (写2条)。
查阅资料:
Ca(OH)2与铝粉混合遇水后发生化学反应,放大量热和气体,可加快疏通毛发等物质。
【实验1】
按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
| 序号 | Ca(OH)2质量/g | 铝粉质量/g | 缓蚀阻垢剂质量/g | 混合前后温度升高值/℃ |
| ① | 1.3 | 0.55 | 0.18 | 63 |
| ② | 1.3 | 0.75 | 0.18 | 78 |
| ③ | 1.3 | 0.95 | 0.18 | 89 |
| ④ | 1.3 | 1.15 | 0.18 | 83 |
| ⑤ | 1.3 | 0.95 | 0.04 | 86 |
| ⑥ | 1.3 | 0.95 | 0.09 | 87 |
| ⑦ | 1.3 | 0.95 | 0.27 | 87 |
(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是
(4)由实验1可得知:Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为
【实验2】
其他条件相同时,改变下水管道材料,测定管道疏通颗粒对各种材料的腐蚀率。
实验结果记录如表格:
| 材料 | 塑料 | 铜 | 铁 | 钢 | 铝 | 铝合金 |
| 腐蚀率 | 0.1% | 0.4% | 0.5% | 0.3% | 100% | 80% |
(6)该管道疏通颗粒不宜对
(7)进行实验2时,需要控制相同的变量有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】氢化镁(化学式为MgH2)是一种常用的焰火剂,某兴趣小组拟选用如图装置制备氢化镁。

[查阅资料]
(1)氢化镁可用氢气与纳米级镁粉加热制得。氢化镁遇水反应生成氢氧化镁[Mg (OH)2]和氢气,并放出热量。.
(2)常温下镁不与水反应,标准状况下氢气的密度为0.09g/L。
实验步骤:
①先连接装置,再……;
②装入药品,打开分液漏斗活塞向装置中通入氢气,D处收集的气体验纯后,给C装置加热。继续通入平稳的氢气流。
③实验结束时,先停止加热,等装置冷却到室温停止通入氢气。
[回答问题]
(1)请将步骤①中的操作补充完整_____ 。
(2)分别写出实验时圆底烧瓶和C处玻璃管中发生反应的化学方程式:____ 、__ 。氢化镁中氢元素的化合价为;__ 价,氢化镁保存时应注意____ 。
(3)兴趣小组活动时,组长特别提醒大家实验开始操作时注意氢气要早通入,酒精灯晚点燃,对这个提醒,你的理解是_____ ,盛放干燥剂的仪器的名称为:______ ,请写出一种可用作本题实验的干燥剂的化学式:_______ 。
(4)实验结束同学们利用如图装置收集氢气测体积,进而计算氢化镁的质量、检测氢化镁的纯度。若未冷却到室温,且导管伸入量筒里太长,也未将导管拿出就读氢气的体积数。则检测的氢化镁的纯度会______ (填“偏大”、“偏小”或“无影响”)。写出Y型管中水与样品接触后发生反应的化学方程式:____ 。


[查阅资料]
(1)氢化镁可用氢气与纳米级镁粉加热制得。氢化镁遇水反应生成氢氧化镁[Mg (OH)2]和氢气,并放出热量。.
(2)常温下镁不与水反应,标准状况下氢气的密度为0.09g/L。
实验步骤:
①先连接装置,再……;
②装入药品,打开分液漏斗活塞向装置中通入氢气,D处收集的气体验纯后,给C装置加热。继续通入平稳的氢气流。
③实验结束时,先停止加热,等装置冷却到室温停止通入氢气。
[回答问题]
(1)请将步骤①中的操作补充完整
(2)分别写出实验时圆底烧瓶和C处玻璃管中发生反应的化学方程式:
(3)兴趣小组活动时,组长特别提醒大家实验开始操作时注意氢气要早通入,酒精灯晚点燃,对这个提醒,你的理解是
(4)实验结束同学们利用如图装置收集氢气测体积,进而计算氢化镁的质量、检测氢化镁的纯度。若未冷却到室温,且导管伸入量筒里太长,也未将导管拿出就读氢气的体积数。则检测的氢化镁的纯度会

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小涛家的下水管道堵了,爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了。小涛对此很好奇,于是想探究“管道通”中的物质成分。
[提出问题]“管道通”中的物质是什么?
[查阅资料]主要内容如下:
(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体。铝与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是____ 。
②铝与氢氧化钠溶液反应能生成偏铝酸钠( NaAlO2)和氢气,化学方程式是______ 。
[猜想与验证]小涛打开一盒“管道通” ,内有一袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
结论:银灰色粉末为铝粉。
[反思]根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)__ 。
[提出问题]“管道通”中的物质是什么?
[查阅资料]主要内容如下:
(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉为银灰色固体。铝与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是
②铝与氢氧化钠溶液反应能生成偏铝酸钠( NaAlO2)和氢气,化学方程式是
[猜想与验证]小涛打开一盒“管道通” ,内有一袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
| 实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在玻璃片上,曝露在空气中一会儿。 | 白色固体颗粒 |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁。 | 试管外壁发烫 |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间。 | 羊毛线逐渐消失。 |
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
| 实验操作 | 实验现象 |
①按照下图安装两套装置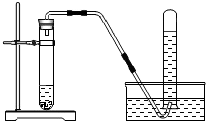 |  |
| ②一套装置中加入银灰色粉末和稀盐酸;另一套装置中加入银灰色粉末和 | 都产生大量无色气体, 试管外壁温度明显升高。 |
| ③待导管口有气泡均匀持续冒出时,分别收集1试管气体,验纯。 | 用拇指堵住试管口,移近酒精灯火焰,松开拇指,发出轻微的 |
| ④在导管口点燃气体。 | 火焰颜色为 |
结论:银灰色粉末为铝粉。
[反思]根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】有白色固体,可能含有CuSO4、Na2CO3、CaCO3、NaOH、NaCl中的一种或几种。将此白色固体溶于足量水中,得到无色溶液。
(1)白色固体中一定不含有的物质是_____ ;原因是_________ 。
(2)若白色固体一定含有氯化钠,请你设计一个实验方案来检验白色固体中还可能含有的物质。提供的试剂有:酚酞溶液、稀硝酸、氯化钡溶液(呈中性)、氢氧化钙溶液
(1)白色固体中一定不含有的物质是
(2)若白色固体一定含有氯化钠,请你设计一个实验方案来检验白色固体中还可能含有的物质。提供的试剂有:酚酞溶液、稀硝酸、氯化钡溶液(呈中性)、氢氧化钙溶液
| 实验操作 | 预期现象与结论 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。某活动小组准备研究某铁红中铁元素的质量分数。
【资料1】草酸晶体(H2C2O4·3H2O)在浓 作用下受热分解,化学方程式为:H2C2O4·3H2O
作用下受热分解,化学方程式为:H2C2O4·3H2O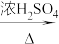 CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是______ (填字母编号)
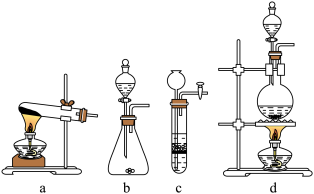
(2)【问题讨论】用图所示装置进行实验:实验前应先______ 。

(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是______ (填字母编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是______ 。
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前______ ,②停止加热后驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰(CaO和NaOH的混合物)吸收。
(6)写出D装置中所发生反应的一个化学方程式______ 。
(7)【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
称取铁红样品10.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为m g,则______ <m<______ 。
②实验前后称得E装置增重6.6 g,则此铁红中铁的质量分数是______ 。
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会______ (填“偏小”、“不变”或“偏大”)。
反思2:请指出【问题讨论】中实验装置的一个明显缺陷______ 。
【资料1】草酸晶体(H2C2O4·3H2O)在浓
 作用下受热分解,化学方程式为:H2C2O4·3H2O
作用下受热分解,化学方程式为:H2C2O4·3H2O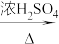 CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O(1)下列可用作草酸分解制取气体的装置是

(2)【问题讨论】用图所示装置进行实验:实验前应先

(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前
(6)写出D装置中所发生反应的一个化学方程式
(7)【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为m g,则
②实验前后称得E装置增重6.6 g,则此铁红中铁的质量分数是
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会
反思2:请指出【问题讨论】中实验装置的一个明显缺陷
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐3】某实验小组的同学在学习了铁的冶炼后,想探究炼铁高炉排放出的高炉气体中含有污染环境的气体有哪些,请我们共同参与探究并回答下列问题:
【提出问题】高炉气体中含有污染环境的气体是什么?
【作出猜想】猜想一:只有CO;
猜想二:只有SO2;
猜想三:CO和SO2都有;
【查阅资料】二氧化硫能使澄清石灰水变浑浊(与CO2相似),能使品红溶液褪色,可被酸性高锰酸钾溶液吸收。
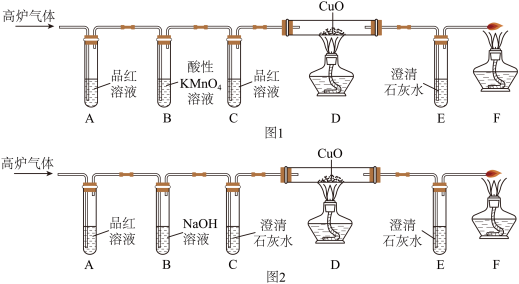
【实验探究】该实验小组的同学组装了如图1装置进行实验。
(1)甲同学在实验中发现A中品红溶液褪色,高炉气体中含有气体_____ ,B中酸性高锰酸钾溶液的作用是_____ ,C 中品红溶液的作用是_____ ;
(2)乙同学发现C中品红溶液没有褪色,E中澄清石灰水变浑浊,得出高炉气体中含有CO.丙同学认为乙同学的结论不正确,理由是_____ 。
(3)该实验小组的同学经过讨论后,改进了实验装置,如图2所示。用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是_____ ,写出SO2与 NaOH溶液反应的化学方程式_____ 。
【实验结论】炼铁厂排放的高炉气体中含有有害气体CO和SO2,直接排放到空气中会污染环境,需达标后才能排放。
【提出问题】高炉气体中含有污染环境的气体是什么?
【作出猜想】猜想一:只有CO;
猜想二:只有SO2;
猜想三:CO和SO2都有;
【查阅资料】二氧化硫能使澄清石灰水变浑浊(与CO2相似),能使品红溶液褪色,可被酸性高锰酸钾溶液吸收。
【实验探究】该实验小组的同学组装了如图1装置进行实验。
(1)甲同学在实验中发现A中品红溶液褪色,高炉气体中含有气体
(2)乙同学发现C中品红溶液没有褪色,E中澄清石灰水变浑浊,得出高炉气体中含有CO.丙同学认为乙同学的结论不正确,理由是
(3)该实验小组的同学经过讨论后,改进了实验装置,如图2所示。用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是
【实验结论】炼铁厂排放的高炉气体中含有有害气体CO和SO2,直接排放到空气中会污染环境,需达标后才能排放。

您最近一年使用:0次



