兴趣小组用100g含碳酸钾6.9%的草木灰样品,制取氢氧化钾用于制作“叶脉书签”。操作过程如下:

(1)100g样品中碳酸钾的质量为________g。
(2)反应后所得滤液中氢氧化钾的质量分数为多少______?(写出计算过程)

(1)100g样品中碳酸钾的质量为________g。
(2)反应后所得滤液中氢氧化钾的质量分数为多少______?(写出计算过程)
更新时间:2019-06-05 08:52:14
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。

【提示】鱼骨中其它成分与盐酸不反应,浓硫酸有吸水性。
(1)根据图中的数据计算鱼骨中碳酸钙的质量分数。(请写出计算过程)
(2)若将装置中的浓硫酸撤掉,则实验后计算得到的碳酸钙的质量分数会______ (填“偏大”、“偏小”或“不变”)

【提示】鱼骨中其它成分与盐酸不反应,浓硫酸有吸水性。
(1)根据图中的数据计算鱼骨中碳酸钙的质量分数。(请写出计算过程)
(2)若将装置中的浓硫酸撤掉,则实验后计算得到的碳酸钙的质量分数会
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】黄铜是铜和锌的合金(Cu-Zn),小明利用一瓶稀盐酸和相关仪器,测定黄铜样品的组成(不考虑其他杂质)。将30mL 稀盐酸分3次加入到10g黄铜粉末中,每次充分反应后,测定本次生成氢气的质量,实验数据如下:
(1)从上表数据分析,小明用 10g 合金共收集到氢气 g
(2)求合金中铜的质量分数。
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(2)求合金中铜的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
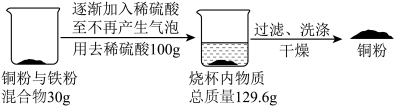
【推荐3】学习小组同学利用下图实验,回收实验室废弃的铜粉与铁粉混合物中的铜粉。_____ g。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数_____ (填“可能”或“不可能”)是15%。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某小组用大理石和稀盐酸制取二氧化碳后,对剩余废液继续探究。取100g实验后的废液样品于烧杯中,向其中逐滴加入10%的氢氧化钠溶液,至恰好完全反应(废液中其它物质不参与反应)时,共消耗氢氧化钠溶液40g。回答下列问题:
(1)计算该废液中稀盐酸的溶质质量分数。
(2)化学兴趣小组的同学们思考后提出,处理该废液有以下多种方法,你认为其中最合理的是_______ (填序号)。
①滴加适量的硝酸银溶液 ②加入过量的熟石灰 ③加入过量的石灰石
(1)计算该废液中稀盐酸的溶质质量分数。
(2)化学兴趣小组的同学们思考后提出,处理该废液有以下多种方法,你认为其中最合理的是
①滴加适量的硝酸银溶液 ②加入过量的熟石灰 ③加入过量的石灰石
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】生铁是由铁和碳组成的合金。某化学兴趣小组的同学为了测定某稀盐酸中溶质的质量分数,取一定量的该生铁样品,分四次加入稀盐酸200g,充分反应后,实验数据如表:
请根据有关信息计算该稀盐酸中溶质的质量分数。
| 次数 | 1 | 2 | 3 | 4 |
| 稀盐酸质量/g | 50 | 50 | 50 | 50 |
| 氢气质量/g | 0.2 | 0.2 | 0.2 | 0.1 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】夏利同学称取18g黄铜(铜锌合金)样品,放入小烧杯中,慢慢加入一定量的稀盐酸,测得稀盐酸的用量与剩余固体的质量关系如图。

请回答下列问题:
(1)黄铜样品中铜的质量为 g,图中m= 。
(2)求所用稀盐酸的溶质质量分数(写出计算过程)。

请回答下列问题:
(1)黄铜样品中铜的质量为 g,图中m= 。
(2)求所用稀盐酸的溶质质量分数(写出计算过程)。
您最近一年使用:0次



