盐化工是我市的一项重点产业,绿色应用是化工生产的发展方向!为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
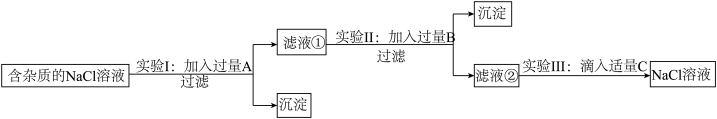
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是____ ;
(2)实验Ⅱ中加入的试剂B是_____ 溶液;
(3)滤液②中除Na+和Cl-外,还含有的离子是____ (填离子符号);
(4)实验Ⅲ中发生的中和反应的化学方程式____ 。

回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是
(2)实验Ⅱ中加入的试剂B是
(3)滤液②中除Na+和Cl-外,还含有的离子是
(4)实验Ⅲ中发生的中和反应的化学方程式
更新时间:2019-06-16 23:13:42
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】以橄榄石尾矿(主要成分MgO、Fe2O3等为原料,生产高纯 的部分工艺流程如下(此流程不考虑其它微量杂质的反应):
的部分工艺流程如下(此流程不考虑其它微量杂质的反应):

(1)过滤时要用的玻璃仪器除漏斗和玻璃棒外还需要______ 。
(2)写出“酸浸”中反应方程式______ (其中一个)。
(3)“酸浸”过程中加入“稍过量盐酸”。盐酸不能加得太多的原因是______ 。
(4)由工艺流程中先“沉铁”后“沉镁”,可推断:氢氧化铁完全沉淀时的pH______ (选填“高于”“低于”“等于”)氢氧化镁完全沉淀时的pH。
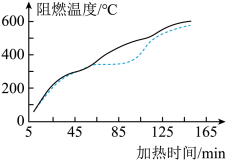
(5)添加了氢氧化镁的沥青有阻燃作用,原理是氢氧化镁受热分解会吸收热量。取同质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图所示。表示阻燃沥青的是______ (选填“虚线”“实线”)。
 的部分工艺流程如下(此流程不考虑其它微量杂质的反应):
的部分工艺流程如下(此流程不考虑其它微量杂质的反应):

(1)过滤时要用的玻璃仪器除漏斗和玻璃棒外还需要
(2)写出“酸浸”中反应方程式
(3)“酸浸”过程中加入“稍过量盐酸”。盐酸不能加得太多的原因是
(4)由工艺流程中先“沉铁”后“沉镁”,可推断:氢氧化铁完全沉淀时的pH
(5)添加了氢氧化镁的沥青有阻燃作用,原理是氢氧化镁受热分解会吸收热量。取同质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图所示。表示阻燃沥青的是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。
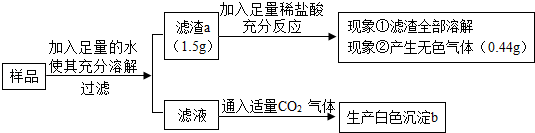
请回答下列问题:
【查阅资料】CO2 不能直接与 BaCl2 和 MgCl2 发生反应。
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒、__________________ 。
(2)滤渣 a 的成分是__________________ ;白色沉淀 b 的成分是__________________ 。
(3)滤渣 a 中加入足量稀盐酸的目的:__________________ 。
(4)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是______ 。

请回答下列问题:
【查阅资料】CO2 不能直接与 BaCl2 和 MgCl2 发生反应。
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒、
(2)滤渣 a 的成分是
(3)滤渣 a 中加入足量稀盐酸的目的:
(4)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐3】A、 B、C、D、E、F分别代表初中化学六种常见的物质。已知: A由一种元素组成,B、C、D、E均由两种元素组成,F由三种元素组成。其中B为黑色固体, C是生活中常用于灭火的物质。它们之间有如下图所示的关系(“一”表示相连的两种物质能在一定条件下发生反应,“→”表示一种物质可以通过一个化学变化转化为另一种物质。其中部分反应物、生成物和反应条件已省略) 。请回答下列问题:
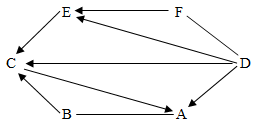
(1)物质A的化学式:_____ ;
(2)请写出E→C的化学方程式:_____

(1)物质A的化学式:
(2)请写出E→C的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙)。某实验小组的同学在粗盐提纯实验中,并把少量可溶性杂质CaCl2,MgCl2一并除去,设计如下实验方案,请回答问题:
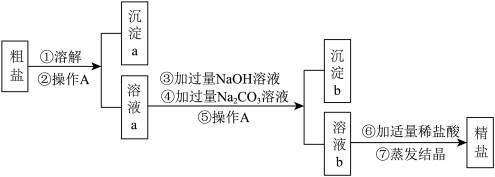
(1)实验操作A的名称是___________________ ;
(2)写出步骤③中发生反应的主要化学方程式_________________ ;沉淀b中含有物质____________ (填化学式);
(3)实验中某同学对溶液b的成分进行了探究。
【提出问题】溶液b中除了含有水和氯化钠外,还含有哪些物质?
【提出猜想】根据实验①②③④⑤的操作后,作出如下猜想。
猜想一:还含有碳酸钠;
猜想二:还含有氢氧化钠;
猜想三:还含有碳酸钠和氢氧化钠。
【验证猜想】
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除去杂质,请写出其中一个反应的化学方程式:________________ 。

(1)实验操作A的名称是
(2)写出步骤③中发生反应的主要化学方程式
(3)实验中某同学对溶液b的成分进行了探究。
【提出问题】溶液b中除了含有水和氯化钠外,还含有哪些物质?
【提出猜想】根据实验①②③④⑤的操作后,作出如下猜想。
猜想一:还含有碳酸钠;
猜想二:还含有氢氧化钠;
猜想三:还含有碳酸钠和氢氧化钠。
【验证猜想】
步骤 | 实验操作 | 实验现象 | 推断 |
1 | 取少量溶液b于试管中,加入过量的氯化钙溶液,振荡,静置 | 溶液b中还含有 | |
2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入 | 溶液b中还含有氢氧化钠 |
【实验结论】经过兴趣小组的实验分析,判断猜想
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤⑥的作用是除去杂质,请写出其中一个反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某校兴趣小组欲利用Mg(OH)2和Cu2O的混合物制备MgCl2和金属铜。该小组设计了如图的实验流程,回答下列有关问题:
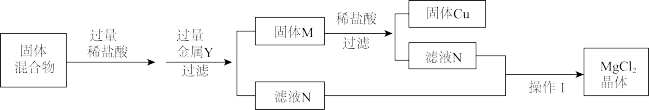
(1)Cu2O是红色固体,它与稀盐酸反应产生红色固体单质和蓝色溶液,则该反应的化学方程式为__ 。
(2)加入过量的金属Y时,发生的化学方程式为____ 。(写1个)固体M的成分____ (填名称)。
(3)MgCl2的溶解度受温度的影响较小,则操作Ⅰ为_____ 。实际操作时会向固体M中加入过量的稀盐酸,这一操作并不会让最终产品MgCl2里出现新杂质,请说明理由____ 。
(4)若混合物中Cu2O的质量为2.88g,则理论上得到Cu的质量为_____ g。
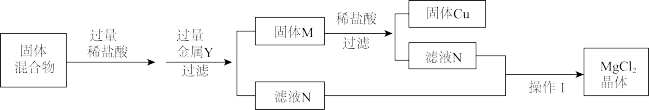
(1)Cu2O是红色固体,它与稀盐酸反应产生红色固体单质和蓝色溶液,则该反应的化学方程式为
(2)加入过量的金属Y时,发生的化学方程式为
(3)MgCl2的溶解度受温度的影响较小,则操作Ⅰ为
(4)若混合物中Cu2O的质量为2.88g,则理论上得到Cu的质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】海洋中有丰富的水生生物和化学物质资源。
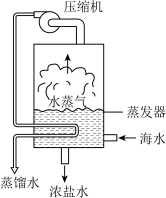
(1)海水淡化获取淡水资源。压汽蒸馏能大大提高热功效率,节约能源。利用压气蒸馏的方法淡化海水的过程如图所示。蒸发器中发生的变化属于______ (填“物理”或“化学”)变化,从微观角度分析,在压缩机内发生变化的是______ 。
(2)海水“晒盐”、“制碱”、“氯碱工业”体现了人类利用化学科学征服和改造自然的智慧。

【流程图一】粗盐的提纯。
①海水“晒盐”得到的粗盐,往往含有不溶性杂质(如泥沙等)和可溶性杂质(如Mg2+、Ca2+等)。工业上以粗盐为原料制取精盐,试剂Ⅰ与试剂Ⅱ的组合为______ (填字母)
A.NaOH B.Ca(OH)2 C.K2CO3 D.Na2CO3
②流程中Mg元素必须转化成______ (填化学式)才能完全除去。
③如果称量Ⅰ中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是______ (填字母)。
A.精盐的产率为103.3% B.蒸发操作中可能有水分没有蒸干
C.除杂过程中有NaCl生成 D.溶解操作中粗盐没有完全溶解
【流程图二】海水的综合利用。
①海水“制碱”工业中,为了提高产率,向饱和NaCl溶液中通入气体时,应先通入的气体是______ (填“NH3”或“CO2”)。
②以电解饱和NaCl溶液为基础制取氯气、氢气和氢氧化钠产品的工业称为“氯碱工业”。它是目前化学工业的重要支柱之一。电解饱和NaCl溶液的化学方程式______ 。该流程中可以循环使用的物质是______ 。
(1)海水淡化获取淡水资源。压汽蒸馏能大大提高热功效率,节约能源。利用压气蒸馏的方法淡化海水的过程如图所示。蒸发器中发生的变化属于

(2)海水“晒盐”、“制碱”、“氯碱工业”体现了人类利用化学科学征服和改造自然的智慧。

【流程图一】粗盐的提纯。
①海水“晒盐”得到的粗盐,往往含有不溶性杂质(如泥沙等)和可溶性杂质(如Mg2+、Ca2+等)。工业上以粗盐为原料制取精盐,试剂Ⅰ与试剂Ⅱ的组合为
A.NaOH B.Ca(OH)2 C.K2CO3 D.Na2CO3
②流程中Mg元素必须转化成
③如果称量Ⅰ中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是
A.精盐的产率为103.3% B.蒸发操作中可能有水分没有蒸干
C.除杂过程中有NaCl生成 D.溶解操作中粗盐没有完全溶解
【流程图二】海水的综合利用。
①海水“制碱”工业中,为了提高产率,向饱和NaCl溶液中通入气体时,应先通入的气体是
②以电解饱和NaCl溶液为基础制取氯气、氢气和氢氧化钠产品的工业称为“氯碱工业”。它是目前化学工业的重要支柱之一。电解饱和NaCl溶液的化学方程式
您最近一年使用:0次



