小红同学将未知浓度的过氧化氢溶液34g,加入盛有0.5g二氧化锰的烧杯中,待完全反应后,称得烧杯中剩余物质的质量为33.7g。计算该过氧化氢溶液中溶质的质量分数。
2019九年级下·青海西宁·学业考试 查看更多[9]
陕西省西安爱知初级中学2022-2023学年九年级上学期期中化学试题山东省烟台市海阳市2020-2021学年八年级下学期期末化学试题山东省济宁市嘉祥县第三中学2020-2021学年九年级上学期12月月考化学试题山东省济宁市经济技术开发区嘉祥县马集镇中学2020-2021学年九年级上学期12月月考化学试题(已下线)【万唯原创】2020年安徽省中考化学面对面卷九年级第二部分专题六(已下线)(海南卷)学科网2020年九年级化学第二次模拟大联考《学科网2020年中考模拟考试》2020中考化学章节强化训练——专题二十一:化学方程式辽宁省营口市大石桥市石佛中学2019-2020学年九年级上学期期中化学试题青海省西宁城区2019年中考化学试题
更新时间:2019-06-27 01:32:47
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】石灰石的主要成分为CaCO3(其余杂质不溶于水,亦不参加反应)。某化学兴趣小组为了测定石灰石中CaCO3的质量分数,进行了以下探究实验:称石灰石样品二份,分别放入大烧杯中,第一个烧杯中加入50克稀盐酸,第二个烧杯中放入100克稀盐酸,充分反应至不再有气泡产生时称量残留物质量,有关数据如下表。求:(1)二个烧杯中CO2的质量;(2)石灰石样品中CaCO3的质量分数;(3)稀盐酸中溶质的质量分数。
| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 样品质量 | 16g | 16 g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 61.6 g | 109.4g |
| 产生的CO2质量 |
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学小组的同学们对一份固体样品进行了探究.通过实验已确定该样品由氧 化铁和铁粉混合而成.他们取了 7.2g 固体样品,用图 1 所示的装置继续实验,测定的部分数据如图 2 所示。
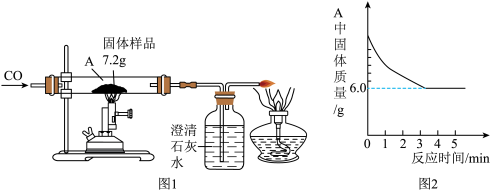
请计算:
(1)写出硬质玻璃管内的实验现象_____;
(2)该样品中含有氧化铁的质量为_____g;
(3)若澄清石灰水足量,反应结束后,装置 B 增重质量为多少?_____(写出具体计算步骤)

请计算:
(1)写出硬质玻璃管内的实验现象_____;
(2)该样品中含有氧化铁的质量为_____g;
(3)若澄清石灰水足量,反应结束后,装置 B 增重质量为多少?_____(写出具体计算步骤)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】同学为了测定某含杂质7%的黄铜(Cu、Zn)样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
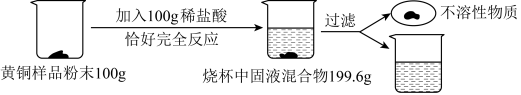
(1)发生反应的化学方程式为______ ;
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为______ ;
(3)反应生成的硫酸锌的质量为______ g;
(4)该黄铜样品中铜的质量分数是______ ;
(5)若工业上用100t含Cu2S80%的辉铜矿炼制上述黄铜样品,转化过程中损失10%,则可得到黄铜的质量为______ t。

(1)发生反应的化学方程式为
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为
(3)反应生成的硫酸锌的质量为
(4)该黄铜样品中铜的质量分数是
(5)若工业上用100t含Cu2S80%的辉铜矿炼制上述黄铜样品,转化过程中损失10%,则可得到黄铜的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如下图所示。另取相同质量的该混合物溶于水得到106.6 g溶液,向该溶液中加入100 g 7.3% 的稀盐酸,恰好完全反应。(已知:2NaHCO3 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)

计算:(1)混合物与盐酸反应生成二氧化碳的质量。
(2)所得溶液中溶质的质量分数。
 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
计算:(1)混合物与盐酸反应生成二氧化碳的质量。
(2)所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某化学兴趣小组为了测定镁铜合金中镁的质量分数,取了该合金样品2.0g并将30稀硫酸分6次加入样品中。充分反应后过滤,称重,得到相关数据如下:
(1) 表格中m的数值为 ________。
(2) 样品中镁的质量分数为 ________ 。
(3) 求所用硫酸溶液中溶质质量分数为_____________。
| 稀硫酸的用量 | 剩余固体质量 | 稀硫酸的用量 | 剩余固体质量 |
| 第一次 5 g | m | 第四次 5 g | 0.8 g |
| 第二次 5 g | 1.4g | 第五次 5 g | 0.6g |
| 第三次 5 g | 1.1g | 第六次 5 g | 0.6g |
(1) 表格中m的数值为 ________。
(2) 样品中镁的质量分数为 ________ 。
(3) 求所用硫酸溶液中溶质质量分数为_____________。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】小明用含碳酸钠的氢氧化钠样品进行了如图所示的实验。请根据图示计算

(1)样品中碳酸钠的质量分数
(2)过滤后滤液中溶质的质量分数

(1)样品中碳酸钠的质量分数
(2)过滤后滤液中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】为了测定某含杂质的碳酸氢钠样品中碳酸氢钠的质量分数(杂质不溶于水,也不与其他物质反应),进行如下实验:

请回答下列问题;
(1)上述实验过程中 发生的化学方程式:______ 。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式______ 。
(3)此碳酸氢钠样品中碳酸氢钠的质量分数______ 。
(4)用36.5%的浓盐酸配制200g,上述稀盐酸,所需浓盐酸的质量为______ g。
(5)若将反应后的滤液蒸发91g水(无晶体析出),所得溶液中溶质的质量分数为______ 。
(6)若要生产106t纯碱,需要上述碳酸氢钠样品的质量为______ t。

请回答下列问题;
(1)上述实验过程中 发生的化学方程式:
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式
(3)此碳酸氢钠样品中碳酸氢钠的质量分数
(4)用36.5%的浓盐酸配制200g,上述稀盐酸,所需浓盐酸的质量为
(5)若将反应后的滤液蒸发91g水(无晶体析出),所得溶液中溶质的质量分数为
(6)若要生产106t纯碱,需要上述碳酸氢钠样品的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
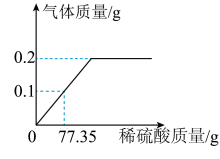
(1)充分反应后,产生氢气的质量为______ g。
(2)原硫酸溶液溶质的质量分数为多少?(写出计算过程)。

(1)充分反应后,产生氢气的质量为
(2)原硫酸溶液溶质的质量分数为多少?(写出计算过程)。
您最近一年使用:0次



