根据所给氯化钠和碳酸钠的溶解度及溶解度曲线的信息,回答下列问题:
温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
氯化钠溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
碳酸钠溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
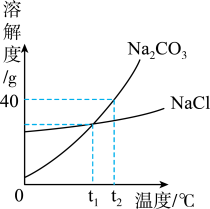
(1)t1℃时,NaCl的溶解度是
(2)t2℃时,将40g Na2CO3固体加入50g水中,充分溶解后所得Na2CO3溶液中溶质与溶剂的质量比为
(3)若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是
2019·山东聊城·中考真题 查看更多[6]
山东省聊城市2019年中考化学试题(已下线)专题04 溶液的形成及其配制 溶解度《备战2020年中考化学真题分类汇编》(山东省)(已下线)【万唯原创】2020年河北省中考化学面对面卷练习册九年级第九单元(已下线)主题 溶液·基础必练2(已下线)【万唯原创】2020年陕西省中考化学试题研究卷填空题及简答题特训2022年山东省惠民县初中学业水平模拟化学试题(二)
更新时间:2019/06/26 21:57:10
|
相似题推荐
【推荐1】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
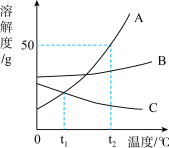
(1)t2℃,A、B、C三种物质的溶解度由大到小的顺序为_______ 。
(2)温度在_______ ℃时,A、C两物质的溶解度相等。
(3)t2℃,将30克A物质投入50克水中充分溶解,所得溶液的质量分数为_______ 。(保留一位小数)
(4)t2℃,等质量的A、B、C分别加水配成饱和溶液,所得溶液的质量由大到小的顺序为___ 。
(5)保持溶液质量不变将A由不饱和溶液变成饱和溶液的方法是:_______ 。
(6)将一盛有饱和C溶液的试管放在盛水的烧杯中,向烧杯中加入氧化钙固体,则试管中的现象_______ ,解释出现该现象的原因_______ 。

(1)t2℃,A、B、C三种物质的溶解度由大到小的顺序为
(2)温度在
(3)t2℃,将30克A物质投入50克水中充分溶解,所得溶液的质量分数为
(4)t2℃,等质量的A、B、C分别加水配成饱和溶液,所得溶液的质量由大到小的顺序为
(5)保持溶液质量不变将A由不饱和溶液变成饱和溶液的方法是:
(6)将一盛有饱和C溶液的试管放在盛水的烧杯中,向烧杯中加入氧化钙固体,则试管中的现象
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是甲、乙、丙三种物质的溶解度曲线,回答下列问题:
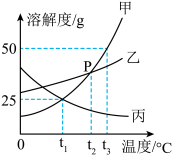
(1)P点表示乙的溶解度_______ 甲的溶解度(选填“大于,小于或者等于”)。
(2)t3℃时,50g甲物质溶解在50g水中,得到溶液的质量是_______ 。
(3)甲、乙、丙三种物质的饱和溶液从t2℃降低到t1℃时,得到的三种物质的质量分数从大到小的顺序是____ 。
(4)要使丙物质的饱和溶液变为不饱和溶液,在不改变物质的组成条件下,应采取的方法是___ 。
(5)下列说法正确的是

(1)P点表示乙的溶解度
(2)t3℃时,50g甲物质溶解在50g水中,得到溶液的质量是
(3)甲、乙、丙三种物质的饱和溶液从t2℃降低到t1℃时,得到的三种物质的质量分数从大到小的顺序是
(4)要使丙物质的饱和溶液变为不饱和溶液,在不改变物质的组成条件下,应采取的方法是
(5)下列说法正确的是
| A.P点是表示在t2℃时,甲、乙的质量分数相等 |
| B.t3℃时,在100g水中最多溶解50g的甲物质 |
| C.t1℃时,在50g水中加入15g物质甲,得到溶液65g |
| D.甲的溶解度大于丙的溶解度 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水和溶液在生产生活中都有着重要的作用。
(1)常用来区分硬水和软水的物质是_________ 。
(2)下列物质溶于水后,溶液温度降低的是( )
A硝酸铵B浓硫酸C食盐D蔗糖
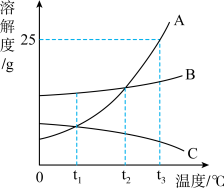
(3)A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
①当温度为_____ ℃时,A、B两种物质的溶解度相同;
②若B中混有少量的A,最好采用______ 的方法提纯B;
③t3℃时将15g A物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是_____ ;
④将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是_____ 。

(1)常用来区分硬水和软水的物质是
(2)下列物质溶于水后,溶液温度降低的是
A硝酸铵B浓硫酸C食盐D蔗糖
(3)A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
①当温度为
②若B中混有少量的A,最好采用
③t3℃时将15g A物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是
④将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是
您最近一年使用:0次
【推荐1】为除去粗盐中混有的泥沙,某学习小组按以下步骤进行实验:
Ⅰ.称量与溶解
Ⅱ.
Ⅲ.蒸发。
请回答下列问题:
(1)将步骤 Ⅱ补充完整___________ 。
(2)如图中图1为氯化钠的溶解度曲线,图2为步骤Ⅰ中的部分操作:
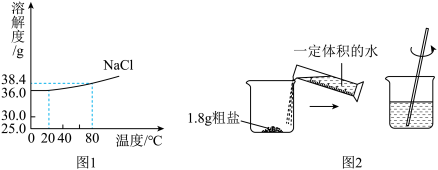
①由图1给出的信息可知:80℃时,NaCl的饱和溶液的溶质质量分数是__ 。(保留0.1%)
②图2中所用水的体积偏多的后果是__________ (填一条即可)
③用玻璃棒搅拌的目的是加速固体溶解,请再写出一种加速溶解的方法___________ 。
(3)过滤时,若漏斗中的滤纸没有紧贴漏斗壁,造成的后果是__ 。(填“过滤慢”或“过滤失败”)
Ⅰ.称量与溶解
Ⅱ.
Ⅲ.蒸发。
请回答下列问题:
(1)将步骤 Ⅱ补充完整
(2)如图中图1为氯化钠的溶解度曲线,图2为步骤Ⅰ中的部分操作:

①由图1给出的信息可知:80℃时,NaCl的饱和溶液的溶质质量分数是
②图2中所用水的体积偏多的后果是
③用玻璃棒搅拌的目的是加速固体溶解,请再写出一种加速溶解的方法
(3)过滤时,若漏斗中的滤纸没有紧贴漏斗壁,造成的后果是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下表是氯化钠和硝酸钾在不同温度时的溶解度。
⑴两种物质中,溶解度受温度影响较大的是______
⑵欲从海水中获得粗盐,可采取_______ 的方法。
⑶在_______________ 温度范围内,氯化钠和硝酸钾的溶解度会相等。
⑷50℃时,100g水中加入40g氯化钠充分搅拌,所得溶液是(填“饱和”或“不饱和”)_______ 溶液,溶液的质量是_______ g。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸钾 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
⑵欲从海水中获得粗盐,可采取
⑶在
⑷50℃时,100g水中加入40g氯化钠充分搅拌,所得溶液是(填“饱和”或“不饱和”)
您最近一年使用:0次
【推荐3】水和水溶液是生产生活中常见的物质。
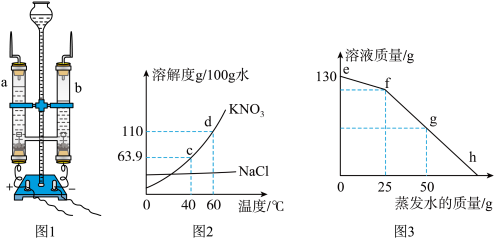
(1)用图1装置可进行电解水实验,电解水的化学方程式是______ ,检验a管中产生的气体常用的方法是______ ,该实验证明水由______ 组成。
(2)KNO3和NaCl的溶解度曲线如图2,回答下列问题:
Ⅰ、c点的含义是______ 。
Ⅱ、60℃时,KNO3饱和溶液的溶质质量分数为______ (列式即可)。
Ⅲ、要使KNO3的不饱和溶液变为饱和溶液,可以采用的方法是______ (只需写出一种方法)。
Ⅳ、KNO3中含有少量NaCl,要提纯KNO3可采用______ 方法。
Ⅴ、60℃时,将130g一定质量分数的KNO3溶液恒温蒸发水,溶液的质量与蒸发水的质量变化关系如图3所示,f点时溶液处于______ 状态(在“饱和”、“不饱和”、“无法确定”中选填)。从图3可以发现同样蒸发25克水,fg段溶液减少的质量明显大于ef段溶液减少的质量,请以图2、图3提供的信息为依据,利用数据说明产生差异的原因______ 。

(1)用图1装置可进行电解水实验,电解水的化学方程式是
(2)KNO3和NaCl的溶解度曲线如图2,回答下列问题:
Ⅰ、c点的含义是
Ⅱ、60℃时,KNO3饱和溶液的溶质质量分数为
Ⅲ、要使KNO3的不饱和溶液变为饱和溶液,可以采用的方法是
Ⅳ、KNO3中含有少量NaCl,要提纯KNO3可采用
Ⅴ、60℃时,将130g一定质量分数的KNO3溶液恒温蒸发水,溶液的质量与蒸发水的质量变化关系如图3所示,f点时溶液处于
您最近一年使用:0次



