为探究CuO和C反应的最佳质量比(忽略副反应),化学兴趣小组取CuO和C的混合物17.2g,按不同的质量比进行实验,实验结果如图所示,横坐标表示混合物中CuO所占的质量分数,纵坐标表示生成物中Cu的质量。

(1)分析可知,CuO和C的最佳质量比对应图中的_____点。
(2)计算a点时,产生CO2的质量_____(写出详细计算过程)。

(1)分析可知,CuO和C的最佳质量比对应图中的_____点。
(2)计算a点时,产生CO2的质量_____(写出详细计算过程)。
2019·湖南永州·中考真题 查看更多[5]
湖南省永州市2019年中考化学试题2020年山东省淄博市临淄区中考一模化学试题(已下线)《单元测试定心卷》第六单元 碳和碳的氧化物(能力提升)-2020-2021学年九年级化学上册单元测试定心卷(人教版)(已下线)考点18 碳的单质-备战2021年中考化学考点天天刷安徽省六安市2022-2023学年九年级上学期期末化学试题
更新时间:2019-07-07 21:37:30
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】实验室常用加热高锰酸钾的方法制氧气。
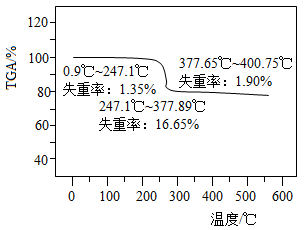
(1)取31.6g高锰酸钾固体充分加热(377.89℃)至质量不再减少,理论上可产生氧气多少克?(写出计算过程)
(2)采用TGA热重分析法(如图)进行该实验,实际测得:相同温度下,固体的失重率为18%。则实际产生的氧气与理论值相差______ g。
(3)产生该差值的可能原因是______ 。

(1)取31.6g高锰酸钾固体充分加热(377.89℃)至质量不再减少,理论上可产生氧气多少克?(写出计算过程)
(2)采用TGA热重分析法(如图)进行该实验,实际测得:相同温度下,固体的失重率为18%。则实际产生的氧气与理论值相差
(3)产生该差值的可能原因是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为测定混有少量氯化钠的碳酸氢钠(NaHCO3)固体的质量分数,现进行如下实验:向盛有13.6g该混合物的烧杯中加入109.5g稀盐酸,恰好完全反应。反应的化学方程式为: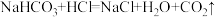 。反应过程中用精密仪器测得烧杯和药品的质量与反应时间的数据记录如表所示:
。反应过程中用精密仪器测得烧杯和药品的质量与反应时间的数据记录如表所示:
求:(1)混合物中NaHCO3的质量分数是_____。
(2)反应后所得溶液中溶质的质量分数为_____(写出计算过程)。
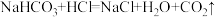 。反应过程中用精密仪器测得烧杯和药品的质量与反应时间的数据记录如表所示:
。反应过程中用精密仪器测得烧杯和药品的质量与反应时间的数据记录如表所示:| 反应时间/min |  |  |  |  |  |  |
| 烧杯和药品的质量/g | 210.0 | 206.7 | 204.6 | 203.9 | 203.4 | 203.4 |
求:(1)混合物中NaHCO3的质量分数是_____。
(2)反应后所得溶液中溶质的质量分数为_____(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】已知CuO被C还原的产物是 Cu2O(红色)。现有 CuO 和木炭粉组成的混合物4.36g,在高温下充分反应后,得到红色固体产物。反应后产生的气体能全部被过量的澄清的石灰水吸收,得沉淀3.00g。试计算所得红色固体产物质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】有一包黑色粉末 9.6g,它由氧化铜和木炭粉混合而成。现将它装入大试管中加热到不再生成红色物质为止,冷却后分离,得到红色铜 4.8g,试计算原混合物中氧化铜的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某研究学习小组为探究木炭还原氧化铜的实验。
(1)氧化铜中铜元素的质量分数为______ 。
(2)要使80g氧化铜完全被还原,需要碳的质量至少是多少?
(3)小组同学将80g氧化铜和8.4g的炭粉在隔绝空气的容器中持续加强热,通过CO2传感器测得容器内CO2的质量变化曲线如图所示。
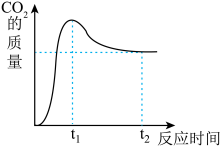
①t1时CO2的质量≤______ 。
②分析t1-t2密闭容器中CO2的质量减少的原因是______ 。
③t2时容器内气体的碳、氧元素质量比为______ 。
(1)氧化铜中铜元素的质量分数为
(2)要使80g氧化铜完全被还原,需要碳的质量至少是多少?
(3)小组同学将80g氧化铜和8.4g的炭粉在隔绝空气的容器中持续加强热,通过CO2传感器测得容器内CO2的质量变化曲线如图所示。

①t1时CO2的质量≤
②分析t1-t2密闭容器中CO2的质量减少的原因是
③t2时容器内气体的碳、氧元素质量比为
您最近一年使用:0次

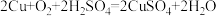 来生产硫酸铜,若要制得80kg硫酸铜。试计算:
来生产硫酸铜,若要制得80kg硫酸铜。试计算:

