请根据下列实验和溶解度曲线回答问题:(已知水的密度约为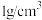 )
)
(1)③中溶液的质量为_____  ;一定属于不饱和溶液的是
;一定属于不饱和溶液的是 _____ (填序号,下同);溶质的质量分数一定相等的是 _____ 。
(2)析出晶体的质量为_____ 。
A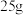 B
B  C
C 
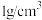 )
)| 实验操作 | 实验结果 |
取 水,加入 水,加入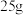 硝酸钾,搅拌,恢复至 硝酸钾,搅拌,恢复至 | 全部溶解,得溶液① |
再加  硝酸钾,搅拌,恢复至 硝酸钾,搅拌,恢复至 | 恰好饱和,得溶液② |
再加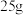 硝酸钾,搅拌,恢复至 硝酸钾,搅拌,恢复至 | 得溶液③ |
| 加热 | 全部溶解, 得溶液④ |
冷却至 | 析出晶体,得溶液⑤ |

(1)③中溶液的质量为
 ;一定属于不饱和溶液的是
;一定属于不饱和溶液的是 (2)析出晶体的质量为
A
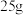 B
B  C
C 
更新时间:2019-05-27 17:36:47
|
相似题推荐
【推荐1】甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答:

(1)t2℃时,甲物质的溶解度是_____ g。
(2)t1℃时,三种物质的溶解度由大到小的排列顺序是_____ 。
(3)P点对应的乙物质溶液是_____ (填“饱和”或“不饱和”)溶液。
(4)在压强为101KPa时,氧气的溶解度随温度变化的趋势与图中_____ 物质相似。

(1)t2℃时,甲物质的溶解度是
(2)t1℃时,三种物质的溶解度由大到小的排列顺序是
(3)P点对应的乙物质溶液是
(4)在压强为101KPa时,氧气的溶解度随温度变化的趋势与图中
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国幅员辽阔,海洋资源丰富。下面是氯化钠、氯化钙的溶解度表以及一体化和利用流程,认真分析,解答问题。
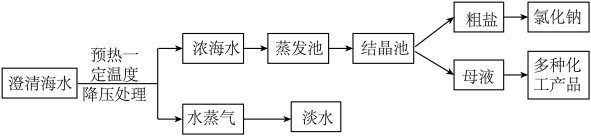
(1)从微观角度解释水蒸气变为淡水的原因:______ 。
(2)析出晶体后的母液是氯化钠的______ (填“饱和”或“不饱和”)溶液。
(3)40℃时,10mL水中最多溶解氯化钙______ g。
(4)得到的粗盐中含有少量 ,除去该物质时发生反应的化学方程式为
,除去该物质时发生反应的化学方程式为______ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |

(1)从微观角度解释水蒸气变为淡水的原因:
(2)析出晶体后的母液是氯化钠的
(3)40℃时,10mL水中最多溶解氯化钙
(4)得到的粗盐中含有少量
 ,除去该物质时发生反应的化学方程式为
,除去该物质时发生反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】t1℃时,将等质量的硝酸钾和氯化钾分别加入到盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。___________ 溶液(填“饱和”或“不饱和”)。
(2)烧杯①中溶解的溶质是___________ 。(写化学式)
(3)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水___________ g。
(4)关于图中烧杯内的物质,下列说法正确的是___________ 。
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)

(2)烧杯①中溶解的溶质是
(3)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水
(4)关于图中烧杯内的物质,下列说法正确的是
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
您最近一年使用:0次
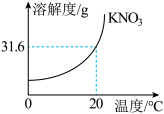
【推荐1】下图为NaCl、KNO3的溶解度曲线和相关的实验,回答下列问题。
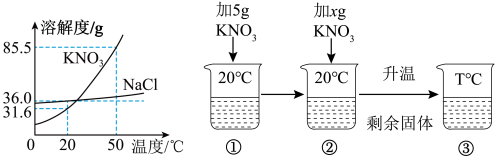
(1)20℃时,将35gKNO3固体加入100g水中充分溶解,所得溶液的质量为__________ g。
(2)除去KNO3溶液中混有的少量杂质NaCl,可采用_______ 的方法提纯KNO3。
(3)在①~③的溶液中,一定是不饱和溶液的是_______ (填序号)。
(4)当x=________ g时,②中溶液恰好没有固体剩余。

(1)20℃时,将35gKNO3固体加入100g水中充分溶解,所得溶液的质量为
(2)除去KNO3溶液中混有的少量杂质NaCl,可采用
(3)在①~③的溶液中,一定是不饱和溶液的是
(4)当x=
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】如图是几种固体物质的溶解度曲线。

(1)80℃时,KCl、NH4Cl与NaNO3的溶解度由大到小依次为______ 。
(2)20℃时,50g水中加入20g NaCl,充分搅拌后,形成______ 溶液(填“饱和”或“不饱和”)。
(3)60℃时,分别将相同质量的NaCl、NH4Cl与KNO3饱和溶液降温至20℃,析出晶体质量最大的是______ 。
(4)60℃时,配制KNO3溶液,其溶质质量分数最高不会超过______ (精确到0.1%)。

(1)80℃时,KCl、NH4Cl与NaNO3的溶解度由大到小依次为
(2)20℃时,50g水中加入20g NaCl,充分搅拌后,形成
(3)60℃时,分别将相同质量的NaCl、NH4Cl与KNO3饱和溶液降温至20℃,析出晶体质量最大的是
(4)60℃时,配制KNO3溶液,其溶质质量分数最高不会超过
您最近一年使用:0次




