氯碱厂电解饱和食盐水溶液制取 的工艺流程示意图如下:
的工艺流程示意图如下:

依据图示完成下列填空:
(1)如果粗盐中 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去 ,该钡试剂可以是
,该钡试剂可以是_____ 。
A B
B 
C D
D 
(2)为了有效地除去 、
、 、
、 ,加入试剂的合理顺序为
,加入试剂的合理顺序为_____ 。
A 先加入 ,后加入
,后加入 ,再加入钡试剂
,再加入钡试剂
B 先加入 ,后加入钡试剂,再加入
,后加入钡试剂,再加入
C 先加入钡试剂,后加入 ,再加入
,再加入
D 先加入 ,后加入钡试剂,再加
,后加入钡试剂,再加
(3)粗盐提纯后,电解精制的饱和食盐水可生产烧碱、氢气和氯气,反应的化学方程式是_____ 。
(4)脱盐工序中,通过加热、浓缩、冷却、过滤的方法除去 ,该方法利用的是
,该方法利用的是 与
与 这两物质在
这两物质在_____ 上的性质差异。
(5)检验脱盐是否完全的实验方法是_____ 。
 的工艺流程示意图如下:
的工艺流程示意图如下:
依据图示完成下列填空:
(1)如果粗盐中
 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去 ,该钡试剂可以是
,该钡试剂可以是A
 B
B 
C
 D
D 
(2)为了有效地除去
 、
、 、
、 ,加入试剂的合理顺序为
,加入试剂的合理顺序为A 先加入
 ,后加入
,后加入 ,再加入钡试剂
,再加入钡试剂B 先加入
 ,后加入钡试剂,再加入
,后加入钡试剂,再加入
C 先加入钡试剂,后加入
 ,再加入
,再加入
D 先加入
 ,后加入钡试剂,再加
,后加入钡试剂,再加
(3)粗盐提纯后,电解精制的饱和食盐水可生产烧碱、氢气和氯气,反应的化学方程式是
(4)脱盐工序中,通过加热、浓缩、冷却、过滤的方法除去
 ,该方法利用的是
,该方法利用的是 与
与 这两物质在
这两物质在(5)检验脱盐是否完全的实验方法是
更新时间:2019-08-27 00:59:36
|
相似题推荐
【推荐1】硝酸钾、氯化钾的溶解度曲线如图1所示。

(1)P点的含义是___________ 。
(2)当氯化钾中混有少量硝酸钾时,可用___________ 方法提纯氯化钾。
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是___________ ,其溶液的溶质质量分数为___________ (结果精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为___________ 。
(5)下列有关说法不正确的是___________ 。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾

(1)P点的含义是
(2)当氯化钾中混有少量硝酸钾时,可用
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为
(5)下列有关说法不正确的是
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】KCl和KNO3的溶解度表及溶解度曲线如图。

(1)KC1和KNO3进行焰色反应,通过蓝色钴玻璃片观察,火焰都呈___________ 色。
(2)甲表示____________ (填“KCl”或“KNO3”)的溶解度曲线。
〔3)b点时乙溶液处于__________ (填“饱和”或“不饱和”)状态。
(4)T2的温度范围是_______________ 。
(5)T2等质量的KC1和KNO3饱和溶液降温至T1,溶剂质量大小关系是KCl__________ KNO3(填“>”、“=”或“<”)。
(6)20°C时在100g水中加入KC1,配制成恰好饱和的KC1溶液,恒温蒸发90g水,析出KCl晶体的质量为__________ g,此时KCl溶液的溶质质量分数为__________ 。

| 温度(℃) | 10 | 20 | 30 | 40 | 50 | |
| 溶解度(g/100g水) | KC1 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 21.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
(2)甲表示
〔3)b点时乙溶液处于
(4)T2的温度范围是
(5)T2等质量的KC1和KNO3饱和溶液降温至T1,溶剂质量大小关系是KCl
(6)20°C时在100g水中加入KC1,配制成恰好饱和的KC1溶液,恒温蒸发90g水,析出KCl晶体的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】“侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱。
NaCl和NH4Cl的溶解度表:
请根据提供的信息,回答问题:
①10℃时,NaCl的溶解度是______ ;
②如 图中,表示NH4Cl的溶解度曲线是_______ (填“A”或“B”)。

③常温20℃时,配制的饱和食盐水的质量分数为_____ ,将食盐水的温度提高,溶液中溶质的质量分数也将提高,而实际生产中往往在常温下进行,这样做的理由是 ____________________ ;
④若NaCl和NH4Cl溶液溶质质量分数相同,表示其溶NaCl和NH4Cl的溶解度曲线图液状态的点在右图中可能位于的区域是_______ (选填I、II、III、IV);
⑤生产中通入氨气及二氧化碳,若要提高这些气体的溶解度,下列做法可行的是______ (选填编号)。
NaCl和NH4Cl的溶解度表:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
①10℃时,NaCl的溶解度是
②如 图中,表示NH4Cl的溶解度曲线是

③常温20℃时,配制的饱和食盐水的质量分数为
④若NaCl和NH4Cl溶液溶质质量分数相同,表示其溶NaCl和NH4Cl的溶解度曲线图液状态的点在右图中可能位于的区域是
⑤生产中通入氨气及二氧化碳,若要提高这些气体的溶解度,下列做法可行的是
A.增大压强 B.升高温度 C.增加水量
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】某活动小组的同学查阅资料得知,传统腌制松花蛋的主要配料是生石灰、纯碱和食盐。小组同学将这三种物质混合后加入适量的水搅拌、过滤得滤渣和滤液,对滤液中溶质的成分进行探究:
【猜想与假设】
甲同学认为:可能是NaCl、Na2CO3、Ca(OH)2
乙同学认为:可能是NaCl、NaOH、Na2CO3
丙同学认为:可能是NaCl、NaOH、Ca(OH)2
丁同学认为:可能是NaCl、NaOH
【交流与评价】
(1)经过讨论,大家一致认为______ 同学的猜想不合理。理由一是__________________ ;理由二是___________________________________________________ 。
【活动与探究】
乙同学取原滤液向其中加入一定量的稀盐酸观察到有大量气泡产生,于是得出该滤液中的溶质是NaCl、NaOH、Na2CO3的结论,证实了自己的猜想。
(2)丙同学取原滤液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原滤液,向其中加入CaCl2溶液观察到________________ ,得出了和乙同学相同的结论.丁同学为了验证上述结论也取原滤液向其中滴加了少量稀盐酸,却发现无气泡产生。
【解释与结论】
(3)大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因.你认为可能的原因是_____________________________________________________ 。经过上述四位同学的共同努力,大家终于对滤液中溶质的成分得出了正确结论。
【应用与拓展】
(4)假设乙同学的猜想是合理的,现只用一种试剂 对滤液进行处理,回收NaCl晶体。请简述其操作过程__________________________________________________ 。
【猜想与假设】
甲同学认为:可能是NaCl、Na2CO3、Ca(OH)2
乙同学认为:可能是NaCl、NaOH、Na2CO3
丙同学认为:可能是NaCl、NaOH、Ca(OH)2
丁同学认为:可能是NaCl、NaOH
【交流与评价】
(1)经过讨论,大家一致认为
【活动与探究】
乙同学取原滤液向其中加入一定量的稀盐酸观察到有大量气泡产生,于是得出该滤液中的溶质是NaCl、NaOH、Na2CO3的结论,证实了自己的猜想。
(2)丙同学取原滤液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原滤液,向其中加入CaCl2溶液观察到
【解释与结论】
(3)大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因.你认为可能的原因是
【应用与拓展】
(4)假设乙同学的猜想是合理的,现
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】现有含氯化镁、氯化钡,氯化铁三种物质的溶液,如果只让钡离子生成沉淀时,需加一种钠的化合物,其化学式为:_____ ;如果要让镁离子和铁离子同时生成沉淀时,需加一种钠的化合物,其化学式____ 。
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】图示中A——F是初中化学常见的物质。按单质、氧化物、酸、碱、盐分类,A、B、C、D、E是五种不同类别的物质,F是大理石的主要成分。图中“--”表示相连的两种物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。请回答:
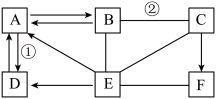
(1)物质F的化学式__________ ;
(2)反应②的化学方程式____________________ ;
(3)反应①的基本反应类型是_____________ ;
(4)E是由两种元素组成的,请写出其的一种用途_______ 。

(1)物质F的化学式
(2)反应②的化学方程式
(3)反应①的基本反应类型是
(4)E是由两种元素组成的,请写出其的一种用途
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】我国海洋资源丰富。如图是从海水中获得一些资源的简易流程图。

【粗盐提纯】除去难溶性杂质后的食盐水中还含有杂质(CaCl2、MgCl2、Na2SO4),得到较纯的氯化钠,进行如下 的流程的实验操作。
(1)第②③步操作中需要的试剂可以用一种试剂替代,此试剂是_____ (填化学式)
(2)在实验室第⑤步操作中需要用到的玻璃仪器有_______ 、玻璃棒和烧杯,其中玻璃棒的作用是
__________ 。
(3)第⑥步操作中,加入适量盐酸的目的是________ 。
【海水制碱】工业上电解饱和食盐水能获得烧碱、氯气和另一种可燃性气体
(4)配置氯化钠饱和溶液。已知常温下氯化钠溶解度为 36.0g,现要将 125g、20%的氯化钠溶液配成饱和溶液,仅需加氯化钠_____ g;配好的溶液溶质质量分数为____ (精确到 0.1%)
(5)写出电解饱和食盐水的化学反应方程式_____________ 。

【粗盐提纯】除去难溶性杂质后的食盐水中还含有杂质(CaCl2、MgCl2、Na2SO4),得到较纯的氯化钠,进行如下 的流程的实验操作。
(1)第②③步操作中需要的试剂可以用一种试剂替代,此试剂是
(2)在实验室第⑤步操作中需要用到的玻璃仪器有
(3)第⑥步操作中,加入适量盐酸的目的是
【海水制碱】工业上电解饱和食盐水能获得烧碱、氯气和另一种可燃性气体
(4)配置氯化钠饱和溶液。已知常温下氯化钠溶解度为 36.0g,现要将 125g、20%的氯化钠溶液配成饱和溶液,仅需加氯化钠
(5)写出电解饱和食盐水的化学反应方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】<汉代古火井碑序>记载:“诸葛丞相躬莅视察,改进技法,刳班竹以导气,引井火以煮盐”。
(1)“刳斑竹以导气”中的“气”指天然气,请写出天然气完全燃烧的化学方程式_______ 。
(2)“引井火以煮盐”中的“盐”指食盐。某氯化钠样品中含有CaCl2、MgCl2、NaSO4,等可溶性杂质,将样品溶解后进行下列操作:①加过量的Ba(OH)2溶液;②加过量的Na2CO3溶液;③____ (填操作名称);④加过量盐酸;⑤蒸发结晶。请设计实验验证进行操作④之前所得溶液中除氯化钠外的其他溶质____ 。(写出步骤、现象和结论)
(1)“刳斑竹以导气”中的“气”指天然气,请写出天然气完全燃烧的化学方程式
(2)“引井火以煮盐”中的“盐”指食盐。某氯化钠样品中含有CaCl2、MgCl2、NaSO4,等可溶性杂质,将样品溶解后进行下列操作:①加过量的Ba(OH)2溶液;②加过量的Na2CO3溶液;③
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】海水“晒盐”得到的粗盐中,除了含有泥沙等不溶性杂质外,还含有氯化镁、氯化钙、硫酸钠等可溶性杂质,要得到较纯净的氯化钠晶体,需进行提纯。某兴趣小组称取7.2g粗盐,在室温下,设计如下实验流程进行提纯。请回答下列问题

资料显示:20℃时氯化钠的溶解度为36g。
(1)步骤I用_____ mL水溶解最合理。
(2)在混合液1中加入的物质有:①过量的碳酸钠溶液、②过量的氢氧化钠溶液、③过量的氯化钡溶液,加入的正确顺序是(用序号表示)_____ 。
(3)实验的各步骤中都必需用到的一种玻璃仪器是_____ ,步骤II的实验操作是_____ 。
(4)步骤Ⅲ中所加试剂X是_____ (填名称)。
(5)工业上电解饱和氯化钠溶液可制得烧碱,同时还有氯气和氢气生成。该反应的化学方程式为_____ 。

资料显示:20℃时氯化钠的溶解度为36g。
(1)步骤I用
(2)在混合液1中加入的物质有:①过量的碳酸钠溶液、②过量的氢氧化钠溶液、③过量的氯化钡溶液,加入的正确顺序是(用序号表示)
(3)实验的各步骤中都必需用到的一种玻璃仪器是
(4)步骤Ⅲ中所加试剂X是
(5)工业上电解饱和氯化钠溶液可制得烧碱,同时还有氯气和氢气生成。该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】海水通过晒制可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是实验室模拟粗盐制备精盐的过程。
①步骤一:去除粗盐中的泥沙
Ⅰ.称取粗盐样品10.0g,用蒸馏水充分溶解; Ⅱ.过滤去除泥沙得溶液A;
以上两步操作中均需要使用到玻璃棒,过滤时玻璃棒的作用是_____ 。
②步骤二:去除粗盐中的可溶性杂质

Ⅰ.加入“过量Na2CO3溶液”时,发生反应的化学方程式______ 。
Ⅱ.理论上用过量的____ 溶液(填一种物质)代替NaOH和BaCl2两种溶液,也可以达到相同实验目的。
Ⅲ.为了证明所加的盐酸已过量,某同学取少量溶液B,向其中加入_____ (填一种试剂),若产生_____ (填实验现象),则证明盐酸已过量。
③步骤三:获得产品
将溶液B注入______ (填仪器名称)中,在不断搅拌下加热,观察到大量晶体析出时,停止加热,利用余热蒸干。最终得到精盐9.4g。
④步骤四:数据处理
该粗盐样品中,氯化钠的质量分数为94%。
【结果与反思】实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是______ 。
①步骤一:去除粗盐中的泥沙
Ⅰ.称取粗盐样品10.0g,用蒸馏水充分溶解; Ⅱ.过滤去除泥沙得溶液A;
以上两步操作中均需要使用到玻璃棒,过滤时玻璃棒的作用是
②步骤二:去除粗盐中的可溶性杂质

Ⅰ.加入“过量Na2CO3溶液”时,发生反应的化学方程式
Ⅱ.理论上用过量的
Ⅲ.为了证明所加的盐酸已过量,某同学取少量溶液B,向其中加入
③步骤三:获得产品
将溶液B注入
④步骤四:数据处理
该粗盐样品中,氯化钠的质量分数为94%。
【结果与反思】实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐2】海洋资源十分丰富:
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的 Ba(OH)2 溶液;b.加入过量碳酸钠溶液;c.加入适量盐酸d.过滤;e.蒸发.正确的操作顺序是_____ (填字母).加 Na2CO3 溶 液的作用是除去 _____ .
(2)晒盐后得到的卤水中含有 MgCl2、KCl 和 MgSO4 等物质,如图是它们的溶解度曲线示意图.设 t1℃时 MgCl2、KCl 和 MgSO4 三种物质的溶解度分别为 a、b、c, 则它们的大小关系为_____ .
(3)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是_______ .
(4)海底矿产资源“可燃冰”的主要成分是水合甲烷晶体(CH4•nH2O),若水合甲烷晶体中 CH4 的质量分数为 10%,则水合甲烷晶体的化学式为______ .甲烷燃烧的化学方程式是 _______ .

(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的 Ba(OH)2 溶液;b.加入过量碳酸钠溶液;c.加入适量盐酸d.过滤;e.蒸发.正确的操作顺序是
(2)晒盐后得到的卤水中含有 MgCl2、KCl 和 MgSO4 等物质,如图是它们的溶解度曲线示意图.设 t1℃时 MgCl2、KCl 和 MgSO4 三种物质的溶解度分别为 a、b、c, 则它们的大小关系为
(3)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是
(4)海底矿产资源“可燃冰”的主要成分是水合甲烷晶体(CH4•nH2O),若水合甲烷晶体中 CH4 的质量分数为 10%,则水合甲烷晶体的化学式为

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】氯化钠和氯化镁是重要的化工原料.某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计如图实验方案:

请回答下列问题:
(1)步骤①溶解过程中用玻璃棒搅拌的目的是_____ 。
(2)步骤④⑤的顺序颠倒会引发的后果是_____ 。
(3)滤液乙中所含的溶质除氯化钠外还含有_____ ;沉淀B中除含碳酸钙、碳酸钡外还含有_____ ;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?_____ 原因是_____ 。
(4)写出步骤⑨中反应的化学方程式_____ .属于_____ 反应(填基本反应类型)。
(5)实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有_____ 个。

请回答下列问题:
(1)步骤①溶解过程中用玻璃棒搅拌的目的是
(2)步骤④⑤的顺序颠倒会引发的后果是
(3)滤液乙中所含的溶质除氯化钠外还含有
(4)写出步骤⑨中反应的化学方程式
(5)实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有
您最近一年使用:0次



