现有一包白色粉末,可能由 、
、 、
、 、
、 、
、 、
、 中的一种或几种组成。现做如下实验:①取适量白色粉末与熟石灰混匀、共热,没有任何异味产生;②取少量粉末,加水溶解得无色溶液,③另取少量粉末,滴加稀盐酸,无明显现象;④另取少量粉末按图12-2所示流程进行实验。
中的一种或几种组成。现做如下实验:①取适量白色粉末与熟石灰混匀、共热,没有任何异味产生;②取少量粉末,加水溶解得无色溶液,③另取少量粉末,滴加稀盐酸,无明显现象;④另取少量粉末按图12-2所示流程进行实验。
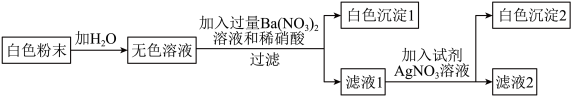
(1)原粉末的成分是___________ ;滤液2中溶质的成分可能有 ___________ 种情况,其中一定含有 ______________________ ,可能含有 ____________ 。
(2)上述实验中,无色溶液中加入的 溶液不能用
溶液不能用 溶液取代,原因是
溶液取代,原因是 ________ 。
(3)上述实验中,无色溶液中加入的 溶液不能用
溶液不能用 或
或 溶液取代,原因是
溶液取代,原因是 __________________ 。
 、
、 、
、 、
、 、
、 、
、 中的一种或几种组成。现做如下实验:①取适量白色粉末与熟石灰混匀、共热,没有任何异味产生;②取少量粉末,加水溶解得无色溶液,③另取少量粉末,滴加稀盐酸,无明显现象;④另取少量粉末按图12-2所示流程进行实验。
中的一种或几种组成。现做如下实验:①取适量白色粉末与熟石灰混匀、共热,没有任何异味产生;②取少量粉末,加水溶解得无色溶液,③另取少量粉末,滴加稀盐酸,无明显现象;④另取少量粉末按图12-2所示流程进行实验。
(1)原粉末的成分是
(2)上述实验中,无色溶液中加入的
 溶液不能用
溶液不能用 溶液取代,原因是
溶液取代,原因是 (3)上述实验中,无色溶液中加入的
 溶液不能用
溶液不能用 或
或 溶液取代,原因是
溶液取代,原因是
更新时间:2019-08-26 10:46:51
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A~H是初中化学常见的物质,A、B、C、D、E属于不同类别(指单质、氧化物、酸、碱、盐)物质。已知D是铁锈的主要成分,B、E常用于配制农药“波尔多液”。它们之间有如图所示的转化关系(“—”表示两种物质可以反应,“→”表示两种物质可以一步转化,部分反应物、生成物略去)。请回答:

(1)D的化学式为_______ 。
(2)请写出F与H反应的化学方程式:_______ 。

(1)D的化学式为
(2)请写出F与H反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】水钻矿中除SiO2外,还有CoO、Fe2O3、CaO、MgO,从水钻矿中提取钻(Co)的预处理步骤如下:

(1)写出步骤①中发生反应的一个化学方程式:_____________________ ;
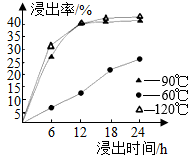
(2)步骤①在一定浓度的稀硫酸中钻的浸出率随时间和温度的变化如下图所示,考虑生产成本及效率,最佳的浸出温度是___________ ,最佳的浸出时间是____________ ;
(3)滤液A中大量存在______________ 种阳离子;
(4)步骤②)除去的金属离子主要是______________ ;
(5)步骤③中通过复分解反应将Ca2+和Mg2+转化成_______________ (填化学式)沉淀被除去;
(6)滤液B中大量存在的金属离子是Co2+和_____________ (填化学符号)。

(1)写出步骤①中发生反应的一个化学方程式:
(2)步骤①在一定浓度的稀硫酸中钻的浸出率随时间和温度的变化如下图所示,考虑生产成本及效率,最佳的浸出温度是

(3)滤液A中大量存在
(4)步骤②)除去的金属离子主要是
(5)步骤③中通过复分解反应将Ca2+和Mg2+转化成
(6)滤液B中大量存在的金属离子是Co2+和
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
【推荐3】已知A~G是初中化学常见的物质,A、B、C、E、F属于不同类别的物质,G溶液呈 黄色,A与C反应产生白色沉淀(微溶物不列为沉淀),它们相互间发生反应或转化 的关系如图所示(“﹣”表示两种物质间能发生反应,“→”表示两种物质间的转化 关系,部分反应物、生成物和反应条件已经略去).

(1)A、F的化学式分别为_____ ,_____ ;
(2)B与E反应的化学方程式为_____ ,其反应的基本反应类型为_____ ;G→D的化学方程式为_____ ;
(3)A→D反应的实验现象为_____ .

(1)A、F的化学式分别为
(2)B与E反应的化学方程式为
(3)A→D反应的实验现象为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】有一包白色固体样品,可能含有NaCl、Na2CO3, (NH4)2SO4、 BaCl2、Na2SO4中的一种或几种,为分析其组成,进行如下实验:
①取适量样品与熟石灰混匀、研磨,没有任何异味产生。
②另取适量样品加入足量水,搅拌、静置、过滤,得到白色沉淀和无色滤液。
③取步骤②中的白色沉淀,加入过量稀盐酸,产生大量气泡,白色沉淀全部消失。
根据以上实验回答下列问题:
(1)样品中一定含有_____ ,一定不含有_________________ 。
(2)步骤②中反应的化学方程式为______________________ 。
(3)步骤②中的滤液,其组成有_____ 种可能,如要确定该滤液的组成,需要用到的一种试剂是______________ (填化学式)。
①取适量样品与熟石灰混匀、研磨,没有任何异味产生。
②另取适量样品加入足量水,搅拌、静置、过滤,得到白色沉淀和无色滤液。
③取步骤②中的白色沉淀,加入过量稀盐酸,产生大量气泡,白色沉淀全部消失。
根据以上实验回答下列问题:
(1)样品中一定含有
(2)步骤②中反应的化学方程式为
(3)步骤②中的滤液,其组成有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸亚铁是一种重要的补铁剂。实验室以表面有油污的废铁屑(主要成分是铁,含少量Fe2O3)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的流程如下:

【资料】①铁与硫酸铁反应的化学方程式为Fe + Fe2(SO4)3 = 3FeSO4
②硫酸亚铁晶体能溶于水,不溶于酒精。
(1)“碱洗”的目的是______ 。
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。
①写出铁与稀硫酸反应的化学方程式______ 。
②所用硫酸溶液浓度不能太稀,原因是浓度太稀会导致反应速率慢、______ 。
③废铁屑中的少量Fe2O3不需要进行除杂处理,原因是______ 。
(3)“结晶”的相关操作依次为:______ 、降温结晶。
(4)“过滤”后用酒精洗涤硫酸亚铁晶体的优点______ (写一点)。

【资料】①铁与硫酸铁反应的化学方程式为Fe + Fe2(SO4)3 = 3FeSO4
②硫酸亚铁晶体能溶于水,不溶于酒精。
(1)“碱洗”的目的是
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。
①写出铁与稀硫酸反应的化学方程式
②所用硫酸溶液浓度不能太稀,原因是浓度太稀会导致反应速率慢、
③废铁屑中的少量Fe2O3不需要进行除杂处理,原因是
(3)“结晶”的相关操作依次为:
(4)“过滤”后用酒精洗涤硫酸亚铁晶体的优点
您最近一年使用:0次




