我国化工专家侯德榜的“侯氏制碱法”曾获世博会金奖。有关反应的原理为:
 ;
;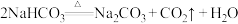 。
。
(1)某碱厂生产纯碱的工艺流程可简单表示如下,下列有关叙述正确的是___________ 。
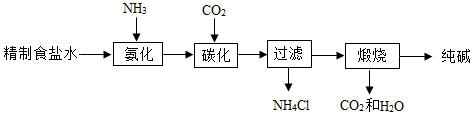
A.先通入氨气使溶液呈碱性可促进对 的吸收
的吸收
B.过滤后获得的滤液中溶质只有
C.在过滤后的滤液中通入氨气可提高析出铵盐的纯度
D..上述流程中可以循环利用的物质只有水和二氧化碳
(2)某校学生设计了如图(2)所示装置,模拟“侯氏制碱法”,获得碳酸氢钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且两者均已达到饱和。
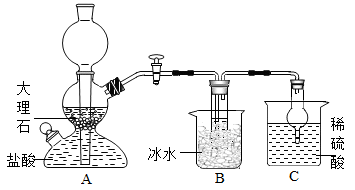
①C装置中稀硫酸的作用是吸收从B装置中的试管内逸出的氨气减少污染,使用球形干燥管的目的是__________ 。
②B装置中使用冰水有利于碳酸氢钠析出,是因为__________ 。
③该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A与B装置之间连接一个盛有饱和 溶液的洗气瓶,其作用是
溶液的洗气瓶,其作用是________ 。
(3)某同学为了测定该碱厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的纯度即质量分数不低于99.2%),设计了如下两种实验方案:
①方案一:用沉淀法测定纯碱样品纯度称取样品10.65g,加水完全溶解向其中加入足量的氯化钡溶液(杂质不与氯化钡反应),充分反应后,过滤、洗涤,干燥得固体19.70g。沉淀试剂用 代替
代替 ,可减小测定误差,原因是
,可减小测定误差,原因是_____ .测得纯碱样品纯度为_______ ;结论是__________ 。
②方案二:用如图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。实验后同学们发现所测的碳酸钠的纯度偏低,造成此结果的原因可能是_____________ (装置的气密性良好)
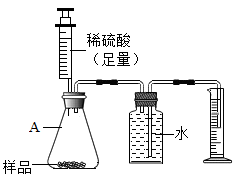
 ;
;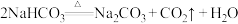 。
。(1)某碱厂生产纯碱的工艺流程可简单表示如下,下列有关叙述正确的是

A.先通入氨气使溶液呈碱性可促进对
 的吸收
的吸收B.过滤后获得的滤液中溶质只有

C.在过滤后的滤液中通入氨气可提高析出铵盐的纯度
D..上述流程中可以循环利用的物质只有水和二氧化碳
(2)某校学生设计了如图(2)所示装置,模拟“侯氏制碱法”,获得碳酸氢钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且两者均已达到饱和。

①C装置中稀硫酸的作用是吸收从B装置中的试管内逸出的氨气减少污染,使用球形干燥管的目的是
②B装置中使用冰水有利于碳酸氢钠析出,是因为
③该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A与B装置之间连接一个盛有饱和
 溶液的洗气瓶,其作用是
溶液的洗气瓶,其作用是(3)某同学为了测定该碱厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的纯度即质量分数不低于99.2%),设计了如下两种实验方案:
①方案一:用沉淀法测定纯碱样品纯度称取样品10.65g,加水完全溶解向其中加入足量的氯化钡溶液(杂质不与氯化钡反应),充分反应后,过滤、洗涤,干燥得固体19.70g。沉淀试剂用
 代替
代替 ,可减小测定误差,原因是
,可减小测定误差,原因是②方案二:用如图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。实验后同学们发现所测的碳酸钠的纯度偏低,造成此结果的原因可能是

更新时间:2019-08-26 10:46:51
|
相似题推荐
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐1】我国有较长的海岸线,海水综合利用对促进经济发展有重要意义,下图是海水综合利用的流程示意图,请回答相关问题。

(1)从海水中获得粗盐的化学原理是_______ 。第①步除去粗盐中的 、Ca2+、Mg2+等杂质,常用到盐酸、NaOH溶液、Na2CO3溶液、BaCl2溶液四种试剂。可先加入过量NaOH溶液,再加入过量的
、Ca2+、Mg2+等杂质,常用到盐酸、NaOH溶液、Na2CO3溶液、BaCl2溶液四种试剂。可先加入过量NaOH溶液,再加入过量的_______ 溶液,_______ 溶液,经过滤后滴加适量的盐酸,蒸发,可得到纯净的氯化钠。
(2)第②和③步中涉及的反应基本类型有_______ 。
(3)食盐是重要的化工原料,氨碱法制纯碱的工业流程如下:

在步骤I中通入氨气的作用是_______ ,请写出步骤II中发生反应的化学方程式_______ 。
(4)从海水中提取溴常用吹出法,即用氯气(C12)将海水里溴化钠(NaBr)中的溴置换出来,再用空气吹出溴(Br2)。流程示意图如下:

①写出氯气从NaBr中置换出溴单质的化学方程式_______ 。
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应:Br2+SO2+2H2O=H2SO4+2HBr)。根据流程图分析,通入SO2和H2O的目的是_______ 。

(1)从海水中获得粗盐的化学原理是
 、Ca2+、Mg2+等杂质,常用到盐酸、NaOH溶液、Na2CO3溶液、BaCl2溶液四种试剂。可先加入过量NaOH溶液,再加入过量的
、Ca2+、Mg2+等杂质,常用到盐酸、NaOH溶液、Na2CO3溶液、BaCl2溶液四种试剂。可先加入过量NaOH溶液,再加入过量的(2)第②和③步中涉及的反应基本类型有
(3)食盐是重要的化工原料,氨碱法制纯碱的工业流程如下:

在步骤I中通入氨气的作用是
(4)从海水中提取溴常用吹出法,即用氯气(C12)将海水里溴化钠(NaBr)中的溴置换出来,再用空气吹出溴(Br2)。流程示意图如下:

①写出氯气从NaBr中置换出溴单质的化学方程式
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应:Br2+SO2+2H2O=H2SO4+2HBr)。根据流程图分析,通入SO2和H2O的目的是
您最近一年使用:0次
【推荐2】海洋是一个巨大的资源宝库,可以从海水中制得粗盐,以粗盐水为原料综合利用的部分途径如下图所示:

(1)为除去粗盐水中的CaCl2、MgCl2和Na2SO4杂质,加入下列3种过量试剂的顺序依次可以是___________(填字母序号);
(2)按加入试剂的正确顺序,过滤后的滤液A中溶质有___________ (填化学式)。
(3)写出生成碳酸氢钠的化学方程式___________ ;在该流程中,是先向饱和食盐水中通入过量的氨气,然后再通入过量的二氧化碳,先通入过量氨气的目的是___________ 。
(4)若向分离出NaHCO3晶体后的母液B(含有NH4C1)中加入过量Ca(OH)2,则可获得一种可以循环使用的物质,其化学式是___________ 。工业上氨碱法制纯碱的优点是___________ ,___________ ,缺点是___________ 。

(1)为除去粗盐水中的CaCl2、MgCl2和Na2SO4杂质,加入下列3种过量试剂的顺序依次可以是___________(填字母序号);
| A.Na2CO3、NaOH、BaCl2 | B.BaCl2、Na2CO3、NaOH | C.NaOH、BaCl2、Na2CO3 |
(3)写出生成碳酸氢钠的化学方程式
(4)若向分离出NaHCO3晶体后的母液B(含有NH4C1)中加入过量Ca(OH)2,则可获得一种可以循环使用的物质,其化学式是
您最近一年使用:0次



