铁暴露在空气中会生锈、不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好像是生了“锈”一样、某化学活动小组对此进行了探究
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次
观察到下列实验现象、请你将他们设计的可行的实验探究方案,填写在下表中:
【得出结论】___________________________________________
【反思与评价】
(1)在②一⑤四种猜想中,你认为猜想_________ (填代号)最不合理,理由是___________ 。
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是_________ 。
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施_______ 。
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的二种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次
观察到下列实验现象、请你将他们设计的可行的实验探究方案,填写在下表中:
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象 | 果肉表面不变色 |
| 猜想② | 将一小块苹果果肉放入盛有氧气的集气瓶中,观察现象 | 果肉表面变色 |
| 猜想③ | 将一小块苹果果肉放入盛有氮气的集气瓶中,观察现象 | 果肉表面不变色 |
| 猜想④ | 将一小块苹果果肉放入盛有二氧化碳的集气瓶中,观察现象 | 果肉表面不变色 |
| 猜想⑤ | 温度高的先变色 |
【得出结论】
【反思与评价】
(1)在②一⑤四种猜想中,你认为猜想
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施
更新时间:2019-09-18 16:21:31
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】硝酸是一种常见的酸,它与稀盐酸、稀硫酸化学性质是否完全相同呢?某化学小组
对此很感兴趣,向老师提出探究硝酸的化学性质,老师高兴答应并带领同学们进行了
硝酸某些化学性质的实验探究。
【猜想与假设】(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变成______ 色。
(2)将Zn片投入稀硝酸中,预计将产生氢气。
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B。
【提出问题】(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成氢气。
(2)硝酸具有强氧化性,能使有色物质褪色。
(3)氮元素某些气态化合物的某些性质如下表:
【交流与讨论】(1)甲同学认为石蕊变色后又褪色的原因是___________________ 。
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①乙同学认为A是N2,遭到大家的一致反对,原因是__________________ 。
②丙同学认为A是NH3,也遭到大家的一致反对,原因是___________________________ 。
(3)经讨论,最终大家获得了A是NO的共识。
【延伸与拓展】丁同学对硝酸能与Cu反应很感兴趣,他取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象。请完成Cu与稀HNO3反应的化学方程式3Cu+8HNO3= 3Cu(NO3)2+______ +______ H2O。
对此很感兴趣,向老师提出探究硝酸的化学性质,老师高兴答应并带领同学们进行了
硝酸某些化学性质的实验探究。
【猜想与假设】(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变成
(2)将Zn片投入稀硝酸中,预计将产生氢气。
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B。
【提出问题】(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成氢气。
(2)硝酸具有强氧化性,能使有色物质褪色。
(3)氮元素某些气态化合物的某些性质如下表:
| NH3 | NO | NO2 | |
| 颜色 | 无色 | 无色 | 红棕色 |
| 溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
【交流与讨论】(1)甲同学认为石蕊变色后又褪色的原因是
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①乙同学认为A是N2,遭到大家的一致反对,原因是
②丙同学认为A是NH3,也遭到大家的一致反对,原因是
(3)经讨论,最终大家获得了A是NO的共识。
【延伸与拓展】丁同学对硝酸能与Cu反应很感兴趣,他取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象。请完成Cu与稀HNO3反应的化学方程式3Cu+8HNO3= 3Cu(NO3)2+
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】人通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳气体和水蒸气。但人体排出的二氧化碳气体究竟是空气中原有的,还是人体代谢的最终产物,为了证实这个问题,有人采用了下图所示的装置进行实验。

(1)人吸气时,应将活塞A______ (填“打开”或“关闭”),活塞B_____ (同上);
(2)人呼气时,应将活塞A关闭,活塞B打开,此时可观察到(Ⅱ)瓶内的现象是_____ ;将上述操作反复进行,能得出的结论是_____ 。

(1)人吸气时,应将活塞A
(2)人呼气时,应将活塞A关闭,活塞B打开,此时可观察到(Ⅱ)瓶内的现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】小红同学与其他同学一起对课本上的科学实验进行了自主探究。
探究Ⅰ、人体吸入空气和呼出气体的不同。
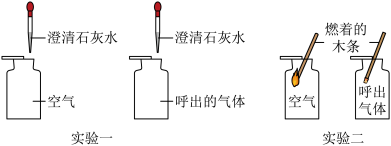
(1)实验1中要控制向两个集气瓶中加入的澄清石灰水______ 相同。
(2)实验1中______ 现象,说明呼出气体中含有较多的二氧化碳。
(3)实验2中观察到燃着的木条在呼出气体中较快熄灭,说明呼出气体和空气比较______ 。
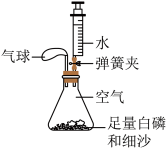
探究Ⅱ、兴趣小组同学们又设计了如图装置测定空气中氧气的含量。
【查阅资料】当温度达到 时,白磷可以燃烧。
时,白磷可以燃烧。
【实验准备】锥形瓶内空气体积为200mL,注射器中水的体积为50mL,该装置气密性良好。
【实验过程】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】
(4)将锥形瓶底部放入热水中,白磷剧烈燃烧,产生大量白烟,此反应的符号表达式为______ 。
(5)在整个实验过程中,锥形瓶内气压的变化是______ 。
(6)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,最后可观察到注射器中的水还剩下约______ mL。
【实验结论】空气中氧气约占空气体积分数的 。
。
【反思总结】
(7)反应结束后,集气瓶内剩余的气体主要是氮气,据以上实验现象可以推测氮气具有的化学性质是______ (写出一条即可)。
探究Ⅰ、人体吸入空气和呼出气体的不同。

(1)实验1中要控制向两个集气瓶中加入的澄清石灰水
(2)实验1中
(3)实验2中观察到燃着的木条在呼出气体中较快熄灭,说明呼出气体和空气比较
探究Ⅱ、兴趣小组同学们又设计了如图装置测定空气中氧气的含量。
【查阅资料】当温度达到
 时,白磷可以燃烧。
时,白磷可以燃烧。【实验准备】锥形瓶内空气体积为200mL,注射器中水的体积为50mL,该装置气密性良好。
【实验过程】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。

【现象分析】
(4)将锥形瓶底部放入热水中,白磷剧烈燃烧,产生大量白烟,此反应的符号表达式为
(5)在整个实验过程中,锥形瓶内气压的变化是
(6)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,最后可观察到注射器中的水还剩下约
【实验结论】空气中氧气约占空气体积分数的
 。
。【反思总结】
(7)反应结束后,集气瓶内剩余的气体主要是氮气,据以上实验现象可以推测氮气具有的化学性质是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】小致发现切开的苹果在空气中很快会变色,于是在老师的指导下,探究使苹果变色的气体成分。小致提出假设:氧气参与了苹果变色的过程。老师指导小致要进行对比实验,小致设计并完成如下实验。
(1)进行实验:探究使苹果变色的气体成分。实验步骤:
I.准备如图所示的实验装置,3个集气瓶容积均为250mL。A为用排水集气法收集的一瓶_______ 气,B为一瓶空气,C为一瓶空气。
Ⅱ.在C瓶中做红磷燃烧的实验,观察到的明显现象是产生大量_______ ,待装置_______ 后打开弹簧夹,至水不再进入集气瓶中,测量进入集气瓶中水的体积约为50mL,此时瓶内剩余气体主要成分为_______ 气。

III.将大小相同的苹果块依次迅速放入集气瓶A、B和做完实验Ⅱ后的C中记录苹果的变色时间。(忽略水及其他杂质对结果影响)
(2)实验结论:苹果变色与氧气_______ (填“有”或“无”)关。
(3)实验反思:
①实验Ⅱ中有一些因素会导致测量的结果不够准确,任写出其中一种因素:_______ 。
②生活中通常食品包装袋内填充氮气,其作用是_______ ,因为氮气比氧气_______ 。
(1)进行实验:探究使苹果变色的气体成分。实验步骤:
I.准备如图所示的实验装置,3个集气瓶容积均为250mL。A为用排水集气法收集的一瓶
Ⅱ.在C瓶中做红磷燃烧的实验,观察到的明显现象是产生大量

III.将大小相同的苹果块依次迅速放入集气瓶A、B和做完实验Ⅱ后的C中记录苹果的变色时间。(忽略水及其他杂质对结果影响)
| 集气瓶 | A | B | C |
| 放入苹果起始时间 | 下午2:00 | 下午2:00 | 下午2:00 |
| 实验现象 | 下午2:03苹果变色 | 下午2:09苹果变色 | 下午2:19苹果未变色 |
(3)实验反思:
①实验Ⅱ中有一些因素会导致测量的结果不够准确,任写出其中一种因素:
②生活中通常食品包装袋内填充氮气,其作用是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】燃烧与灭火紧密联系着我们的生活。请你依据下列实验探究,回答下列问题。
(1)在空气中点燃镁条,观察到镁条剧烈燃烧,发出耀眼白光,说明该反应___ (填“放出”或“吸收”)能量,生成白色固体MgO,说明镁发生了___ (填“氧化”或“还原”)反应。
(2)CO2可用于灭火,是否也可熄灭燃着的镁呢?某实验小组进行了如下探究:
【实验探究】取两块大小相同的干冰,在一块干冰中央挖一个小穴,放入一些镁屑,用红热的铁棒点燃镁屑(如图甲)。
迅速将另一块干冰盖上,镁在两块干冰间剧烈反应,发出耀眼的白光,像冰块中装入一个明亮的电灯泡一样(如图乙、丙)。
取走上面一块干冰,观察到有白色固体产生(如图丁),用铁片拨开图丁产物的表面(如图戊),还观察到的现象是_____ ,写出该反应的化学方程式_____ 。

【反思与交流】
①小组实验后讨论,对初中教材中燃烧的条件有了新的认识:_____ (合理即可)。
②通过本实验,金属镁着火时,可以采用的灭火方法是___ (填字母)。
A.用水浇灭 B.用CO2灭火器 C.用沙子灭火
(1)在空气中点燃镁条,观察到镁条剧烈燃烧,发出耀眼白光,说明该反应
(2)CO2可用于灭火,是否也可熄灭燃着的镁呢?某实验小组进行了如下探究:
【实验探究】取两块大小相同的干冰,在一块干冰中央挖一个小穴,放入一些镁屑,用红热的铁棒点燃镁屑(如图甲)。
迅速将另一块干冰盖上,镁在两块干冰间剧烈反应,发出耀眼的白光,像冰块中装入一个明亮的电灯泡一样(如图乙、丙)。
取走上面一块干冰,观察到有白色固体产生(如图丁),用铁片拨开图丁产物的表面(如图戊),还观察到的现象是

【反思与交流】
①小组实验后讨论,对初中教材中燃烧的条件有了新的认识:
②通过本实验,金属镁着火时,可以采用的灭火方法是
A.用水浇灭 B.用CO2灭火器 C.用沙子灭火
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小红发现切开的苹果会很快变色,于是在老师的指导下,探究氧气是否参与了苹果变色的过程。小红提出假设:氧气参与了苹果变色的过程。老师指导小红要进行对比 实验,小红设计并完成了如下2个实验。
(1)实验1:探究使苹果变色的气体成分。
实验步骤:
①准备如下图所示的实验装置,A为用排水集气法收集的1瓶_______ 气,B为1瓶空气,C瓶中为空气,3个集气瓶容积均为250 mL;

②在C瓶中做红磷燃烧的实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进入集气瓶中水的体积约为50 mL,剩余气体的主要成分为________ ;
③将大小相同的苹果块依次迅速放入集气瓶A、B和C中,记录苹果的变色时间。
结论:____________________________________________________________________ 。
(2)实验2:探究苹果变色消耗的气体体积。
小红为了探查集气瓶A、B中消耗气体的体积,她采取的实验步骤是:_____________ 。
实验后小红记录了进入集气瓶内水的体积,由此计算出A瓶中苹果消耗气体的体积,请你在表格中填写B瓶苹果消耗气体的体积。
(3)实验反思:实验过程中有一些因素会导致测量的结果不够准确,写出其中一种因素______________ 。
(1)实验1:探究使苹果变色的气体成分。
实验步骤:
①准备如下图所示的实验装置,A为用排水集气法收集的1瓶

②在C瓶中做红磷燃烧的实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进入集气瓶中水的体积约为50 mL,剩余气体的主要成分为
③将大小相同的苹果块依次迅速放入集气瓶A、B和C中,记录苹果的变色时间。
| A | B | C | |
| 放入苹果起始时间 | 下午2:00 | 下午2:00 | 下午2:00 |
| 实验现象 | 下午2:03 苹果变色 | 下午2:09 苹果变色 | 下午2:19 苹果未变色 |
(2)实验2:探究苹果变色消耗的气体体积。
小红为了探查集气瓶A、B中消耗气体的体积,她采取的实验步骤是:
实验后小红记录了进入集气瓶内水的体积,由此计算出A瓶中苹果消耗气体的体积,请你在表格中填写B瓶苹果消耗气体的体积。
| A | B | |
| 进入水的体积 | 200 mL | 42 mL |
| 苹果消耗气体的体积 | 50 mL |
(3)实验反思:实验过程中有一些因素会导致测量的结果不够准确,写出其中一种因素
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐1】实验课上,同学们利用澄清石灰水检验空气中的二氧化碳,实验中发现各组石灰水混浊程度存在较大差异,于是设计实验探究影响石灰水混浊程度的因素。
【进行实验】装置图如下所示。
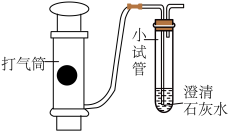
实验1:取饱和澄清石灰水进行实验。
实验2:利用向饱和石灰水中添加蒸馏水来调节石灰水浓度进行实验(溶液浓度变化引起的溶液密度变化忽略不计)。
【解释与结论】
(1)小试管中发生反应的化学方程式为____________ 。
(2)实验1的目的为____________ 。
(3)实验2中a、b、c三处数据,设计合理的是________ 。
A 0.5 0.5 0.5 B 0.5 1.0 1.5
C 1.0 1.5 2.0 D 1.0 2.0 3.0
(4)实验2的结论是________ 。
【反思与评价】
(5)通过对比实验1-1和2-1,可得出影响石灰水混浊程度的另一因素是________ ,理由是________ 。
【进行实验】装置图如下所示。

实验1:取饱和澄清石灰水进行实验。
| 实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
| 饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
| 缓慢通入2 L空气后的浑浊程度 | 不明显 | 明显 | 非常明显 | 明显 |
| 实验序号 | 2-1 | 2-2 | 2-3 | 2-4 |
| 饱和澄清石灰水体积/mL | 2.0 | 1.5 | 1.0 | 0.5 |
| 加入蒸馏水体积/mL | 0 | a | b | c |
| 缓慢通入3 L空气后的浑浊程度 | 非常明显 | 明显 | 不明显 | 无现象 |
(1)小试管中发生反应的化学方程式为
(2)实验1的目的为
(3)实验2中a、b、c三处数据,设计合理的是
A 0.5 0.5 0.5 B 0.5 1.0 1.5
C 1.0 1.5 2.0 D 1.0 2.0 3.0
(4)实验2的结论是
【反思与评价】
(5)通过对比实验1-1和2-1,可得出影响石灰水混浊程度的另一因素是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】蒸汽眼罩是我们日常生活中常见的缓解眼睛疲劳的产品,简单实用。某化学兴趣小组的同学对蒸汽眼罩开展了以下研究。
【查阅资料】
I.蒸汽眼罩由无纺布眼罩和发热体构成。发热体内含有铁粉、活性炭、氯化钠、蛭石(保温作用,可以减缓热量散失)、吸水树脂(良好保水性能,为眼罩提供水蒸气)等。
II.铁粉、四氧化三铁均能被磁铁吸引。
【任务一】验证蒸汽眼罩发热体内含有铁粉和氯化钠
(1)甲同学用磁铁吸引了部分发热体内固体粉末,放入试管中,滴加硫酸铜溶液,观察到有红色固体析出,证明发热体内含有铁粉。该反应的化学方程式为_____ 。
(2)乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是_____ 。静置后,取上层清液于试管中,加入硝酸银溶液,产生白色沉淀,证明发热体内含有氯化钠。
【任务二】探究蒸汽眼罩的发热原理
(3)根据“使用方法——打开蒸汽眼罩包装,接触空气即开始发热”,小组同学讨论后一致认为氮气对铁生锈没有影响,理由是______ 。
(4)同学们在老师指导下进行了以下实验:取20g发热体内的固体粉末放入密闭容器中,通过数字传感器分别测得氧气和二氧化碳含量变化,如图所示。据图回答:发热体内的物质和空气中的______ (填物质名称)发生反应。
(5)实验2 中应取用氯化钠质量是_____ g。
(6)实验4中温度迅速上升的原因是_____ 。
【拓展延伸】
(7)工厂里在蒸汽眼罩装袋时,应确保_____ 。
【查阅资料】
I.蒸汽眼罩由无纺布眼罩和发热体构成。发热体内含有铁粉、活性炭、氯化钠、蛭石(保温作用,可以减缓热量散失)、吸水树脂(良好保水性能,为眼罩提供水蒸气)等。
II.铁粉、四氧化三铁均能被磁铁吸引。
【任务一】验证蒸汽眼罩发热体内含有铁粉和氯化钠
(1)甲同学用磁铁吸引了部分发热体内固体粉末,放入试管中,滴加硫酸铜溶液,观察到有红色固体析出,证明发热体内含有铁粉。该反应的化学方程式为
(2)乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,玻璃棒的作用是
【任务二】探究蒸汽眼罩的发热原理
(3)根据“使用方法——打开蒸汽眼罩包装,接触空气即开始发热”,小组同学讨论后一致认为氮气对铁生锈没有影响,理由是
(4)同学们在老师指导下进行了以下实验:取20g发热体内的固体粉末放入密闭容器中,通过数字传感器分别测得氧气和二氧化碳含量变化,如图所示。据图回答:发热体内的物质和空气中的

| 方案 | 药品 | 1分钟前后氧气的含量变化 | 1分钟前后温度的变化 |
| 1 | 4g铁粉、2mL水 | 20.1%-20.1% | 16℃-16℃ |
| 2 | 4g铁粉、2mL水、 g氯化钠 | 20.1%-20.1% | 16℃-16℃ |
| 3 | 4g铁粉、2mL水、2g活性炭 | 20.1%-20.1% | 16℃-16℃ |
| 4 | 4g铁粉、2mL水、2g氯化钠、2g活性炭 | 20.1%-15% | 16℃-55℃-26℃ |
(5)实验2 中应取用氯化钠质量是
(6)实验4中温度迅速上升的原因是
【拓展延伸】
(7)工厂里在蒸汽眼罩装袋时,应确保
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐3】某研究小组为探究“影响镁与稀硫酸反应快慢的因素”,进行了如下实验探究:
【猜想与假设】假设一:与反应初始温度有关;猜想二:与稀硫酸的浓度有关
【实验探究】
用砂纸打磨镁条,进行下列实验。打磨的目的是_____________ 。
(1)小组的同学用相同质量和长度的镁条与相同体积的稀硫酸进行反应,探究过程如下:
(2)写出镁与稀硫酸反应的化学方程式___________________ 。
【实验结论】
(3)实验②和③比较,镁与稀硫酸反应快慢与_________ 有关。
(4)通过实验①和②比较,结论_____________________ 。
(5)上述实验最好选用收集方法_____ ,除了上述的测量方法以外,还可以通过测量________ ,也可以达到实验目的。
【反思与评价】
(6)实验①结束时测得溶液的温度为30℃,该反应属于____ (填“吸热”或“放热”)反应。
【猜想与假设】假设一:与反应初始温度有关;猜想二:与稀硫酸的浓度有关
【实验探究】
用砂纸打磨镁条,进行下列实验。打磨的目的是
(1)小组的同学用相同质量和长度的镁条与相同体积的稀硫酸进行反应,探究过程如下:
| 反应初温/℃ | 镁的形状 | 稀硫酸的浓度/% | 气体的体积/ml | |
| ① | 20 | 镁条 | 5 | 40 |
| ② | 20 | 镁条 | 10 | 55 |
| ③ | 30 | 镁条 | 10 | 62 |
(2)写出镁与稀硫酸反应的化学方程式
【实验结论】
(3)实验②和③比较,镁与稀硫酸反应快慢与
(4)通过实验①和②比较,结论
(5)上述实验最好选用收集方法
【反思与评价】
(6)实验①结束时测得溶液的温度为30℃,该反应属于
您最近一年使用:0次



