物质的性质决定物质的用途。氢氧化钙在工农业生产、国防建设等领域用途极广。请回答下列问题:
(1)某化工厂生产过程产生的污水中,主要污染物是盐酸,可用成本较低的熟石灰进行处理。写出该反应的化学方程式:_____ 。请分析该反应的微观实质:_____ 。请另外再写出一个符合上述反应实质的化学方程式_____ 。
(2)在农业上用石灰乳(主要成分是氢氧化钙)和硫酸铜晶体混合配制波尔多液,可防治多种病害。氢氧化钙在农业中还可以用于_____ 。(请写一种即可)
(3)在国防建设中石灰乳和苦卤水(海水晒盐析出粗盐晶体后剩余的液体)为原料,通过一系列化学变化制得“国防金属”镁。综合利用苦卤水制备金属镁的流程如下图所示,请根据下图回答下列问题:
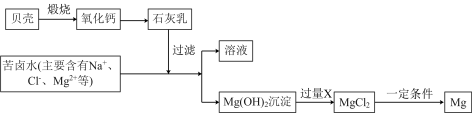
①要使苦卤水中的MgCl2完全转化为沉淀Mg(OH)2,分批加入过量的石灰乳。使海水中的MgCl2全部转化为Mg(OH)2。写出该反应的化学方程式_____ .
②要将沉淀出的氢氧化镁转化为氯化镁,可以加入过量的X溶液,写出X的化学式_____ .
③无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式:MgCl2 Mg+Cl2↑;反应基本类型是
Mg+Cl2↑;反应基本类型是_____ 。
(1)某化工厂生产过程产生的污水中,主要污染物是盐酸,可用成本较低的熟石灰进行处理。写出该反应的化学方程式:
(2)在农业上用石灰乳(主要成分是氢氧化钙)和硫酸铜晶体混合配制波尔多液,可防治多种病害。氢氧化钙在农业中还可以用于
(3)在国防建设中石灰乳和苦卤水(海水晒盐析出粗盐晶体后剩余的液体)为原料,通过一系列化学变化制得“国防金属”镁。综合利用苦卤水制备金属镁的流程如下图所示,请根据下图回答下列问题:

①要使苦卤水中的MgCl2完全转化为沉淀Mg(OH)2,分批加入过量的石灰乳。使海水中的MgCl2全部转化为Mg(OH)2。写出该反应的化学方程式
②要将沉淀出的氢氧化镁转化为氯化镁,可以加入过量的X溶液,写出X的化学式
③无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式:MgCl2
 Mg+Cl2↑;反应基本类型是
Mg+Cl2↑;反应基本类型是
更新时间:2019-11-05 22:22:41
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
【推荐1】A、B、C、D、E是初中化学常见的五种物质,它们分别是单质、酸、碱、盐、氧化物中的一种,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,其相互反应情况如图所示(短线“一”相连的物质间能反应,箭头“→”表示能转化)。

(1)构成A的微粒是___ (填微粒名称);C的水溶液中阳离子符号是___ 。
(2)D可由两种氧化物反应生成,请写出化学方程式:___ 。
(3)写出一个E与D反应可能的化学方程式:___ 。

(1)构成A的微粒是
(2)D可由两种氧化物反应生成,请写出化学方程式:
(3)写出一个E与D反应可能的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】已知A是黑色固体粉末,F为金属单质,X是气体,溶液Y和Z分别是一种碱溶液和盐溶液,各物质之间的转化关系如图所示,请回答下列问题

(1)写出D的化学式_____
(2)反应①的化学方程式_____
(3)反应②的化学方程式_____ ,基本反应类型为_____
(4)写出物质C的一种用途_____

(1)写出D的化学式
(2)反应①的化学方程式
(3)反应②的化学方程式
(4)写出物质C的一种用途
您最近一年使用:0次
【推荐3】某化学小组需要用到质量分数为10%的氢氧化钠溶液来做实验,但实验室的氢氧化钠刚好用完。同学们提出用熟石灰与碳酸钠反应制取氢氧化钠,再配成溶液来做实验。
下表是氢氧化钙和氢氧化钠的溶解度数据
请回答问题:
(1)制备氢氧化钠。写出制取氢氧化钠反应的化学方程式______ 。反应后过滤,蒸发结晶得到固体氢氧化钠。小明提出这样制得的氢氧化钠可能含有少量杂质,其理由是______ 。
(2)提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是______ (双选)。
A 滤渣中只有氢氧化钠
B 滤渣中主要是氢氧化钠,可能有少量氢氧化钙
C 滤液中一定有氢氧化钙,可能有氢氧化钠
D 滤液中一定有氢氧化钠和氢氧化钙
E 滤液中只有氢氧化钙
(3)配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为______ g,称取时必须将氢氧化钠固体放在______ 里进行称量。
(4)进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为______ (精确到0.1%)
下表是氢氧化钙和氢氧化钠的溶解度数据
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100gH2O) | 氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| 氢氧化钠 | 31 | 90 | 111 | 129 | 313 | 336 | |
(1)制备氢氧化钠。写出制取氢氧化钠反应的化学方程式
(2)提纯氢氧化钠。将上述制得的氢氧化钠(含少量氢氧化钙)在60℃时配成饱和溶液,降温、结晶、过滤,对滤渣和滤液成分的分析,正确的是
A 滤渣中只有氢氧化钠
B 滤渣中主要是氢氧化钠,可能有少量氢氧化钙
C 滤液中一定有氢氧化钙,可能有氢氧化钠
D 滤液中一定有氢氧化钠和氢氧化钙
E 滤液中只有氢氧化钙
(3)配制氢氧化钠溶液。配制50克10%氢氧化钠溶液,需要氢氧化钠固体的质量为
(4)进行实验。完全中和40g上述配得的氢氧化钠溶液,用去了稀硫酸的质量为20克,则稀硫酸的质量分数为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组同学模拟如下流程对含有大量H2SO4和CuSO4的废水进行处理,以回收金属铜,并使废水pH和重金属含量达到排放标准。

已知:步骤I无蓝色沉淀生成。
⑴Ca(OH)2的俗名为______ ;稀硫酸的工业用途有:______ (举一例即可)。
⑵步骤Ⅱ和步骤Ⅲ都需进行的操作是______ ,该操作常用的玻璃仪器除玻璃棒、烧杯外,还有______ ;玻璃棒作用______ 。
⑶步骤Ⅱ得到金属铜的反应的化学方程式为______ 。
⑷步骤Ⅰ中加入少量Ca(OH)2最终 目的是______ 。
⑸步骤Ⅲ需加入Na2S才能使废水达到排放标准。从微观角度看,溶液中实际发生的反应为:
Cu2+ +______ = CuS↓

已知:步骤I无蓝色沉淀生成。
⑴Ca(OH)2的俗名为
⑵步骤Ⅱ和步骤Ⅲ都需进行的操作是
⑶步骤Ⅱ得到金属铜的反应的化学方程式为
⑷步骤Ⅰ中加入少量Ca(OH)2
⑸步骤Ⅲ需加入Na2S才能使废水达到排放标准。从微观角度看,溶液中实际发生的反应为:
Cu2+ +
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A-E是初中化学常见的五种不同类别的物质,其中B由两种元素组成,C常用作食品干燥剂,并且C、D、E含有一种相同的金属元素,它们之间的转化关系如图所示(图中“一”表示两端的物质间能反应,“→”表示物质间存在转化关系,部分反应物、生成物和反应条件已略去)。请回答:

(1)物质C的化学式:___________ 。
(2)物质D俗称为___________ (写一个);
(3)图中涉及的基本反应类型有___________ 个。
(4)反应“B-E”的化学方程式是___________ 。

(1)物质C的化学式:
(2)物质D俗称为
(3)图中涉及的基本反应类型有
(4)反应“B-E”的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】2020年6月8日是第12个“世界海洋日”,海洋是巨大的资源宝库。某课题小组模拟工业海水提镁的流程,在实验室制取生产镁的原料——氯化镁,设计方案如下:

【信息】
(1)海水和苦卤中都含有NaCl、Na2SO4、MgCl2、CaCl2、KCl等。
(2)苦卤是海水晒盐后剩余的溶液。
(3)如下表是某品牌不同碱的价格。
请分析与计算。
(1)海水和苦卤都可以作为制取氯化镁的原料,甲同学提出选择苦卤更好,小组同学一致同意他的观点,理由是______ 。
(2)在工业生产中为了降低成本,试剂X最好选择表格中的______ 。
(3)该方案制取氯化镁时,要经历步骤I和步骤II两步转化,其主要目的是____ 。
(4)小组同学按上述方案进行了实验,并制得19.0g干燥纯净的氯化镁固体。若步骤Ⅱ中溶质质量分数为10%的稀盐酸与氢氧化镁恰好完全反应,且步骤III中氯化镁没有损失,求步骤II中消耗稀盐酸的质量___ 。(写出计算步骤)

【信息】
(1)海水和苦卤中都含有NaCl、Na2SO4、MgCl2、CaCl2、KCl等。
(2)苦卤是海水晒盐后剩余的溶液。
(3)如下表是某品牌不同碱的价格。
| 试剂 | NaOH | Ca(OH)2 | Ba(OH)2 | KOH |
| 价格(元/吨) | 2400 | 850 | 5300 | 5500 |
(1)海水和苦卤都可以作为制取氯化镁的原料,甲同学提出选择苦卤更好,小组同学一致同意他的观点,理由是
(2)在工业生产中为了降低成本,试剂X最好选择表格中的
(3)该方案制取氯化镁时,要经历步骤I和步骤II两步转化,其主要目的是
(4)小组同学按上述方案进行了实验,并制得19.0g干燥纯净的氯化镁固体。若步骤Ⅱ中溶质质量分数为10%的稀盐酸与氢氧化镁恰好完全反应,且步骤III中氯化镁没有损失,求步骤II中消耗稀盐酸的质量
您最近一年使用:0次



