用科学方法认识和改造物质。请你参与探究并填空:按照科学认识的过程,科学方法主要蕴含在两个阶段:一是感性认识阶段,主要是为了获得证据,如观察、预测、实验等;二是理性认识(理性思维)阶段,主要是为了形成科学认识,如科学抽象、科学假说,像比较与对比、归纳与演绎等。在前一阶段的学习中,我们通过实验、观察等手段验证了很多化学反应的发生,运用了“归纳、演绎;比较、对比”等科学的一般方法认识了几种典型的酸、碱、盐。请你运用以上方法认识硫酸铜。
(1)用归纳/演绎的方法认识硫酸铜的化学性质已知下列反应:
H2SO4+BaCl2═BaSO4↓+2HClNa2SO4+BaCl2=BaSO4↓+2NaCl
MgSO4+BaCl2═BaSO4↓+MgCl2K2SO4+BaCl2=BaSO4↓+2KCl
①从微观分析这组反应能够发生的原因是_____ 。
②由①中得到的规律可以推论“硫酸铜溶液也能跟氯化钡溶液反应”,运用的是_____ 的方法.
(2)用实验的方法认识硫酸铜的化学性质首先验证(1)②中“硫酸铜溶液也能跟氯化钡溶液反应”的推论,需进行实验是:
②用实验的方法认识硫酸铜的其他性质
(3)用重要的学科实验方法——“化学转化法”改造物质人类利用化学变化,创造出我们所需要的物质,极大地促进了人类社会的发展。我们的祖先很早就掌握了多种炼铜工艺。
◆火法炼铜:将孔雀石【主要成分是Cu2(OH)2CO3】和木炭一起加热可以得到红色的金属铜,请写出上述反应的化学方程式:①_____ 。②_____ 。(友情提示:孔雀石受热易分解,得到氧化铜、二氧化碳和水;在加热的条件下木炭和氧化铜反应得到铜和二氧化碳。)
◆湿法炼铜:将天然铜的化合物进行湿法炼铜,先用硫酸与氧化铜反应,再用铁置换出铜。“曾青得铁则化为铜”,“曾青”指可溶性铜盐,即铜盐遇到铁,就有铜生成。请写出上述反应的化学方程式:①_____ 。②_____ 。(友情提示:先用硫酸与氧化铜反应得到可溶性铜盐;铜盐遇到铁就有铜生成。)
(1)用归纳/演绎的方法认识硫酸铜的化学性质已知下列反应:
H2SO4+BaCl2═BaSO4↓+2HClNa2SO4+BaCl2=BaSO4↓+2NaCl
MgSO4+BaCl2═BaSO4↓+MgCl2K2SO4+BaCl2=BaSO4↓+2KCl
①从微观分析这组反应能够发生的原因是
②由①中得到的规律可以推论“硫酸铜溶液也能跟氯化钡溶液反应”,运用的是
(2)用实验的方法认识硫酸铜的化学性质首先验证(1)②中“硫酸铜溶液也能跟氯化钡溶液反应”的推论,需进行实验是:
| 实验操作 | 实验现象 | 结论 |
| 取少量硫酸铜溶液于A试管中,然后再滴加氯化钡溶液 | 结论:硫酸铜溶液能跟氯化钡溶液反应 |
②用实验的方法认识硫酸铜的其他性质
| 实验操作 | 实验现象 | 结论 |
| 取少量硫酸铜溶液于B试管中,然后再滴加2﹣3滴紫色石蕊试液,振荡 | 石蕊试液变红 | 结论:硫酸铜溶液显 |
| 取少量硫酸铜溶液于C试管中,然后再滴加氢氧化钠溶液 | 结论: |
(3)用重要的学科实验方法——“化学转化法”改造物质人类利用化学变化,创造出我们所需要的物质,极大地促进了人类社会的发展。我们的祖先很早就掌握了多种炼铜工艺。
◆火法炼铜:将孔雀石【主要成分是Cu2(OH)2CO3】和木炭一起加热可以得到红色的金属铜,请写出上述反应的化学方程式:①
◆湿法炼铜:将天然铜的化合物进行湿法炼铜,先用硫酸与氧化铜反应,再用铁置换出铜。“曾青得铁则化为铜”,“曾青”指可溶性铜盐,即铜盐遇到铁,就有铜生成。请写出上述反应的化学方程式:①
更新时间:2019-11-05 22:22:41
|
相似题推荐
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐1】在青竹湖学校的科技节活动中小青、小竹和小湖同学结伴来到化学实验室。
(1)小青同学通过降温结晶制备硝酸钾晶体,需要用到100克 40%的硝酸钾溶液,该浴液可由10%的硝酸钾溶液蒸发______ 克水获得。
(2)小竹和小湖同学发现实验室台面上有一包固体粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠中的四种物质。为确定其组成他们设计并进行如下实验。
小竹同学进行如下探究。请完成表中空白。
小湖同学进行如下探究。
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素。
(3)试综合小竹、小湖两位同学的实验进行分析,固体粉末的组成中除Na2CO3外,一定还含有的物质是______ ,可能含有的物质是______ (均填写化学式)。
(1)小青同学通过降温结晶制备硝酸钾晶体,需要用到100克 40%的硝酸钾溶液,该浴液可由10%的硝酸钾溶液蒸发
(2)小竹和小湖同学发现实验室台面上有一包固体粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠中的四种物质。为确定其组成他们设计并进行如下实验。
小竹同学进行如下探究。请完成表中空白。
| 实验操作 | 实验现象 | 实验结论及分析 |
| I、取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有 |
| II、向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中含有 |
| III、向II中所得溶液滴加过量稀盐酸 | 原固体粉末中一定含有Na2CO3 |
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素。
(3)试综合小竹、小湖两位同学的实验进行分析,固体粉末的组成中除Na2CO3外,一定还含有的物质是
您最近一年使用:0次
【推荐2】根据所学,回答问题。
(1)实验室有两瓶未贴标签的试剂,一瓶是氢氧化钠溶液,一瓶是稀硫酸。某化学兴趣小组利用这两瓶试剂进行了如下探究:
①区分两瓶试剂。下列药品中能成功达到实验目的的是______ 。
A.氯化钠溶液B.酚酞试液C.铁粉D.氧化铜
②经过区分后,兴趣小组向氢氧化钠溶液中加入了过量的稀盐酸,发现有少量气泡冒出,则该气泡的主要成分为________ 。兴趣小组据此得出结论,该氢氧化钠溶液已经变质。请写出变质的原因:_______ (用化学方程式表示)。
(2)有某固体混合物,已知该混合物中可能含有FeCl3、Na2SO4、NH4NO3、CuSO4四种物质中的两种或多种。某化学兴趣小组按如图所示进行实验,出现的现象如图所述(设过程中所有发生的反应都恰好完全反应)。

试根据实验过程和发生的现象填写以下空白:
①气体A的化学式为______ ,它能使紫色石蕊试液变_____ 色。
②生成蓝色沉淀C的化学方程式为______ 。
③固体混合物里,上述四种物质中,肯定不存在的物质是______ ,理由是______ 。
④实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号)_____ 。
⑤实验过程②中发生反应的化学方程式为_____ 。
(1)实验室有两瓶未贴标签的试剂,一瓶是氢氧化钠溶液,一瓶是稀硫酸。某化学兴趣小组利用这两瓶试剂进行了如下探究:
①区分两瓶试剂。下列药品中能成功达到实验目的的是
A.氯化钠溶液B.酚酞试液C.铁粉D.氧化铜
②经过区分后,兴趣小组向氢氧化钠溶液中加入了过量的稀盐酸,发现有少量气泡冒出,则该气泡的主要成分为
(2)有某固体混合物,已知该混合物中可能含有FeCl3、Na2SO4、NH4NO3、CuSO4四种物质中的两种或多种。某化学兴趣小组按如图所示进行实验,出现的现象如图所述(设过程中所有发生的反应都恰好完全反应)。

试根据实验过程和发生的现象填写以下空白:
①气体A的化学式为
②生成蓝色沉淀C的化学方程式为
③固体混合物里,上述四种物质中,肯定不存在的物质是
④实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号)
⑤实验过程②中发生反应的化学方程式为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
真题
解题方法
【推荐3】含有镁的合金广泛应用于航空航天领域,回答下列问题:
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到______ 的现象可推断二者发生了化学反应;
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是______ ;
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中, 滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式______ ;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为______ g。
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中, 滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】在研究酸和碱的化学性质时,某同学发现稀H2SO4与NaOH溶液混合后无明显现象产生,于是设计并完成了如下实验方案。
方案一:测定稀H2SO4与NaOH溶液混合前后的pH.
(1)用pH试纸测定NaOH溶液的pH,测得pH___________ 7 (选填“大于”、“等于”或“小于”);
(2)将定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH, pH=7。
方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色。
结论:稀H2SO4与NaOH溶液发生了化学反应;
在上述实验中需要用到溶质质量分数为10%的稀硫酸,现用20g溶质质量分数为98%的浓硫酸进行稀释,则需要增加水的质量为________ g, 若实验过程中量水时仰视读数,则会造成所得溶液溶质质量分数_____ (选填“偏大”、“不变”或“偏小”)
(3)甲酸(HCOOH)是一种具有挥发性的酸, 甲酸在热的浓硫酸中会分解生成两种氧化物;CO和H2O。如图是制取CO,用CO还原氧化铁并检验气体产物,同时收集尾气中的CO的实验装置。

①写出E装置玻璃管内发生反应的化学方程式______ 。
②若没有B装置,则不能达到检验气体产物的目的,原因是_____ 。
③E装置可起到收集CO的作用,实验结束时,E中有部分溶液进入到F烧杯中,请设计实验证明该溶液溶质的成分中含有NaOH,写出实验步骤、现象和结论__ 。
(4)某特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。请计算:

①20g赤铁矿石样品中氧化铁的质量_____ 。
②计算该样品中铁元素的质量分数,由此判断该赤铁矿石是否属于富铁矿石_____ 。
③实验中所用稀盐酸溶质的质量分数_____ 。
方案一:测定稀H2SO4与NaOH溶液混合前后的pH.
(1)用pH试纸测定NaOH溶液的pH,测得pH
(2)将定量的稀H2SO4加入该NaOH溶液中,混合均匀后测定其pH, pH=7。
方案二:向盛有NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色。
结论:稀H2SO4与NaOH溶液发生了化学反应;
在上述实验中需要用到溶质质量分数为10%的稀硫酸,现用20g溶质质量分数为98%的浓硫酸进行稀释,则需要增加水的质量为
(3)甲酸(HCOOH)是一种具有挥发性的酸, 甲酸在热的浓硫酸中会分解生成两种氧化物;CO和H2O。如图是制取CO,用CO还原氧化铁并检验气体产物,同时收集尾气中的CO的实验装置。

①写出E装置玻璃管内发生反应的化学方程式
②若没有B装置,则不能达到检验气体产物的目的,原因是
③E装置可起到收集CO的作用,实验结束时,E中有部分溶液进入到F烧杯中,请设计实验证明该溶液溶质的成分中含有NaOH,写出实验步骤、现象和结论
(4)某特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe2O3)中的含铁量,进行实验:取20g赤铁矿石样品,逐渐加入稀盐酸,充分反应。实验相关数据如图所示(假设杂质不溶于水,也不与酸反应)。请计算:

①20g赤铁矿石样品中氧化铁的质量
②计算该样品中铁元素的质量分数,由此判断该赤铁矿石是否属于富铁矿石
③实验中所用稀盐酸溶质的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐2】“鱼浮灵”主要成分是过碳酸钙和氢氧化钠(xNa2CO3•yH2O2)的混合物,俗称固体双氧水。碱石灰的成分是固体氧化钙和氢氧化钠的混合物,兴趣小组对其进行以下探究:
【“鱼浮灵”性质探究】
(1)收少量“鱼浮灵”于试管中加水,有持续组小气泡缓慢放出: 向试管中加少量MnO2。粉末,产生大量气泡。将带火星木条伸入试管内,木条______ 说明有O2生成。
(2)取实验(1)中上层清液,测得溶液pH>7;向溶波中滴加足量稀硫酸,产生大量气泡,将产生的气体通入澄清石灰水中,出现浑浊现象,说明该气体为______ 写出实验中两个反应的化学方程式______ 、______ 。
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
【工业制备】

[查阅资料]异丙醇是种有机溶剂,过碳酸钠在异丙醇中溶解度较小。
(3)稳定剂的作用是______
(4)操作II中洗涤晶体的试剂最好选用______(填字母)。
[“鱼浮灵”组成探究]

(5)实验前先缓慢过N段时间, 加热钢网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应:继续缓慢通N2,其目的是______
(6)装置B的作用是______ (填序号)
①除去气体中的水蒸气②便于观察和控制气流速度装置
C中的现象是______ ,装置E的作用是______
(7)实验测得C装置中铜网增重1.2g, D装置增重2.2g。x:y=______
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值______ (填“偏大”或“偏小”)。
【“鱼浮灵”性质探究】
(1)收少量“鱼浮灵”于试管中加水,有持续组小气泡缓慢放出: 向试管中加少量MnO2。粉末,产生大量气泡。将带火星木条伸入试管内,木条
(2)取实验(1)中上层清液,测得溶液pH>7;向溶波中滴加足量稀硫酸,产生大量气泡,将产生的气体通入澄清石灰水中,出现浑浊现象,说明该气体为
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
【工业制备】

[查阅资料]异丙醇是种有机溶剂,过碳酸钠在异丙醇中溶解度较小。
(3)稳定剂的作用是
(4)操作II中洗涤晶体的试剂最好选用______(填字母)。
| A.饱和NaCl溶液 | B.水 | C.异丙醇 | D.稀盐酸 |
[“鱼浮灵”组成探究]

(5)实验前先缓慢过N段时间, 加热钢网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应:继续缓慢通N2,其目的是
(6)装置B的作用是
①除去气体中的水蒸气②便于观察和控制气流速度装置
C中的现象是
(7)实验测得C装置中铜网增重1.2g, D装置增重2.2g。x:y=
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】某兴趣小组对某氯化钠样品(可能含有硝酸钾)进行实验探究。
(1)为检验氯化钠样品中是否含有硝酸钾,甲同学取少量样品进行焰色反应,透过蓝色的钴玻璃片观察,火焰呈___________ 色,证明样品中含有硝酸钾。
(2)为测定样品中氯化钠的含量,乙同学称取一定质量的样品溶于足量的水,再进行如下实验。___________ 。
II.为确定一定量样品中氯化钠的含量,还需进行的实验操作为___________ 。
(3)下表是硝酸钾和氯化钠的部分溶解度数据。
I.40℃时,氯化钠的溶解度为___________ 。
II.80℃时,200g硝酸钾加到100g水中,充分溶解并恢复至原温度,所得溶液中溶质的质量分数是___________ (用相应的数据列式表示,不用计算)。
III.某样品中含38.9g氯化钠、9.8g硝酸钾。20℃时,在该样品中加入110g水,充分溶解后,蒸发浓缩;当蒸发至剩余水量为10g时,至60℃时过滤,用数据分析此过程中析出晶体的组成情况___________ 。
(1)为检验氯化钠样品中是否含有硝酸钾,甲同学取少量样品进行焰色反应,透过蓝色的钴玻璃片观察,火焰呈
(2)为测定样品中氯化钠的含量,乙同学称取一定质量的样品溶于足量的水,再进行如下实验。
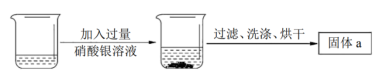
II.为确定一定量样品中氯化钠的含量,还需进行的实验操作为
(3)下表是硝酸钾和氯化钠的部分溶解度数据。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | |
| 溶解度(g/100g水) | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
II.80℃时,200g硝酸钾加到100g水中,充分溶解并恢复至原温度,所得溶液中溶质的质量分数是
III.某样品中含38.9g氯化钠、9.8g硝酸钾。20℃时,在该样品中加入110g水,充分溶解后,蒸发浓缩;当蒸发至剩余水量为10g时,至60℃时过滤,用数据分析此过程中析出晶体的组成情况
您最近一年使用:0次



