熟石灰在部分温度下的溶解度如下表所示。
①20℃时,0.56 g氧化钙放入到盛有100 g水的烧杯中。恢复到20℃时,所得溶液中水的质量_____ (填“增大”、“减小”或“不变”),溶液中溶质的质量分数是 _____ (写计算式)。
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液。下列说法正确的是____ 。
A 溶液的质量可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 可以升温使之变成不饱和溶液
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
①20℃时,0.56 g氧化钙放入到盛有100 g水的烧杯中。恢复到20℃时,所得溶液中水的质量
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液。下列说法正确的是
A 溶液的质量可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 可以升温使之变成不饱和溶液
更新时间:2019-11-15 21:11:58
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
【推荐1】向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤,如下图所示.

资料:A的溶解度如下表所示.
(1)溶液①~⑤中属于饱和溶液的是__________ (填序号,以下同).
(2)溶质质量分数相等的溶液是__________ .
(3)溶质质量分数最小的溶液是__________ .
(4)有固体存在的溶液是__________ .

资料:A的溶解度如下表所示.
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
(2)溶质质量分数相等的溶液是
(3)溶质质量分数最小的溶液是
(4)有固体存在的溶液是
您最近一年使用:0次
【推荐2】20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象。

(1)20℃时,______ (填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)如图中表示甲物质的溶解度曲线的是______ (填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是______ 。

(3)从a、b混合物中得到较纯净的a所采用的方法是______ 。

(1)20℃时,
(2)如图中表示甲物质的溶解度曲线的是

(3)从a、b混合物中得到较纯净的a所采用的方法是
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
真题
【推荐3】工业上常利用石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3的流程如下:
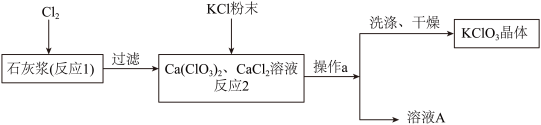
已知:①反应1为:6Cl2 + 6Ca(OH)2=Ca(ClO3)2 + 5CaCl2 + 6H2O。②有关物质在常温下的溶解度如下:
回答下列问题:
(1)在实验中两次涉及过滤操作,完成此操作需要的玻璃仪器有烧杯、玻璃棒、________ ,该操作中玻璃棒的作用是__________ 。
(2)Ca(ClO3)2的名称是___________ 。对于反应1,参加反应的Cl2中有一部分Cl的化合价升高,另一部分降低,则化合价升高的Cl与化合价降低的Cl 的个数比为_________ 。
(3)反应2为KCl与Ca(ClO3)2发生的复分解反应,该反应能发生的主要原因是_____ 。溶液A中含有的溶质为CaCl2和_________ (填化学式)。
(4)上述流程中析出的KClO3晶体表面通常吸附有Ca2+、Cl-等杂质离子,过滤时洗涤KClO3晶体,应选用下列中的___________ 饱和溶液(填编号)。
A KCl B CaCl2C KClO3D Na2CO3

已知:①反应1为:6Cl2 + 6Ca(OH)2=Ca(ClO3)2 + 5CaCl2 + 6H2O。②有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.0 |
(1)在实验中两次涉及过滤操作,完成此操作需要的玻璃仪器有烧杯、玻璃棒、
(2)Ca(ClO3)2的名称是
(3)反应2为KCl与Ca(ClO3)2发生的复分解反应,该反应能发生的主要原因是
(4)上述流程中析出的KClO3晶体表面通常吸附有Ca2+、Cl-等杂质离子,过滤时洗涤KClO3晶体,应选用下列中的
A KCl B CaCl2C KClO3D Na2CO3
您最近一年使用:0次
【推荐1】如图是甲、乙两种固体物质的溶解度曲线,请回答:

(1)t1℃时,甲乙的溶解度大小关系为:甲______ 乙(填“﹥”、“=”或“﹤”);
(2)要使接近饱和的甲物质的溶液变为饱和溶液,可采用的方法是______ (填“升高”或“降低”)温度,还可以采用的方法为______ 。
(3)t2℃时,向50克水中加入乙物质配成该温度下的饱和溶液,需加乙______ g。此时溶液中乙的质量分数为______ (保留1位小数)。

(1)t1℃时,甲乙的溶解度大小关系为:甲
(2)要使接近饱和的甲物质的溶液变为饱和溶液,可采用的方法是
(3)t2℃时,向50克水中加入乙物质配成该温度下的饱和溶液,需加乙
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
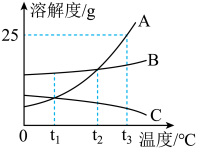
(1)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:加入C物质或恒温蒸发溶剂或__ 。
(2)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数由大到小的顺序是_____ 。

(1)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:加入C物质或恒温蒸发溶剂或
(2)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数由大到小的顺序是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】甲、乙、丙三种固体物质的溶解度曲线如图所示,请根据图示回答下列问题。
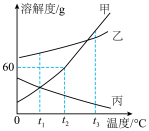
(1)丙物质的溶解度随温度的升高而_____ (填“增大”或“减小”)。
(2)若要从乙物质的饱和溶液中得到乙固体,可用_____ 结晶方法。
(3)t1℃时,将甲物质的饱和溶液升温到t3℃所得溶液中溶质的质量分数_____ (填“变大”、“变小”或“不变”)。
(4)t2℃将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是:_____ 。
(5)t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是_____ 。

(1)丙物质的溶解度随温度的升高而
(2)若要从乙物质的饱和溶液中得到乙固体,可用
(3)t1℃时,将甲物质的饱和溶液升温到t3℃所得溶液中溶质的质量分数
(4)t2℃将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是:
(5)t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐1】依据下列20℃时的实验和数据回答问题。
已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。
(1)①~⑤所得溶液属于饱和溶液的是_____ 。
(2)下列关于①~⑤所得溶液的说法不正确的是_____ 。
A 溶质质量:①<②B 溶液质量:②<④
C 溶质质量分数:①=③D ⑤中溶质与溶剂的质量比为9:10
已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。
 | 序号 | ① | ② | ③ | ④ | ⑤ |
| 固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
| 固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
| 水的质量/g | 100 | 100 | 100 | 100 | 100 |
(2)下列关于①~⑤所得溶液的说法不正确的是
A 溶质质量:①<②B 溶液质量:②<④
C 溶质质量分数:①=③D ⑤中溶质与溶剂的质量比为9:10
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
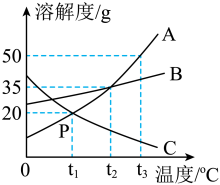
【推荐2】甲和乙两种固体物质的溶解度曲线如图所示。A点的含义是_________ ;将t2℃时等质量的甲和乙两种物质的饱和溶液分别降温到20℃,析出固体质量甲 ________ (选填“>”“=”或“<”)乙;t1℃时,将40g甲物质加入50g的水中,所得溶液的溶质质量分数为 ___________


您最近一年使用:0次