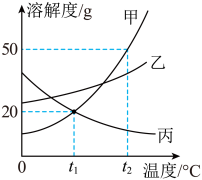
20℃时,取相同质量的a、b、c三种物质的饱和溶液分别置于三个烧杯中,再分别向其中加入相同质量的相应固体溶质,将温度升高到40℃,固体的溶解情况如图1所示。图2为a、b、c三种物质的溶解度曲线。请仔细阅读图1和图2回答下列问题:

(1)30℃时,三种物质的溶解度大小关系为__________________ 。
(2)烧杯丙里的溶液是________________ 物质的溶液;(填a、b、c)
(3)40℃时,烧杯_____________ 里的溶液中溶质量最多。
(4)各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质质量分数的比较一定正确的是_________
A乙(状态1)>甲(状态3) B乙(状态3)>丙(状态3)
C甲(状态1)=乙(状态2) D甲(状态2)>甲(状态1)

(1)30℃时,三种物质的溶解度大小关系为
(2)烧杯丙里的溶液是
(3)40℃时,烧杯
(4)各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质质量分数的比较一定正确的是
A乙(状态1)>甲(状态3) B乙(状态3)>丙(状态3)
C甲(状态1)=乙(状态2) D甲(状态2)>甲(状态1)
更新时间:2019-10-07 20:00:37
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】硝酸钾溶解度曲线如图所示

①10℃时,硝酸钾的溶解度是____________ g/100g水。
②某温度时,6.4g硝酸钾放入10g水中恰好形成饱和溶液,则该温度硝酸钾的溶解度是________ g/100g水。
③如下图所示进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液A1、A2、A3,且溶液质量依次减小。

I.请定量说明“方法一”是_____________ ;
II.请在溶解度曲线图中标出表示溶液A2的点,并标注“A2”_____________ ;
Ⅲ.溶液A1、A2、A3中溶质质量分数的大小关系是_______________ 。

①10℃时,硝酸钾的溶解度是
②某温度时,6.4g硝酸钾放入10g水中恰好形成饱和溶液,则该温度硝酸钾的溶解度是
③如下图所示进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液A1、A2、A3,且溶液质量依次减小。

I.请定量说明“方法一”是
II.请在溶解度曲线图中标出表示溶液A2的点,并标注“A2”
Ⅲ.溶液A1、A2、A3中溶质质量分数的大小关系是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)下表是A物质的溶解度。70°C时, 向盛有100g 水的烧杯中加入30g固体A,充分溶解形成的是_____ (填 “饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20°C,此时溶液中溶质与溶剂的质量比为_____ (填最简整数比);
(2)根据下图回答问题:

①由图一分析,若分别将甲、乙的饱和溶液从t2°C降温到t1°C,下列关于所得溶液的叙述正确的_____ ;(填序号)。
A 甲、乙都是饱和溶液
B 所含溶剂质量:甲<乙
C 溶液质量:甲<乙
D 溶质质量分数:甲>乙
②如图一所示, 现有一杯t2°C时A点的甲溶液,100 水中溶有63g甲,若将其变成饱和溶液,可以增加溶质甲_____ g,或者恒温蒸发掉水_____ g,或者将温度_____ 。
③气体的溶解度也有一定规律。 如图二所示,在t1°C和t2°C两个不同温度下氧气的溶解度随压强而变化的情况,若t1°C对应的温度为40°C,则t2°C对应的温度_____ (填字母序号 )。
A 小于40°C
B 大于40°C
C 等于40°C
D 无法确定
(1)下表是A物质的溶解度。70°C时, 向盛有100g 水的烧杯中加入30g固体A,充分溶解形成的是
| 温度/°C | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(2)根据下图回答问题:

①由图一分析,若分别将甲、乙的饱和溶液从t2°C降温到t1°C,下列关于所得溶液的叙述正确的
A 甲、乙都是饱和溶液
B 所含溶剂质量:甲<乙
C 溶液质量:甲<乙
D 溶质质量分数:甲>乙
②如图一所示, 现有一杯t2°C时A点的甲溶液,100 水中溶有63g甲,若将其变成饱和溶液,可以增加溶质甲
③气体的溶解度也有一定规律。 如图二所示,在t1°C和t2°C两个不同温度下氧气的溶解度随压强而变化的情况,若t1°C对应的温度为40°C,则t2°C对应的温度
A 小于40°C
B 大于40°C
C 等于40°C
D 无法确定
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐1】如图是甲、乙、丙三种固体物质的溶解度曲线。请回答下列问题。

(1)随温度升高,溶解度减小的物质是________ 。
(2)P点表示的含义是_________ 。
(3)欲使乙溶液的状态从P点转化为C点,可采取的措施是_________ 。
(4) t2℃时,把58g乙物质加入到200g水中充分搅拌、静置,形成的是_____ 溶液(填“饱和”或“不饱和”)。
(5)将150g甲的饱和溶液从t3℃降到 t2℃后,向其中加入50g水,此时所得溶液的溶质质量分数是______ (计算结果精确到0.1%)。

(1)随温度升高,溶解度减小的物质是
(2)P点表示的含义是
(3)欲使乙溶液的状态从P点转化为C点,可采取的措施是
(4) t2℃时,把58g乙物质加入到200g水中充分搅拌、静置,形成的是
(5)将150g甲的饱和溶液从t3℃降到 t2℃后,向其中加入50g水,此时所得溶液的溶质质量分数是
您最近一年使用:0次
【推荐2】如图1为甲、乙两种固体物质的溶解度曲线。

(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是_________ (填字母)。向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量为___________ g。
(2)将t2℃时等质量的甲、乙两种物质的饱和溶液降温至t1℃,下列说法正确的是__________。

(1)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是
(2)将t2℃时等质量的甲、乙两种物质的饱和溶液降温至t1℃,下列说法正确的是__________。
| A.降温后,甲溶液的质量大于乙溶液的质量 |
| B.降温前,甲溶液中溶剂的质量比乙溶液中溶剂的质量小 |
| C.降温后,甲溶液的质量分数大于乙溶液的质量分数 |
| D.降温前后乙溶液的质量分数保持不变 |
您最近一年使用:0次
【推荐3】水和溶液在生产、生活和科研中具有广泛的用途。
(1)下列净水的方法中,可以降低水的硬度的是 (填字母)。
(2)自来水厂利用活性炭去除天然水中色素和异味,这是利用了活性炭的__________ 性。
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出,原因是_______ 。
(4)下图是四种固体物质的溶解度曲线;下表是这些固体物质在不同温度时的溶解度。

①图中b曲线表示________ (填物质名称)的溶解度曲线。
②分别将10℃时KCl和KNO3的饱和溶液升高温度到40℃(不考虑水的蒸发),所得溶液中溶质的质量分数相比,前者______ 后者(填“大于” “小于”或“等于”)。
③50℃时,在50 g水中加入20 g上表中的某种固体物质,充分搅拌后不能全部溶解,该物质是________ 。
④分别将80℃时269 g KNO3饱和溶液和138.4 g NaCl的饱和溶液,降低温度到20℃,理论上析出KNO3固体的质量比析出NaCl固体的质量多______ g。
(1)下列净水的方法中,可以降低水的硬度的是 (填字母)。
| A.过滤 | B.煮沸 | C.蒸馏 |
(2)自来水厂利用活性炭去除天然水中色素和异味,这是利用了活性炭的
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出,原因是
(4)下图是四种固体物质的溶解度曲线;下表是这些固体物质在不同温度时的溶解度。
| 温度/℃ | 20 | 50 | 80 | |
| 溶 解 度/g | NaCl | 36.0 | 37.0 | 38.4 |
| KCl | 34.0 | 42.6 | 51.1 | |
| NH4Cl | 37.2 | 50.4 | 65.6 | |
| KNO3 | 31.6 | 85.5 | 169 | |

①图中b曲线表示
②分别将10℃时KCl和KNO3的饱和溶液升高温度到40℃(不考虑水的蒸发),所得溶液中溶质的质量分数相比,前者
③50℃时,在50 g水中加入20 g上表中的某种固体物质,充分搅拌后不能全部溶解,该物质是
④分别将80℃时269 g KNO3饱和溶液和138.4 g NaCl的饱和溶液,降低温度到20℃,理论上析出KNO3固体的质量比析出NaCl固体的质量多
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】“我们比历史上任何时期都更需要建设世界科技强国!”习近平同志在两院院士大会上再次强调了建设世界科技强国的奋斗目标,为我们大力发展科学技术指明了方向。“科技梦”助推“中国梦”,都离不开化学。

(1)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则氯化铷的化学式为______ 。
(2)2021年3月,我国两会通过的“十四五”规划纲要,提出了力争2060年前实现“碳中和”的目标。目前科学家已将从空气中捕获的二氧化碳与氢气混合后,在高温条件下用金属钌催化将其转化为新能源甲醇(CH3OH),同时有水生成。则该反应的化学方程式为______ 。
(3)抗击新冠肺炎(2019-nCoV)疫情期间,我国政府颁布了公共场所必须戴口罩的通知,生产N95口罩的主要原料是聚丙烯,它属于______ (填“金属材料“或“合成材料”)。
(4)某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等阳离子,某化学兴趣小组的同学取该工厂废水样品进行下列实验。

①若a=b,则滤液中一定含有的阳离子是______ (填离子符号)。
②若向滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有______ (填化学式)。
(5)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
若不考虑水蒸发对实验的影响,请回答下列问题。
①65℃时,该溶液是否为饱和溶液?______ (填“是”、“否”或“无法判断”)。
②将40℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的有______ 。
a.升温;b.降温;c.加溶质M;d.加另一种固体N;e.恒温蒸发水;f.与40℃时M的饱和溶液混合。

(1)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则氯化铷的化学式为
(2)2021年3月,我国两会通过的“十四五”规划纲要,提出了力争2060年前实现“碳中和”的目标。目前科学家已将从空气中捕获的二氧化碳与氢气混合后,在高温条件下用金属钌催化将其转化为新能源甲醇(CH3OH),同时有水生成。则该反应的化学方程式为
(3)抗击新冠肺炎(2019-nCoV)疫情期间,我国政府颁布了公共场所必须戴口罩的通知,生产N95口罩的主要原料是聚丙烯,它属于
(4)某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等阳离子,某化学兴趣小组的同学取该工厂废水样品进行下列实验。

①若a=b,则滤液中一定含有的阳离子是
②若向滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有
(5)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
①65℃时,该溶液是否为饱和溶液?
②将40℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的有
a.升温;b.降温;c.加溶质M;d.加另一种固体N;e.恒温蒸发水;f.与40℃时M的饱和溶液混合。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
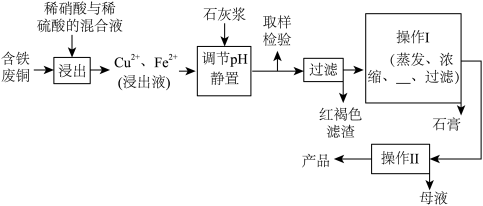
胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
请回答下列问题:
(1)红褐色滤渣的主要成分是____________ ;
(2)石灰浆调pH大约要调节到__________
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式________________________________ ;
(4)操作I最后温度应该控制在___________ ℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、__________ 、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 _________________ 。

胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是
(2)石灰浆调pH大约要调节到
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式
(4)操作I最后温度应该控制在
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】如图是A、B、C三种固体物质在水中的溶解度曲线,据图回答:

①t2℃时,A、B、C三种物质溶解度的大小关系是_____ 。
②有t1℃时A的饱和溶液75 g,其中A的质量为______ g。
③把C物质的不饱和溶液变为饱和溶液,下列有关说法正确
的是____ 。
Ⅰ.溶剂的质量一定变小 Ⅱ.溶质的质量可能不变
Ⅲ.溶质的质量分数一定变大 Ⅳ.溶质的质量一定变大
④将t3℃时A、B、C三种物质饱和溶液的温度降到t1℃后,三种溶液中溶质的质量分数由小到大的顺序是________ 。

①t2℃时,A、B、C三种物质溶解度的大小关系是
②有t1℃时A的饱和溶液75 g,其中A的质量为
③把C物质的不饱和溶液变为饱和溶液,下列有关说法正确
的是
Ⅰ.溶剂的质量一定变小 Ⅱ.溶质的质量可能不变
Ⅲ.溶质的质量分数一定变大 Ⅳ.溶质的质量一定变大
④将t3℃时A、B、C三种物质饱和溶液的温度降到t1℃后,三种溶液中溶质的质量分数由小到大的顺序是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】分别在 、
、 不同温度下,向40 g
不同温度下,向40 g  固体中不断加水,加入水的质量与溶质的质量关系如图所示,请回答下列问题。
固体中不断加水,加入水的质量与溶质的质量关系如图所示,请回答下列问题。 时,
时, 的溶解度为
的溶解度为___________ 。
(2) 和
和 的大小关系为
的大小关系为
___________  (填“>、<或=”)。
(填“>、<或=”)。
(3)用字母表示图中A、B、C、D四点对应的溶质质量分数的大小关系为___________ 。
(4)若将 时D点对应的溶液变为饱和溶液,下列方案可行的是___________(填字母)。
时D点对应的溶液变为饱和溶液,下列方案可行的是___________(填字母)。
 、
、 不同温度下,向40 g
不同温度下,向40 g  固体中不断加水,加入水的质量与溶质的质量关系如图所示,请回答下列问题。
固体中不断加水,加入水的质量与溶质的质量关系如图所示,请回答下列问题。
 时,
时, 的溶解度为
的溶解度为(2)
 和
和 的大小关系为
的大小关系为
 (填“>、<或=”)。
(填“>、<或=”)。(3)用字母表示图中A、B、C、D四点对应的溶质质量分数的大小关系为
(4)若将
 时D点对应的溶液变为饱和溶液,下列方案可行的是___________(填字母)。
时D点对应的溶液变为饱和溶液,下列方案可行的是___________(填字母)。A.温度变为 | B.加入20 g | C.恒温蒸发50 g水 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图1是NaCl、KNO3的溶解度曲线。______ g/100g水。
(2)NaCl中混有少量KNO3,提纯NaCl可采用的方法是______ 。
(3)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈______ 色。
(4)10℃时,KNO3饱和溶液的溶质质量分数为______ (列式即可)。
(5)60℃时,在甲、乙两烧杯中分别取Xg固体进行如图2所示实验。______ (选填“NaCl”或“KNO3”)。
②乙烧杯中状态1时为______ (选填“饱和”或“不饱和”)溶液。若向状态2时的乙烧杯中继续加入一定量该种固体,充分搅拌形成状态3,请在图3中绘出符合状态3的点______ 。

(2)NaCl中混有少量KNO3,提纯NaCl可采用的方法是
(3)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈
(4)10℃时,KNO3饱和溶液的溶质质量分数为
(5)60℃时,在甲、乙两烧杯中分别取Xg固体进行如图2所示实验。

②乙烧杯中状态1时为

您最近一年使用:0次
【推荐3】硝酸钾、氯化钾的溶解度曲线如图1所示。

(1)P点的含义是___________ 。
(2)当氯化钾中混有少量硝酸钾时,可用___________ 方法提纯氯化钾。
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是___________ ,其溶液的溶质质量分数为___________ (结果精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为___________ 。
(5)下列有关说法不正确的是___________ 。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾

(1)P点的含义是
(2)当氯化钾中混有少量硝酸钾时,可用
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为
(5)下列有关说法不正确的是
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
您最近一年使用:0次