学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份进行实验,结果如下:

(1)上表中m的数值是_____ ;
(2)反应中矿石有剩余是第_____次实验;
(3)这种石灰石矿中碳酸钙的质量分数是_____;
(4)稀盐酸中溶质的质量分数是多少?_____

| 实 验 | 一 | 二 | 三 | 四 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | m | 4.4 | 4.4 |
(2)反应中矿石有剩余是第_____次实验;
(3)这种石灰石矿中碳酸钙的质量分数是_____;
(4)稀盐酸中溶质的质量分数是多少?_____
更新时间:2019-10-05 15:28:42
|
相似题推荐
计算题
|
较难
(0.4)
名校
【推荐1】某纯碱样品中含有少量NaCl,小华同学取该样品23g全部溶解于200水中,再逐滴加入160g稀盐酸。反应中产生气体的质量与盐酸的用量关系如图所示。

(1)产生的二氧化碳的质量是_____克;
(2)样品中碳酸钠的质量为多少克?
(3)此时所得到的溶液中氯化钠的质量分数为多少?(结果精确到0.1%)

(1)产生的二氧化碳的质量是_____克;
(2)样品中碳酸钠的质量为多少克?
(3)此时所得到的溶液中氯化钠的质量分数为多少?(结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关信息回答问题。

(1)人体缺钙易出现的疾病是_______ ,这时除在医生指导下服用保健药剂外,日常生活中要多摄入______ 等食物。
(2)该品牌补钙药剂中CaCO3的质量分数是_______ ,a的数值为_________ 。
(3)求5次盐酸加入后所得氯化钙的质量。

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |
(2)该品牌补钙药剂中CaCO3的质量分数是
(3)求5次盐酸加入后所得氯化钙的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某工厂排出的废水中含较多的NaOH和Na2CO3及其它有害物质,某同学为了测定废水中NaOH和Na2CO3的质量分数,取废水157. 4g逐滴加入稀盐酸至过量测得生成气体质量与所加盐酸质量关系如图所示(废水中只有NaOH和Na2CO3能与盐酸反应) ,生成气体全部逸出。请回答问题:

(1)稀盐酸加到80g时,溶液中的溶质是 。
(2)稀盐酸溶质的质量分数为 。
(3)稀盐酸滴加到153g时,所得溶液溶质质量分数是多少?

(1)稀盐酸加到80g时,溶液中的溶质是 。
(2)稀盐酸溶质的质量分数为 。
(3)稀盐酸滴加到153g时,所得溶液溶质质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某同学在实验室用石灰石(杂质不含钙元素,不溶于水也不与酸反应)和稀盐酸制取二氧化碳气体,回答下列问题:
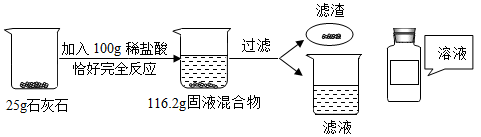
(1)石灰石与稀盐酸反应的化学方程式为_____ 。
(2)列出根据已知条件求解25g石灰石中参加反应的物质的质量(x)的比例式_____ 。
(3)配制100g上述稀盐酸,需质量分数36.5%的浓盐酸的质量为_____ 。
(4)向反应后的滤液中加入332.8g水,最终所得溶液溶质质量分数为_____ ,该溶液应装入_____ 保存,请在上图中填好标签_____ 。
(5)某工厂要用该石灰石制取生石灰,若要制得含杂质5%的生石灰112t,假设在煅烧的过程中有5%的原料损失,则需要上述石灰石的质量为_____ 。

(1)石灰石与稀盐酸反应的化学方程式为
(2)列出根据已知条件求解25g石灰石中参加反应的物质的质量(x)的比例式
(3)配制100g上述稀盐酸,需质量分数36.5%的浓盐酸的质量为
(4)向反应后的滤液中加入332.8g水,最终所得溶液溶质质量分数为
(5)某工厂要用该石灰石制取生石灰,若要制得含杂质5%的生石灰112t,假设在煅烧的过程中有5%的原料损失,则需要上述石灰石的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所取用的稀硫酸与铁样品恰好完全反应,实验数据如下表:
请你认真分析数据,回答下列问题:
(1)哪位同学所取的稀硫酸与铁样品恰好完全反应_______;
(2)计算样品中铁的质量分数________;
(3)计算恰好完全反应后所得溶液中溶质的质量分数__________。(烧杯的质量为25.4g;计算结果精确到1%)
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
(1)哪位同学所取的稀硫酸与铁样品恰好完全反应_______;
(2)计算样品中铁的质量分数________;
(3)计算恰好完全反应后所得溶液中溶质的质量分数__________。(烧杯的质量为25.4g;计算结果精确到1%)
您最近一年使用:0次




