某技术员在分析醋酸(CH3COOH)溶液中溶质的含量时,测得溶液中氧元素的质量分数为80%,则该溶液中醋酸的质量分数为_______ ?
2019八年级下·浙江·专题练习 查看更多[1]
(已下线)【初中科学2171】【初二下】1
更新时间:2019-12-09 21:21:48
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】食物的煎炸过程中会产生一种有害物质---丙烯醛,其化学式为 C3H4O。试回答下列问题:
(1)一个丙烯醛分子中含_______ 个原子;
(2)丙烯醛的相对分子质量是__________ ;
(3)丙烯醛中碳、氢、氧三种元素的质量比为____________ ;
(4)丙烯醛中氧元素的质量分数为____________ ( 保留至 0.1%)。
(1)一个丙烯醛分子中含
(2)丙烯醛的相对分子质量是
(3)丙烯醛中碳、氢、氧三种元素的质量比为
(4)丙烯醛中氧元素的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】“骨质疏松症”是由人体缺钙引起的.可服用补钙剂来治疗.乳酸钙(CaC6H10O6)是一种常见补钙剂,乳酸钙片每片含乳酸钙200mg,一个成年缺钙病人每天服用20片乳酸钙片剂可达到补钙目的.计算:
(1)乳酸钙中各元素的质量比_____?
(2)该成年缺钙病人改用喝牛奶(每100ml牛奶中含钙≥0.10g)来补钙,每天至少需要喝多少毫升牛奶_____?(可取整数)
(1)乳酸钙中各元素的质量比_____?
(2)该成年缺钙病人改用喝牛奶(每100ml牛奶中含钙≥0.10g)来补钙,每天至少需要喝多少毫升牛奶_____?(可取整数)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了10g该镁矿石粉末,加入过量的稀盐酸,充分反应后过滤、除杂,得到只含有 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
请计算:
(1)该镁矿石中镁元素的质量分数为________ 。(假设10g镁矿石中的镁元素全部转化到100g混合溶液中)
(2)加入的氢氧化钠溶液的溶质质量分数为_____________ 。
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:实验编号 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
加入氢氧化钠溶液质量/g | 10 | 10 | 10 | 10 | 10 | 10 |
烧杯中生成沉淀的总质量/g | 0 | 0.58 | 1.16 | 1.74 | 2.32 | 2.32 |
(1)该镁矿石中镁元素的质量分数为
(2)加入的氢氧化钠溶液的溶质质量分数为
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】碱式碳酸镁【Mg2(OH)2CO3】是一种高效的新型阻燃剂,一种工业制备原理的化学方程式如下: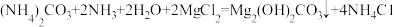 。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
已知相对分子质量:MgCl2-95;Mg2(OH)2CO3-142;NH4Cl-53.5
(1)Mg2(OH)2CO3中质量分数最大的元素是______ (填元素符号)。
(2)最后所得溶液中溶质的质量分数。
(3)欲将475 kgMgCl2溶液的溶质质量分数由20%变为24%,求需要加入MgC12固体的质量。
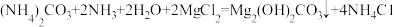 。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:已知相对分子质量:MgCl2-95;Mg2(OH)2CO3-142;NH4Cl-53.5
(1)Mg2(OH)2CO3中质量分数最大的元素是
(2)最后所得溶液中溶质的质量分数。
(3)欲将475 kgMgCl2溶液的溶质质量分数由20%变为24%,求需要加入MgC12固体的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】为了测定 20g 黄铜样品(仅由铜、锌组成)中单质铜的含量,做如下实验:
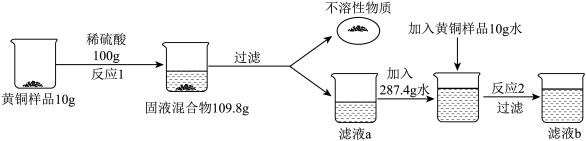
已知反应1和反应2产生氢气质量相同,请回答下列问题:
(1)发生反应的化学方程式为_______ ;
(2)根据已知条件列出10g黄铜样品中单质锌质量(x)的比例式_______ ;
(3)该黄铜样品中单质铜的质量分数为_______ ;
(4)经检验滤液b中只含一种溶质,则溶液中溶质的质量分数为_______ ;
(5)用98%的浓硫酸配制100g上述稀硫酸,需加水的质量为_______ ;
(6)工业上欲用纯度为70%的辉铜矿50t制取上述黄铜样品,若不计炼制过程中的损失,可制得该黄铜样品的质量为_______ 。

已知反应1和反应2产生氢气质量相同,请回答下列问题:
(1)发生反应的化学方程式为
(2)根据已知条件列出10g黄铜样品中单质锌质量(x)的比例式
(3)该黄铜样品中单质铜的质量分数为
(4)经检验滤液b中只含一种溶质,则溶液中溶质的质量分数为
(5)用98%的浓硫酸配制100g上述稀硫酸,需加水的质量为
(6)工业上欲用纯度为70%的辉铜矿50t制取上述黄铜样品,若不计炼制过程中的损失,可制得该黄铜样品的质量为
您最近一年使用:0次



