一碳化学是以分子中只含有一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学,合成气(CO、H2)可通过甲烷(CH4)的重整得到,例如CH4+H2O═CO+3H2。合成气可制取21世纪的新型燃料二甲醚。请阅读以下生产流程,回答问题:
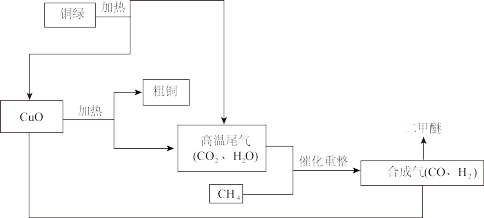
(1)铜绿[化学式为Cu2(OH)2CO3]是由_____ 种元素组成的,其中碳元素、氧元素的质量比为_____ 。
(2)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得。用合成气制二甲醚时,还产生了水,写出该反应的化学方程式:_____ 。
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。仅用合成气为原料不可能 得到的物质是_____ (填字母序号)。
A 草酸(H2C2O4) B 甲醇(CH3OH) C 尿素[CO(NH2)2]

(1)铜绿[化学式为Cu2(OH)2CO3]是由
(2)二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得。用合成气制二甲醚时,还产生了水,写出该反应的化学方程式:
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。仅用合成气为原料
A 草酸(H2C2O4) B 甲醇(CH3OH) C 尿素[CO(NH2)2]
更新时间:2019-12-14 23:44:18
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】汽车安全气囊中的填充物主要成分是NaN3,KNO3和SiO2。
(1)汽车发生猛烈碰撞时,NaN3分解,生成甲、乙两种单质,有关的化学方程式为_____ ;
(2)硝酸钾的作用是与可能会对人体造成伤害的单质甲反应,生成单质乙和两种氧化物,请写出该反应的化学方程式_____ ;
(3)生成的两种氧化物分别与SiO2反应,从理论上计算可知,SiO2与NaN3的质量比宜大于_____ 。
(1)汽车发生猛烈碰撞时,NaN3分解,生成甲、乙两种单质,有关的化学方程式为
(2)硝酸钾的作用是与可能会对人体造成伤害的单质甲反应,生成单质乙和两种氧化物,请写出该反应的化学方程式
(3)生成的两种氧化物分别与SiO2反应,从理论上计算可知,SiO2与NaN3的质量比宜大于
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如下:
表格中“X、Y”分别为_____ ;若要使生成物中无物质M,需要再增加氧气的质量为_____ g。
| 物质(纯净物) | 乙醇 | 氧气 | 二氧化碳 | 水 | M |
| 反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.2 | X | Y |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】已知某白色固体混合物A中可能含有MgCl2、BaCl2、Na2SO4、NaOH、CaCO3五种物质中的两种或多种。小路同学想分析其成分,她进行了实验探究,实验过程及出现的现象如下图所示:(设实验过程中所有可能发生的反应均恰好完全反应)
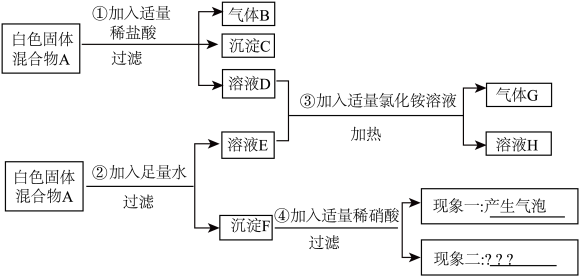
根据上述实验信息和分析推理,试回答下列问题:
(1)沉淀C的化学式为______ ,气体G的化学式为_______ 。
(2)上图中现象二为(至少答一条)____________ 。
(3)溶液D中肯定大量存在的阴离子是(写离子符号)_________ 。
(4)步骤②中发生反应的化学方程式为_______ 。
(5)步骤③中可能发生反应的一个化学方程式为____ 。
(6)由上述信息可推知,固体混合物A中一定不存在的物质是(写化学式)___ 你的理由是____ 。

根据上述实验信息和分析推理,试回答下列问题:
(1)沉淀C的化学式为
(2)上图中现象二为(至少答一条)
(3)溶液D中肯定大量存在的阴离子是(写离子符号)
(4)步骤②中发生反应的化学方程式为
(5)步骤③中可能发生反应的一个化学方程式为
(6)由上述信息可推知,固体混合物A中一定不存在的物质是(写化学式)
您最近一年使用:0次
【推荐2】如右图所示,A、B、C是初中化学中常见液体、气体和固体,气球套在试管口且保证密封性能良好。
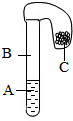
(1)若A能使紫色石蕊变红色,B为空气,将金属固体C倒入试管中产生气泡,同时气球因膨胀而鼓起来。则A是(填化学式)_________ ,金属固体C是(填化学式) ____________ ,发生反应的化学方程式是 ________________________________ ;
(2)若B为空气,将黑色固体C倒入试管中产生气泡,同时气球因膨胀而鼓起来。则A是(填化学式)_________ ,黑色固体C是(填化学式) ____________ ,发生反应的化学方程式是 __________________________________ ;
(3)若A是水,将气球中的固体C倒入试管中,气球很快被吸入试管中,则气体B是(填化学式)___________ ,固体C是(填化学式) ______________ 。

(1)若A能使紫色石蕊变红色,B为空气,将金属固体C倒入试管中产生气泡,同时气球因膨胀而鼓起来。则A是(填化学式)
(2)若B为空气,将黑色固体C倒入试管中产生气泡,同时气球因膨胀而鼓起来。则A是(填化学式)
(3)若A是水,将气球中的固体C倒入试管中,气球很快被吸入试管中,则气体B是(填化学式)
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】蛇纹石矿主要由MgO、 、
、 、
、 组成。由蛇纹石制取碱式碳酸镁的实验步骤如图1所示:查阅资料:几种物质沉淀和溶解时的pH如图2所示。
组成。由蛇纹石制取碱式碳酸镁的实验步骤如图1所示:查阅资料:几种物质沉淀和溶解时的pH如图2所示。______ 。
(2) 不能过量,若
不能过量,若 过量,可能导致
过量,可能导致______ ,造成产品不纯、产率下降。
(3)进行环节Ⅰ时,需控制溶液pH=6~7,此时原溶液中没有沉淀的金属阳离子是______ (写离子符号)。
(4)根据上述制取碱式碳酸镁的工艺流程的信息,请设计一个将某石灰石(成分只考虑碳酸钙和二氧化硅)提纯得到纯净的碳酸钙的简单的实验方案:取少量该石灰石样品,______ 。
 、
、 、
、 组成。由蛇纹石制取碱式碳酸镁的实验步骤如图1所示:查阅资料:几种物质沉淀和溶解时的pH如图2所示。
组成。由蛇纹石制取碱式碳酸镁的实验步骤如图1所示:查阅资料:几种物质沉淀和溶解时的pH如图2所示。
(2)
 不能过量,若
不能过量,若 过量,可能导致
过量,可能导致(3)进行环节Ⅰ时,需控制溶液pH=6~7,此时原溶液中没有沉淀的金属阳离子是
(4)根据上述制取碱式碳酸镁的工艺流程的信息,请设计一个将某石灰石(成分只考虑碳酸钙和二氧化硅)提纯得到纯净的碳酸钙的简单的实验方案:取少量该石灰石样品,
您最近一年使用:0次
【推荐1】氢能是一种“绿色”能源,其制取与储存是氢能综合利用的关键点。
(1)氢气的制取
①电解水可制取氢气,装置如图所示,常温下 a 管内气体的体积是 10 mL,b 管内气体的化学式是______ 。
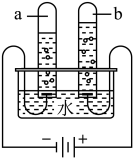
②经测量,b 管内气体的体积略小于理论值。可能的原因是______ (填序号)
A.常温下 H2的溶解度小于 O2的溶解度
B.b 管内产生了 O3
C.水槽中 KOH 的浓度偏小,导致溶液导电能力偏弱
③催化剂条件下,可利用太阳能分解水来制取氢气。与电解水制取氢气相比,从能量的角度,分析该方法制取氢气的优点是______ 。
(2)水热分解可得氢气。高温下水分解体系中微粒含量与温度的关系如图所示。
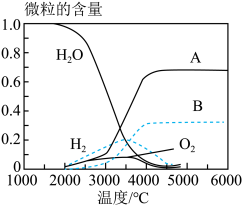
已知:
①温度低于 2000℃时,体系内 H2O 含量没有改变,其原因是______ 。
②曲线 A、B 对应的微粒是原子,曲线 A 对应的微粒是______ (填化学式)。
③从元素守恒角度分析,曲线 A、B 所对应原子的个数比是______ 。
(3)氢气的储存
①一种镁铜合金可用于储氢。将镁、铜单质按质量比为 3∶4 的比例在一定温度下熔炼得到镁铜合金。该镁铜合金的化学式是______ 。
②该镁铜合金完全吸氢后所得混合物与过量盐酸充分反应,整个过程中释放出 H2的量应为______ 的之和。
(1)氢气的制取
①电解水可制取氢气,装置如图所示,常温下 a 管内气体的体积是 10 mL,b 管内气体的化学式是

②经测量,b 管内气体的体积略小于理论值。可能的原因是
A.常温下 H2的溶解度小于 O2的溶解度
B.b 管内产生了 O3
C.水槽中 KOH 的浓度偏小,导致溶液导电能力偏弱
③催化剂条件下,可利用太阳能分解水来制取氢气。与电解水制取氢气相比,从能量的角度,分析该方法制取氢气的优点是
(2)水热分解可得氢气。高温下水分解体系中微粒含量与温度的关系如图所示。

已知:
①温度低于 2000℃时,体系内 H2O 含量没有改变,其原因是
②曲线 A、B 对应的微粒是原子,曲线 A 对应的微粒是
③从元素守恒角度分析,曲线 A、B 所对应原子的个数比是
(3)氢气的储存
①一种镁铜合金可用于储氢。将镁、铜单质按质量比为 3∶4 的比例在一定温度下熔炼得到镁铜合金。该镁铜合金的化学式是
②该镁铜合金完全吸氢后所得混合物与过量盐酸充分反应,整个过程中释放出 H2的量应为
您最近一年使用:0次
【推荐2】阅读下列材料,完成下面小题:
含氯消毒剂可以有效杀灭病毒,其中二氧化氯是国际公认的第四代消毒剂。二氧化氯消毒片(如图3)具有高效、快速、广谱的消毒特点,能有效杀灭细菌繁殖体、细菌芽孢、真菌、病毒等,在水中很少形成有害副产品,使用安全,但本品易潮解失效。图1是其使用时部分反应的微观过程,转化Ⅱ中溶液的pH变化如图2所示。
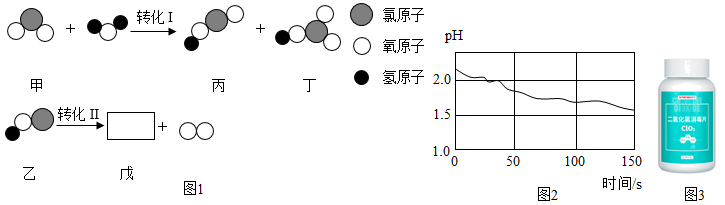
1.氯在元素周期表中相关信息如图,两个氯原子能构成一个氯气分子。下列说法正确的是
2.下列关于转化Ⅰ、转化Ⅱ的说法正确的是
3.下列关于二氧化氯的说法错误的是
含氯消毒剂可以有效杀灭病毒,其中二氧化氯是国际公认的第四代消毒剂。二氧化氯消毒片(如图3)具有高效、快速、广谱的消毒特点,能有效杀灭细菌繁殖体、细菌芽孢、真菌、病毒等,在水中很少形成有害副产品,使用安全,但本品易潮解失效。图1是其使用时部分反应的微观过程,转化Ⅱ中溶液的pH变化如图2所示。

1.氯在元素周期表中相关信息如图,两个氯原子能构成一个氯气分子。下列说法正确的是

| A.1个氯气分子中含有17个电子 | B.氯原子在化学反应中易失去1个电子 |
| C.含氯消毒剂中的“氯”指氯元素 | D.氯的相对原子质量为34.45g |
| A.转化Ⅰ属于复分解反应 |
| B.转化Ⅱ中氧元素的化合价没有发生变化 |
| C.相同条件下戊的酸性比乙强 |
| D.丙、丁组成元素相同,故它们化学性质也相同 |
| A.二氧化氯由1个氯原子和2个氧原子构成 | B.二氧化氯消毒时能使蛋白质变性 |
| C.二氧化氯应密封保存 | D.不能在铁桶中配制二氧化氯消毒水 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】(1)用化学用语填空:
①氯气分子____ ;②电解水过程中不变的微粒____ ;
(2)写出下列反应的化学方程式:①工业上用磁铁矿来炼铁:____ ;②2017年5月18我国首次试采可燃冰(CH4·nH2O)宣告成功,可燃冰分解后,可释放出水和天然气,请写出天然气完全燃烧的化学方程式:____ ;
(3)如图是A、B两种固体物质的溶解度曲线.回答:
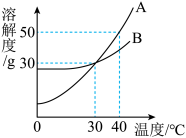
①要使接近饱和的A溶液变为饱和溶液,可采取的方法是__ ;
②在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A____ B(选填“大于”、“小于”或“等于”);
③30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为____ g才能变成饱和溶液;
④当A中混有少量B时,用____ 方法可以得到固体A.
①氯气分子
(2)写出下列反应的化学方程式:①工业上用磁铁矿来炼铁:
(3)如图是A、B两种固体物质的溶解度曲线.回答:

①要使接近饱和的A溶液变为饱和溶液,可采取的方法是
②在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A
③30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为
④当A中混有少量B时,用
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】现有CaCO3和CaO的固体混合物,其中Ca与C的质量比为10:1,则该混合物中Ca与O的质量比为___________ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】铜是人类最早使用的金属之一,炼铜工艺的发展史如图所示。
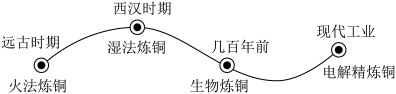
(1)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁釜,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是_____ 。
(2)生物炼铜是先将硫化铜(CuS)在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,这个过程需要保证温度不能过高,原因是_____ 。
(3)电解精炼铜过程中,电能转化为_____ 能。
青铜器的锈蚀产物较为复杂,一般分为有害锈和无害锈两种。无害锈可以保护青铜器,包括CuO、 、
、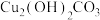 等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质。
等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质。
(4)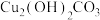 的形成是铜与空气中的
的形成是铜与空气中的_____ 共同作用的结果。
(5)现取2.22g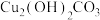 加强热,剩余固体质量随温度变化曲线如题图所示。请判断C点对应的固体物质为
加强热,剩余固体质量随温度变化曲线如题图所示。请判断C点对应的固体物质为_____ 。

(6)有害锈主要为碱式氯化铜[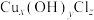 ],蓝绿色固体,其受热会分解生成CuO、
],蓝绿色固体,其受热会分解生成CuO、 和HCl。取一定量蓝绿色固体,充分加热,将生成的
和HCl。取一定量蓝绿色固体,充分加热,将生成的 用足量的吸水剂氯化钙充分吸收,生成的HCl用烧碱溶液充分吸收。实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜中,
用足量的吸水剂氯化钙充分吸收,生成的HCl用烧碱溶液充分吸收。实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜中,
_____ 。

(1)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁釜,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是
(2)生物炼铜是先将硫化铜(CuS)在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,这个过程需要保证温度不能过高,原因是
(3)电解精炼铜过程中,电能转化为
青铜器的锈蚀产物较为复杂,一般分为有害锈和无害锈两种。无害锈可以保护青铜器,包括CuO、
 、
、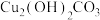 等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质。
等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质。(4)
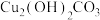 的形成是铜与空气中的
的形成是铜与空气中的(5)现取2.22g
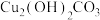 加强热,剩余固体质量随温度变化曲线如题图所示。请判断C点对应的固体物质为
加强热,剩余固体质量随温度变化曲线如题图所示。请判断C点对应的固体物质为
(6)有害锈主要为碱式氯化铜[
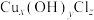 ],蓝绿色固体,其受热会分解生成CuO、
],蓝绿色固体,其受热会分解生成CuO、 和HCl。取一定量蓝绿色固体,充分加热,将生成的
和HCl。取一定量蓝绿色固体,充分加热,将生成的 用足量的吸水剂氯化钙充分吸收,生成的HCl用烧碱溶液充分吸收。实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜中,
用足量的吸水剂氯化钙充分吸收,生成的HCl用烧碱溶液充分吸收。实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜中,
您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
名校
解题方法
【推荐3】阅读下面科普短文“白色污染”是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的形象称呼。普通塑料袋主要成分是聚乙烯【化学式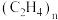 】高分子化合物,难降解处理。科学家经过不懈的研究,从饱含淀粉质的玉米中制取乳酸(
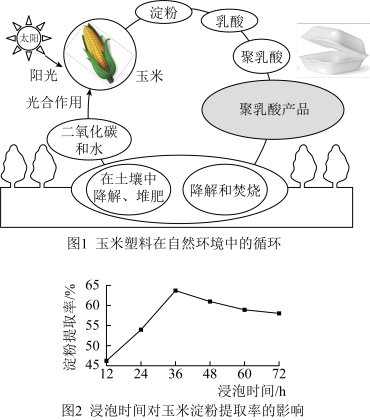
】高分子化合物,难降解处理。科学家经过不懈的研究,从饱含淀粉质的玉米中制取乳酸(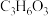 ),再经过聚合反应生产出颗粒状高分子材料聚乳酸来替代塑料,被称为玉米塑料。如图1玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分。
),再经过聚合反应生产出颗粒状高分子材料聚乳酸来替代塑料,被称为玉米塑料。如图1玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分。
玉米粒中营养成分含量最多的是淀粉(70%-75%)。玉米淀粉普遍采用的是湿法提取,浸泡是玉米淀粉提取工艺中的核心环节。在50°C时,相同浸泡液中(水、0.5%亚硫酸钠溶液、0.5%乳酸溶液按8:1:1配比),测定浸泡时间与玉米淀粉提取率的关系如图2。玉米是传统粮食,现在和将来,玉米塑料将广泛应用于食品包装、一次性产品、工程、日用、农业、医疗等领域,它将变成盒子、瓶子和手机等产品,科技是多神奇啊!
依据文章内容回答下列问题。
(1)玉米塑料制品最终被微生物完全分解成的物质是________ 。
(2)聚乙烯中碳元素与氢元素的质量比是________ 。
(3)亚硫酸钠 )中硫元素的化合价是
)中硫元素的化合价是________ 。
(4)下列说法正确的是________(填序号)
(5)由图2得出的结论是,在实验研究范围内,其它条件相同时,________ 。
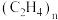 】高分子化合物,难降解处理。科学家经过不懈的研究,从饱含淀粉质的玉米中制取乳酸(
】高分子化合物,难降解处理。科学家经过不懈的研究,从饱含淀粉质的玉米中制取乳酸(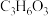 ),再经过聚合反应生产出颗粒状高分子材料聚乳酸来替代塑料,被称为玉米塑料。如图1玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分。
),再经过聚合反应生产出颗粒状高分子材料聚乳酸来替代塑料,被称为玉米塑料。如图1玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分。玉米粒中营养成分含量最多的是淀粉(70%-75%)。玉米淀粉普遍采用的是湿法提取,浸泡是玉米淀粉提取工艺中的核心环节。在50°C时,相同浸泡液中(水、0.5%亚硫酸钠溶液、0.5%乳酸溶液按8:1:1配比),测定浸泡时间与玉米淀粉提取率的关系如图2。玉米是传统粮食,现在和将来,玉米塑料将广泛应用于食品包装、一次性产品、工程、日用、农业、医疗等领域,它将变成盒子、瓶子和手机等产品,科技是多神奇啊!

依据文章内容回答下列问题。
(1)玉米塑料制品最终被微生物完全分解成的物质是
(2)聚乙烯中碳元素与氢元素的质量比是
(3)亚硫酸钠
 )中硫元素的化合价是
)中硫元素的化合价是(4)下列说法正确的是________(填序号)
| A.玉米进行光合作用发生物理变化 | B.浸泡液属于混合物 |
| C.玉米粒富含糖类 | D.玉米塑料可以降解或焚烧 |
您最近一年使用:0次



