某厂生产的产品包装袋上标有Na2CO3 90%字样(杂质为NaCl)。为判断该产品是否合格,取12g样品放入烧杯中,加入100g稀盐酸,恰好完全反应。反应后所得溶液质量为107.6 g(产生的气体全部逸出,且NaCl不与盐酸反应)。试计算:
(1)计算产生二氧化碳的质量为多少g?
(2)所用稀盐酸中溶质的质量分数是多少(写出计算过程)。
(1)计算产生二氧化碳的质量为多少g?
(2)所用稀盐酸中溶质的质量分数是多少(写出计算过程)。
更新时间:2019-12-16 22:59:05
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气质量的实验数据如表所示,试求:
(1)m=________。
(2)此黄铜样品中锌的质量分数是多少?
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(mL) | 10 | 10 | 10 |
| 生成氢气的质量(g) | 0.08 | m | 0.04 |
(1)m=________。
(2)此黄铜样品中锌的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
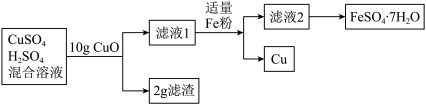
【推荐2】某工厂废水经初步处理后可得CuSO4和H2SO4的混合溶液,化学兴趣小组设计实验模拟后续处理过程,并得到了 Cu 和另一种重要化工原料绿矾(FeSO4·7H2O)。其过程如图:_____ g。
(2)若原混合溶液质量为200g,求混合溶液中H2SO4的质量分数(写出计算过程)。
(3)若反应消耗11.2gFe,求理论上得到的绿矾中硫酸亚铁的质量(写出计算过程)。
(2)若原混合溶液质量为200g,求混合溶液中H2SO4的质量分数(写出计算过程)。
(3)若反应消耗11.2gFe,求理论上得到的绿矾中硫酸亚铁的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】向10g大理石样品(杂质不溶于水,也不与盐酸反应)中分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。
(1)碳酸钙中钙元素的质量分数为______ ;
(2)计算所用稀盐酸中溶质的质量分数。
(3)反应后溶液的质量为______ 。

(1)碳酸钙中钙元素的质量分数为
(2)计算所用稀盐酸中溶质的质量分数。
(3)反应后溶液的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某碳酸钠样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,现称取该样品11 g,加入到盛有50 g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g。计算:
(1)生成气体的质量;
(2)样品中碳酸钠的质量分数。(最终的结果精确到0.1%;化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑)
(1)生成气体的质量;
(2)样品中碳酸钠的质量分数。(最终的结果精确到0.1%;化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为测定某种贝壳中碳酸钙的质量分数,取12.5g贝壳,逐滴加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应也不溶于水)。请计算:

(1)12.5g这种贝壳中碳酸钙的质量是_____ g。
(2)所用稀盐酸中溶质的质量分数。

(1)12.5g这种贝壳中碳酸钙的质量是
(2)所用稀盐酸中溶质的质量分数。
您最近一年使用:0次



