化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,写出产生气泡的化学方程式______ 。充分反应后静置,发现试管中有灰白色沉淀。
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小轩认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小轩的猜想,理由是____ 。
小琬认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
小恬认为灰白色沉淀为脱落的镁粉细颗粒。
【实验探究1】
基于以上探究与分析,原有猜想均遭到了否定。
【查阅资料】
HCl+AgNO3=HNO3+AgCl↓,AgCl是一种白色沉淀。
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了______ 气体。再将湿润的石试液浸泡过的滤纸条悬于试管口,试纸变____ 色。
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀,据文献介绍,碱式氯化镁的化学通式可表示为Mgx(OH)yClz,其不溶于水,能与酸反应。
【反思拓展】
做镁与稀盐酸反应的实验时,镁条的用量_____ 。
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小轩认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小轩的猜想,理由是
小琬认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
小恬认为灰白色沉淀为脱落的镁粉细颗粒。
【实验探究1】
| 实验操作 | 现象 | 结论 |
| ①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体 | 小琬猜想错误 |
| ②取适量白色沉淀加入足量稀盐酸中 | 小恬猜想错误 |
基于以上探究与分析,原有猜想均遭到了否定。
【查阅资料】
HCl+AgNO3=HNO3+AgCl↓,AgCl是一种白色沉淀。
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀,据文献介绍,碱式氯化镁的化学通式可表示为Mgx(OH)yClz,其不溶于水,能与酸反应。
【反思拓展】
做镁与稀盐酸反应的实验时,镁条的用量
更新时间:2019-12-18 06:53:34
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】化学规律建立在实验基础之上,质量守恒定律可以用许多化学实验加以验证。
(1)小东同学按照如图所示实验进行验证。一段时间后,可以观察到铁钉表面出现_____ (填现象),其反应的化学方程式为_____ ,反应前后天平读数不变,但溶液颜色变化不明显。

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
【实验分析】
实验1中溶液颜色几乎不变的原因可能是_____ (填序号)。
A 铁与饱和硫酸铜溶液不反应
B 实验中铁严重生锈,表面形成了一层氧化膜,阻止了反应的进一步进行
C 生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D 水与铁发生反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸
铜溶液中含有少量的硫酸,所以总质量减小的原因可能是_____ 。
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水;将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置还需的改进方法是_____ 。

(1)小东同学按照如图所示实验进行验证。一段时间后,可以观察到铁钉表面出现

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
| 实验内容 | 实验现象 | |
| 实验1 | 烧杯中换成饱和硫酸铜溶液 | ① 1小时后溶液颜色几乎不变 ②天平读数不变 ③铁钉表面有变化 |
| 实验2 | 铁钉换成锌粒 | ①溶液颜色明显变浅 ②天平读数减小 ③锌粒表面有变化 |
实验1中溶液颜色几乎不变的原因可能是
A 铁与饱和硫酸铜溶液不反应
B 实验中铁严重生锈,表面形成了一层氧化膜,阻止了反应的进一步进行
C 生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D 水与铁发生反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸
铜溶液中含有少量的硫酸,所以总质量减小的原因可能是
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水;将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置还需的改进方法是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】回收废旧干电池能减少对水和土壤的污染。某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气。已知氢气密度比空气小且难溶于水,提供装置如图。

(1)用排空气法收集氢气装置应选择
___________ (填编号)。
(2)若用排水法收集并测定气体的体积,气体从C装置导管口
___________ (填“a”或“b”)进;选用仪器D的作用是
___________ 。
【探究】探究影响锌与稀硫酸反应快慢的因素。
【提出问题】锌与硫酸反应快慢受哪些因素影响?
【猜想与假设】I、可能与锌的纯度有关;II、可能与硫酸的浓度有关。
【设计方案和实验】
该小组同学用不同纯度的锌和不同浓度的稀硫酸进行如下实验。
【分析、得出结论】
(3)比较实验①和实验③,可以得到的结论是
___________ 。
(4)为了研究杂质对反应快慢的影响,需比较实验
___________ (填编号)。
【反思】
(5)与同浓度的硫酸反应,锌的形状可能影响反应快慢。请设计实验方案进行验证
___________ 。
(6)还有什么因素会影响锌与硫酸的反应快慢呢?请提出猜想并设计实验验证:
___________ 。

(1)用排空气法收集氢气装置应选择
(2)若用排水法收集并测定气体的体积,气体从C装置导管口
【探究】探究影响锌与稀硫酸反应快慢的因素。
【提出问题】锌与硫酸反应快慢受哪些因素影响?
【猜想与假设】I、可能与锌的纯度有关;II、可能与硫酸的浓度有关。
【设计方案和实验】
该小组同学用不同纯度的锌和不同浓度的稀硫酸进行如下实验。
实验编号 | 试剂 | H2体积(mL)(均收集10分钟) | |
不同纯度的锌(均取1g) | 不同浓度的稀硫酸(均取30mL) | ||
| ① | 纯锌 | 30% | 564.3 |
| ② | 含杂质的锌 | 30% | 634.7 |
| ③ | 纯锌 | 20% | 449.3 |
(3)比较实验①和实验③,可以得到的结论是
(4)为了研究杂质对反应快慢的影响,需比较实验
【反思】
(5)与同浓度的硫酸反应,锌的形状可能影响反应快慢。请设计实验方案进行验证
(6)还有什么因素会影响锌与硫酸的反应快慢呢?请提出猜想并设计实验验证:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】“垃圾是放错了位置的资源!”将垃圾分类回收可以变废为宝。我校环保小组收集了某种铝制易拉罐,剪成条状并打磨后,与纯铝片相互刻画,发现纯铝片表面有划痕。
【发现问题】
根据所学知识,结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝;可能还含有镁、铁;
②铝能与氢氧化钠溶液反应:
③镁和铁不能与氢氧化钠溶液反应。
【作出猜想】该易拉罐的金属组成除铝外,可能还含有镁、铁中的一种或两种。
【实验设计】
小明取打磨后的铝制易拉罐样品按如下方案进行实验:
【实验结论】小明得出该易拉罐是由铝和铁组成
【反思评价】
(3)其他同学分析后认为小明的实验方案不严谨,理由是_______ 。墩墩同学认为应该补充下列实验:取步骤(1)中少量滤渣于试管中,加入某种金属的化合物溶液后,如果无现象产生,则小明的结论正确。你认为加入的化合物溶液理论上可以是_______ (填序号)。
A.硫酸镁溶液 B.硫酸铜溶液 C.硫酸亚铁溶液
【拓展应用】
(4)铝制品被大量使用,其中一个重要原因是铝具有良好的抗腐蚀性能,铝具有良好的抗蚀性能的原因是_______ (用化学方程式表示)。
【发现问题】
根据所学知识,结合上述现象,可得出该易拉罐不是纯铝制作。那么易拉罐中除铝外,还含有什么金属呢?
【查阅资料】①铝制易拉罐中的主要成分是铝;可能还含有镁、铁;
②铝能与氢氧化钠溶液反应:

③镁和铁不能与氢氧化钠溶液反应。
【作出猜想】该易拉罐的金属组成除铝外,可能还含有镁、铁中的一种或两种。
【实验设计】
小明取打磨后的铝制易拉罐样品按如下方案进行实验:
| 实验步骤 | 实验现象 | 解释与结论 |
| (1)取一定量的样品于烧杯中,加入足量的溶液,充分反应后过滤、洗涤、干燥 | 固体表面有大量气泡产生;过滤后得到滤渣 | 样品中含铝 |
| (2)取少量上述滤渣于试管中,加入足量的稀盐酸 | 有气泡产生,溶液变成浅绿色 | 样品中含铁,铁与稀盐酸的反应的化学程式为 |
【反思评价】
(3)其他同学分析后认为小明的实验方案不严谨,理由是
A.硫酸镁溶液 B.硫酸铜溶液 C.硫酸亚铁溶液
【拓展应用】
(4)铝制品被大量使用,其中一个重要原因是铝具有良好的抗腐蚀性能,铝具有良好的抗蚀性能的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】随着中国航天事业快速发展,中国人探索太空的脚步会迈得更大、更远。过氧化钠( )可用作航天器中的供氧剂。化学小组在老师的指导下,对过氧化钠的组成和有关性质进行如下探究。
)可用作航天器中的供氧剂。化学小组在老师的指导下,对过氧化钠的组成和有关性质进行如下探究。
①过氧化钠溶于水时,与水反应生成氧气和一种碱性物质;
②在通常状况下,过氧化钠与 反应生成碳酸钠和氧气;
反应生成碳酸钠和氧气;
③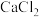 固体具有强烈的吸水性,且不与
固体具有强烈的吸水性,且不与 反应。
反应。
【了解组成】
(1) 的阴离子是由2个氧原子结合形成的带负电荷的原子团,该离子的化学符号是
的阴离子是由2个氧原子结合形成的带负电荷的原子团,该离子的化学符号是________ 。
【探究性质】
(2)少量过氧化钠溶于过量水中,得到________ (填化学式)溶液。向该溶液中加入稀盐酸,如图1中符合溶液 变化曲线的是
变化曲线的是________ (填序号)。
【进行实验】用如图2所示装置进行实验,可以探究过氧化钠与 反应生成氧气等的原理。有关主要实验过程和现象为:
反应生成氧气等的原理。有关主要实验过程和现象为:
①按图示连接装置并检查其气密性。
②从吹气口持续吹气,气体一分为三,分别进入A、B、C三支试管里。
③吹气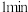 ,用手摸A的底部,感觉发烫,带火星的木条在A中能复燃;用手摸C的底部,感觉温度无明显变化,带火星的木条在C中不复燃;同时观察到B中的脱脂棉发生燃烧现象。
,用手摸A的底部,感觉发烫,带火星的木条在A中能复燃;用手摸C的底部,感觉温度无明显变化,带火星的木条在C中不复燃;同时观察到B中的脱脂棉发生燃烧现象。
【实验结论】
(3)由A、B试管中的现象,可得出的实验结论是 与
与 的反应为放热反应;对比A、C试管中的现象,可得出的实验结论是
的反应为放热反应;对比A、C试管中的现象,可得出的实验结论是_______ 。
【讨论与交流】
(4)某同学对A中残留物的成分产生好奇,为探究其中所含的成分,设计如下实验:
①中反应的化学方程式为________ 。
【拓展延伸】
(5)向长期曝露于空气中的过氧化钠里加入足量的白醋,产生的气体中除氧气外,还可能含有________ (填物质名称)。过氧化钠必须密封保存,否则极易变质。
 )可用作航天器中的供氧剂。化学小组在老师的指导下,对过氧化钠的组成和有关性质进行如下探究。
)可用作航天器中的供氧剂。化学小组在老师的指导下,对过氧化钠的组成和有关性质进行如下探究。
①过氧化钠溶于水时,与水反应生成氧气和一种碱性物质;
②在通常状况下,过氧化钠与
 反应生成碳酸钠和氧气;
反应生成碳酸钠和氧气;③
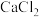 固体具有强烈的吸水性,且不与
固体具有强烈的吸水性,且不与 反应。
反应。【了解组成】
(1)
 的阴离子是由2个氧原子结合形成的带负电荷的原子团,该离子的化学符号是
的阴离子是由2个氧原子结合形成的带负电荷的原子团,该离子的化学符号是【探究性质】
(2)少量过氧化钠溶于过量水中,得到
 变化曲线的是
变化曲线的是【进行实验】用如图2所示装置进行实验,可以探究过氧化钠与
 反应生成氧气等的原理。有关主要实验过程和现象为:
反应生成氧气等的原理。有关主要实验过程和现象为:①按图示连接装置并检查其气密性。
②从吹气口持续吹气,气体一分为三,分别进入A、B、C三支试管里。
③吹气
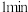 ,用手摸A的底部,感觉发烫,带火星的木条在A中能复燃;用手摸C的底部,感觉温度无明显变化,带火星的木条在C中不复燃;同时观察到B中的脱脂棉发生燃烧现象。
,用手摸A的底部,感觉发烫,带火星的木条在A中能复燃;用手摸C的底部,感觉温度无明显变化,带火星的木条在C中不复燃;同时观察到B中的脱脂棉发生燃烧现象。【实验结论】
(3)由A、B试管中的现象,可得出的实验结论是
 与
与 的反应为放热反应;对比A、C试管中的现象,可得出的实验结论是
的反应为放热反应;对比A、C试管中的现象,可得出的实验结论是【讨论与交流】
(4)某同学对A中残留物的成分产生好奇,为探究其中所含的成分,设计如下实验:
| 操作步骤 | 实验现象 | 实验结论 |
| ①取少量A中固体,加水溶解,向该溶液中加入足量 | 有白色沉淀产生 | A中残留物中含有碳酸钠 |
| ②取①中上层清液,向其中加入无色酚酞溶液 | 溶液变红 | A中残留物中含有 |
【拓展延伸】
(5)向长期曝露于空气中的过氧化钠里加入足量的白醋,产生的气体中除氧气外,还可能含有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐2】某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们提出了如下假设:
【猜 想】猜想一:没有变质; 猜想二:部分变质; 猜想三:________ 。
【查阅资料】Na2CO3溶液呈碱性。
【进行实验】对猜想二进行验证。
写出现象③的化学方程式_________ 。
【反思】氢氧化钠溶液必须密封保存。氢氧化钠溶液变质的原因(用化学方程表示)______ 。
【猜 想】猜想一:没有变质; 猜想二:部分变质; 猜想三:
【查阅资料】Na2CO3溶液呈碱性。
【进行实验】对猜想二进行验证。
| 实验步骤 | 实验现象 | 结论 |
| 1取少许该溶液于试管中,滴入适量的 | 猜想二正确 | |
| 2静置上述溶液,取上层清液少许于另一支试管中,滴入几滴 |
写出现象③的化学方程式
【反思】氢氧化钠溶液必须密封保存。氢氧化钠溶液变质的原因(用化学方程表示)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三个实验小组围绕“酸碱中和反应”在老师引导下开展探究活动,请你参与学习。
【查阅资料】Na2SO4溶液呈中性
【演示实验】
(1)将一定量的稀硫酸加入到盛有无色酚酞试液和NaOH溶液的小烧杯中。当看到_________ 现象,证明稀硫酸和氢氧化钠溶液发生了化学反应。
【学生板演】
(2)该反应的化学方程式为_________ 。
【提出问题】部分同学产生了疑问:反应后溶液中溶质除了酚酞,还有什么呢?
【假设猜想】
(3)针对疑问,大家纷纷提出猜想,甲组同学的猜想如下:
猜想一:只有Na2SO4溶液;猜想二:有Na2SO4溶液和___________ 溶液
猜想三:有Na2SO4溶液和NaOH溶液;猜想四:有H2SO4溶液、Na2SO4溶液和NaOH溶液
乙组同学对以上猜想提出质疑,认为一种猜想是不合理的,不合理的猜想是___________ 。
【实验探究】
(4)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有________ 。
为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
【得出结论】
(5)通过探究确定猜想________ 是正确的。请写出方案2的化学方程式________ 。
【评价反思】
(6)老师对同学们能用多种方法进行探究,得出正确结论给予肯定。同时指出实验方案中有一个是错误的,错误的原因是___________ 。
【反思拓展】
(7)在分析反应后所得物质的成分时,除了考虑生成物,还应考虑_________ 。
【查阅资料】Na2SO4溶液呈中性
【演示实验】
(1)将一定量的稀硫酸加入到盛有无色酚酞试液和NaOH溶液的小烧杯中。当看到
【学生板演】
(2)该反应的化学方程式为
【提出问题】部分同学产生了疑问:反应后溶液中溶质除了酚酞,还有什么呢?
【假设猜想】
(3)针对疑问,大家纷纷提出猜想,甲组同学的猜想如下:
猜想一:只有Na2SO4溶液;猜想二:有Na2SO4溶液和
猜想三:有Na2SO4溶液和NaOH溶液;猜想四:有H2SO4溶液、Na2SO4溶液和NaOH溶液
乙组同学对以上猜想提出质疑,认为一种猜想是不合理的,不合理的猜想是
【实验探究】
(4)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有
为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
| 实验方案 | 1.测溶液pH | 2.滴加Na2CO3溶液 | 3.滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(5)通过探究确定猜想
【评价反思】
(6)老师对同学们能用多种方法进行探究,得出正确结论给予肯定。同时指出实验方案中有一个是错误的,错误的原因是
【反思拓展】
(7)在分析反应后所得物质的成分时,除了考虑生成物,还应考虑
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某石化公司石油化工厂的一个装有液化气等轻烃的罐区发生爆炸。当地某化学兴趣小组想探究爆炸现场附近的空气中是否含有CO气体。设计实验方案如下:
【实验目的】确定气体样品中是否含有CO。
【实验原理】①除去收集的空气样品中的氧气;②假设该样品中不含除CO之外的其他能与Fe2O3反应的物质。甲装置中发生的化学反应方程式是_______ 。
【实验仪器】

请根据他们的设计回答下列问题:
(1)在实验时,上述仪器的连接顺序是:丙→乙→甲→乙。其中乙装置需要使用两次,第一次的作用是_________ 。
(2)根据实验中出现的________ 或________ 现象,能判断出爆炸现场附近的空气样品中有较多CO。
(3)从环境保护的角度考虑,你认为该实验的设计是否存在缺陷,如果有,该如何改进?_________ 。
【实验目的】确定气体样品中是否含有CO。
【实验原理】①除去收集的空气样品中的氧气;②假设该样品中不含除CO之外的其他能与Fe2O3反应的物质。甲装置中发生的化学反应方程式是
【实验仪器】

请根据他们的设计回答下列问题:
(1)在实验时,上述仪器的连接顺序是:丙→乙→甲→乙。其中乙装置需要使用两次,第一次的作用是
(2)根据实验中出现的
(3)从环境保护的角度考虑,你认为该实验的设计是否存在缺陷,如果有,该如何改进?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等。化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示。同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究。

【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
铁与氯化铁溶液在常温下发生反应生成氯化亚铁:Fe+2FeCl3═3FeCl2。
【作出猜想】久置固体中一定有活性炭可能含有及________________ 。
【实验探究】下表是小组同学设计的实验方案和记录的实验报告,请你补充完整:
【实验释疑】确定了久置“双吸剂”固体的成分后,几位同学又提出了以下问题:
Ⅰ步骤③中加入试剂 Y 后,溶液却不呈黄色的原因是_______________ 。
Ⅱ查阅资料得知,铁粉作脱氧剂时,为了达到更好的脱氧效果,会向其中加入少量的氯化钠。请设计实验说明氯化钠存在时铁粉脱氧效果更好:__________________ 。

【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
铁与氯化铁溶液在常温下发生反应生成氯化亚铁:Fe+2FeCl3═3FeCl2。
【作出猜想】久置固体中一定有活性炭可能含有及
【实验探究】下表是小组同学设计的实验方案和记录的实验报告,请你补充完整:
| 实验操作 | 实验现象 | 实验结论 |
| ①取3g固体样品仔细观察,用磁铁吸固体,置于烧杯中,加20 mL水,用温度计测量溶解前后液体温度,过滤,所得滤液备用。 | 固体样品中有黑色粉末, 较多白色固体及少量红棕色固体,少量黑色粉末可以被磁 铁吸引,温度计温度无明显变化,得到无色滤液 | 样品中 |
| ②取少量①中无色滤液,滴加无色酚酞。 | 溶液有无色变为红色 | 样品中一定含Ca(OH)2 |
| ③取少量固体样品放入试管 中,加适量的试剂Y,用带导管的单孔橡皮塞塞紧试管口,导管另一端伸入澄清石灰水中。 | 试管中固体逐渐减少,有大量无色气体产生,得到浅绿色溶液,有少量黑色固体不溶,澄清的石灰水变浑浊。 | 样品中含有活性炭、CaCO3 |
【实验释疑】确定了久置“双吸剂”固体的成分后,几位同学又提出了以下问题:
Ⅰ步骤③中加入试剂 Y 后,溶液却不呈黄色的原因是
Ⅱ查阅资料得知,铁粉作脱氧剂时,为了达到更好的脱氧效果,会向其中加入少量的氯化钠。请设计实验说明氯化钠存在时铁粉脱氧效果更好:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组同学做了如图所示的实验。向试管a中滴加一定量的稀硫酸,再滴加硫酸铜溶液时,没有出现蓝色沉淀,得到b溶液。请回答下列问题:

(1)试管a中发生反应的化学方程式为______ 。
(2)为确定b溶液中溶质的成分,做了如下探究。
【提出问题】b溶液中的溶质由什么物质组成?
【做出猜想】
甲同学猜想:CuSO4和Na2SO4
乙同学猜想:CuSO4、Na2SO4和NaOH
丙同学的猜想:CuSO4、Na2SO4和H2SO4
【进行讨论】小组同学一致认为______ 同学的猜想是错误的,理由是______ 。
【设计实验】请完成实验报告
【反思拓展】通过以上实验操作及现象,你认为用硫酸铜溶液______ (填“能”或“不能”)证明稀硫酸与氢氧化钠溶液发生了反应。

(1)试管a中发生反应的化学方程式为
(2)为确定b溶液中溶质的成分,做了如下探究。
【提出问题】b溶液中的溶质由什么物质组成?
【做出猜想】
甲同学猜想:CuSO4和Na2SO4
乙同学猜想:CuSO4、Na2SO4和NaOH
丙同学的猜想:CuSO4、Na2SO4和H2SO4
【进行讨论】小组同学一致认为
【设计实验】请完成实验报告
| 实验操作 | 实验现象 | 实验结论 |
| 向b溶液中加入过量的铁丝 | 丙同学的猜想正确 |
您最近一年使用:0次



