老师利用图示装置进行甲、乙对比实验,探究温度对一氧化碳还原氧化铁反应的影响.
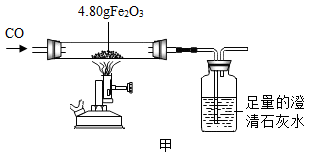
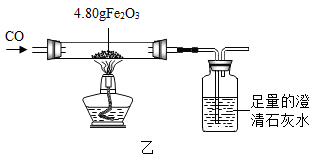
(1)从实验安全和环保角度考虑,图示装置还应采取的改进措施是_____ .
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
①小雨同学查阅资料后发现四氧化三铁能被磁铁吸引、在常温与稀盐酸反应无气体产生、与硫酸铜溶液不反应,故猜想乙组的生成物为四氧化三铁.他又发现m2恰好为_____ g(结果保留至0.01g),这可成为支持上述猜想的新证据.甲乙两组实验说明温度对一氧化碳和氧化铁反应有影响。
②若乙组的澄清石灰水变浑浊,写出乙组玻璃管内发生反应的化学方程式_____ 。
(3)在前面的学习中,出现过反应物种类相同,但_____ 不同而导致反应产物不同的情况,请举例说明 _____ .


(1)从实验安全和环保角度考虑,图示装置还应采取的改进措施是
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 称量黑色粉末质量/g | m1 | m2 |
| 2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
| 3 | 取黑色粉末,加入稀盐酸 | 全部溶解,有大量气泡 | 全部溶解,无气泡 |
| 4 | 取黑色粉末,加入足量硫酸铜溶液 | 有红色物质产生 | 无明显现象 |
①小雨同学查阅资料后发现四氧化三铁能被磁铁吸引、在常温与稀盐酸反应无气体产生、与硫酸铜溶液不反应,故猜想乙组的生成物为四氧化三铁.他又发现m2恰好为
②若乙组的澄清石灰水变浑浊,写出乙组玻璃管内发生反应的化学方程式
(3)在前面的学习中,出现过反应物种类相同,但
更新时间:2019-12-28 21:59:35
|
【知识点】 一氧化碳还原氧化铁实验解读
相似题推荐
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐1】我们的日常生活离不开金属,我校化学兴趣小组同学对金属的部分性质进行了研究。
【任务一】目前常用的1元硬币为钢芯镀镍合金,5角硬币为铜锌合金或钢芯镀铜合金,1角硬币为铝锌合金或不锈钢,请回答下列问题:
(1)铸造币的合金不需考虑的是________。
(2)硬币涉及的金属有Al、Ni(镍)、 ,已知
,已知 能发生如下反应:
能发生如下反应: ,则以上5种金属活动性由强到弱的顺序是
,则以上5种金属活动性由强到弱的顺序是__________________________ 。
【任务二】利用如图1装置探究铁与氧化铁化合的生成物成分。


【查阅资料】铁的氧化物有 ,其中只有Fe3O4能被磁铁吸引,某些铁的氧化物加热时能与氧气反应,二氧化碳与铁粉、铁的氧化物均不反应。
,其中只有Fe3O4能被磁铁吸引,某些铁的氧化物加热时能与氧气反应,二氧化碳与铁粉、铁的氧化物均不反应。
【提出猜想】
(3)猜想① ;猜想②Fe3O4;猜想③
;猜想②Fe3O4;猜想③________ 。
【实验步骤】
(4)①连接组装仪器,检查装置的气密性;
②称取 氧化铁粉末、质量为m的铁粉,均匀混合后,放入玻璃管;
氧化铁粉末、质量为m的铁粉,均匀混合后,放入玻璃管;
③通入 ,当观察到现象:
,当观察到现象:______ 出现时,夹上弹簧夹M,开始加热玻璃管;
④当固体全部呈黑色后,停止加热,将玻璃管中黑色粉末倒在滤纸上,取样滴加稀盐酸,无气泡产生,用磁铁吸引,粉末被部分吸引。
【实验结论】猜想③成立。
【问题讨论】
(5)实验中澄清石灰水的主要作用是:__________________________ 。
(6)根据工业炼铁的原理,用氧化铁和一氧化碳模拟炼铁,反应方程式是:_____________________________________ 。
【任务三】仍然用该装置(图1)称取 氧化铁粉末放在玻璃管中,通入一氧化碳还原这些氧化铁粉末。反应过程中可以看到澄清石灰水变浑浊,固体逐渐变成黑色,反应结束后,将玻璃管中黑色粉末倒在滤纸上,称得重量为
氧化铁粉末放在玻璃管中,通入一氧化碳还原这些氧化铁粉末。反应过程中可以看到澄清石灰水变浑浊,固体逐渐变成黑色,反应结束后,将玻璃管中黑色粉末倒在滤纸上,称得重量为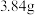 ,取样滴加稀盐酸,有气泡,用磁铁吸引,粉末被部分吸引。
,取样滴加稀盐酸,有气泡,用磁铁吸引,粉末被部分吸引。
查询资料发现管内剩余固体质量变化与反应温度关系如图2,理论上充分反应的情况下,氧化铁与一氧化碳开始反应后,逐步失去氧元素转化为不同的铁的氧化物。
(7)推测玻璃管中倒出黑色粉末的组成是______(填序号)。
(8)可推断此次反应结束前所达温度区间是______ 。
(9)此黑色粉末铁元素与氧元素质量比为______ 。
【任务一】目前常用的1元硬币为钢芯镀镍合金,5角硬币为铜锌合金或钢芯镀铜合金,1角硬币为铝锌合金或不锈钢,请回答下列问题:
(1)铸造币的合金不需考虑的是________。
| A.耐磨性 | B.抗腐蚀性 | C.色泽 | D.导电性 | E.价格 |
 ,已知
,已知 能发生如下反应:
能发生如下反应: ,则以上5种金属活动性由强到弱的顺序是
,则以上5种金属活动性由强到弱的顺序是【任务二】利用如图1装置探究铁与氧化铁化合的生成物成分。


【查阅资料】铁的氧化物有
 ,其中只有Fe3O4能被磁铁吸引,某些铁的氧化物加热时能与氧气反应,二氧化碳与铁粉、铁的氧化物均不反应。
,其中只有Fe3O4能被磁铁吸引,某些铁的氧化物加热时能与氧气反应,二氧化碳与铁粉、铁的氧化物均不反应。【提出猜想】
(3)猜想①
 ;猜想②Fe3O4;猜想③
;猜想②Fe3O4;猜想③【实验步骤】
(4)①连接组装仪器,检查装置的气密性;
②称取
 氧化铁粉末、质量为m的铁粉,均匀混合后,放入玻璃管;
氧化铁粉末、质量为m的铁粉,均匀混合后,放入玻璃管;③通入
 ,当观察到现象:
,当观察到现象:④当固体全部呈黑色后,停止加热,将玻璃管中黑色粉末倒在滤纸上,取样滴加稀盐酸,无气泡产生,用磁铁吸引,粉末被部分吸引。
【实验结论】猜想③成立。
【问题讨论】
(5)实验中澄清石灰水的主要作用是:
(6)根据工业炼铁的原理,用氧化铁和一氧化碳模拟炼铁,反应方程式是:
【任务三】仍然用该装置(图1)称取
 氧化铁粉末放在玻璃管中,通入一氧化碳还原这些氧化铁粉末。反应过程中可以看到澄清石灰水变浑浊,固体逐渐变成黑色,反应结束后,将玻璃管中黑色粉末倒在滤纸上,称得重量为
氧化铁粉末放在玻璃管中,通入一氧化碳还原这些氧化铁粉末。反应过程中可以看到澄清石灰水变浑浊,固体逐渐变成黑色,反应结束后,将玻璃管中黑色粉末倒在滤纸上,称得重量为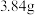 ,取样滴加稀盐酸,有气泡,用磁铁吸引,粉末被部分吸引。
,取样滴加稀盐酸,有气泡,用磁铁吸引,粉末被部分吸引。查询资料发现管内剩余固体质量变化与反应温度关系如图2,理论上充分反应的情况下,氧化铁与一氧化碳开始反应后,逐步失去氧元素转化为不同的铁的氧化物。
(7)推测玻璃管中倒出黑色粉末的组成是______(填序号)。
| A.是四氧化三铁和氧化铁的混合物 | B.是四氧化三铁和氧化亚铁的混合物 |
| C.是四氧化三铁和铁粉的混合物 | D.是氧化亚铁和铁粉的混合物 |
(9)此黑色粉末铁元素与氧元素质量比为
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐2】硫酸铜在纺织、印刷等行业有广泛用途。
Ⅰ.探究硫酸铜的制备
工业上可用铜屑、空气与稀硫酸在80℃条件下制备硫酸铜。如图所示是某研究性学习小组实验室模拟工业制备硫酸铜的装置。

(1)多孔球泡的作用为____________ 。
(2)该反的化学方程式为___________ 。
Ⅱ.探究硫酸铜的性质
实验一:研究性学习小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。这一现象激发起同学们的探究欲望:生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2中的一种或几种。
【查阅资料】①酸性高锰酸钾溶液呈紫红色,SO2能使酸性高锰酸钾溶液褪色。
② ,I2为碘单质,遇淀粉溶液变蓝。
,I2为碘单质,遇淀粉溶液变蓝。
【方案设计】依据上述猜想,研究性小组同学分别设计了如下方案:
(1)甲同学为确定是否含有SO2,他将气体通入酸性高锰钾溶液中,溶液颜色未发生变化,则该气体中___ SO2(填“有”或“无”)。
(2)乙同学认为只有O2,则可用___________ 来检验。实验证明乙同学的观点不正确。
(3)丙同学为判断是否含有O2,同时确定气体成分,设计了如下的实验装置:

【实验结论】A中观察到_____________ ,证明无O2;B中观察到_________________ ,证明该气体是H2。
【实验反思】大家认为丙同学在加热之前,应对气体先______________ 以确保安全。
实验二:小组同学又将过量的Na2CO3溶液滴入到CuSO4溶液中得到一种蓝绿色固体,将蓝绿色固体充分灼烧生成了CuO、H2O和CO2,从而确定其成分为碱式碳酸铜,化学式可表示为Cux(OH)yCOz。
【定量探究】为进一步确定碱式碳酸铜的化学式,小组同学准确称取蓝绿色固体32.0g,用如下装置(夹持仪器未画出)进行实验。

步骤1:打开止水夹K1、K2,关闭K3,通入空气,一段时间后关闭止水夹K1、K2,打开K3;
步骤2:点燃酒精灯,待C中硬质玻璃管中固体完全变成黑色粉末,打开止水夹K1,继续通入空气至冷却到室温。
【问题与讨论】
(1)A装置的作用是________________ 。
(2)硬质玻璃管中固体完全变成黑色粉末后继续通入空气的目的是______________ 。
【数据处理】
(1)若实验结束后,称量反应前后D装置增重3.6g,E中产生白色沉淀的质量为19.7g,则该蓝绿色固体的化学式为______________ 。
(2)E中用Ba(OH)2饱和溶液代替澄清石灰水的原因有:
①BaCO3的相对分子质量大于CaCO3,生成沉淀的质量大,称量误差小;
②__________________ 。
Ⅰ.探究硫酸铜的制备
工业上可用铜屑、空气与稀硫酸在80℃条件下制备硫酸铜。如图所示是某研究性学习小组实验室模拟工业制备硫酸铜的装置。

(1)多孔球泡的作用为
(2)该反的化学方程式为
Ⅱ.探究硫酸铜的性质
实验一:研究性学习小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。这一现象激发起同学们的探究欲望:生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2中的一种或几种。
【查阅资料】①酸性高锰酸钾溶液呈紫红色,SO2能使酸性高锰酸钾溶液褪色。
②
 ,I2为碘单质,遇淀粉溶液变蓝。
,I2为碘单质,遇淀粉溶液变蓝。【方案设计】依据上述猜想,研究性小组同学分别设计了如下方案:
(1)甲同学为确定是否含有SO2,他将气体通入酸性高锰钾溶液中,溶液颜色未发生变化,则该气体中
(2)乙同学认为只有O2,则可用
(3)丙同学为判断是否含有O2,同时确定气体成分,设计了如下的实验装置:

【实验结论】A中观察到
【实验反思】大家认为丙同学在加热之前,应对气体先
实验二:小组同学又将过量的Na2CO3溶液滴入到CuSO4溶液中得到一种蓝绿色固体,将蓝绿色固体充分灼烧生成了CuO、H2O和CO2,从而确定其成分为碱式碳酸铜,化学式可表示为Cux(OH)yCOz。
【定量探究】为进一步确定碱式碳酸铜的化学式,小组同学准确称取蓝绿色固体32.0g,用如下装置(夹持仪器未画出)进行实验。

步骤1:打开止水夹K1、K2,关闭K3,通入空气,一段时间后关闭止水夹K1、K2,打开K3;
步骤2:点燃酒精灯,待C中硬质玻璃管中固体完全变成黑色粉末,打开止水夹K1,继续通入空气至冷却到室温。
【问题与讨论】
(1)A装置的作用是
(2)硬质玻璃管中固体完全变成黑色粉末后继续通入空气的目的是
【数据处理】
(1)若实验结束后,称量反应前后D装置增重3.6g,E中产生白色沉淀的质量为19.7g,则该蓝绿色固体的化学式为
(2)E中用Ba(OH)2饱和溶液代替澄清石灰水的原因有:
①BaCO3的相对分子质量大于CaCO3,生成沉淀的质量大,称量误差小;
②
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐3】金属材料在我们各行各业发挥着重要的作用:
Ⅰ.2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)建造航母用到了钛合金,构成金属钛的粒子是_______ (填“原子”“分子”或“离子”),工业制钛有一种反应为TiF4+2H2SO4=4HF+2X+TiO2,X的化学式为_______ 。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与_______ 接触而锈蚀。
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_______ (填字母)。
A.稀盐酸中加入足量铁粉后,再加入铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
Ⅱ.2020年12月,“嫦娥五号”返回器携带的月球土壤样品,对于全面科学探测月球地质、资源等方面的信息有重要意义。经分析土壤样品中含有金、银、铁、铝,现要从混合金属中回收金、银,将该混合金属放入一定量的硝酸银溶液中充分反应后过滤,得到滤渣和浅绿色溶液,向滤渣中加入一定量稀盐酸,有气泡产生。
(4)滤渣中一定含有的金属是_______ 。
(5)硝酸银溶液和铁反应的化学方程式为_______ 。
Ⅲ.铁不仅能与硝酸银溶液反应,还能与氧气、酸、CuSO4溶液等多种物质发生化学反应。化学兴趣小组在课外资料中发现,铁和Fe2O3竟然也能发生化学反应。
【提出问题】铁和Fe2O3反应的产物是什么?
【查阅资料】①在FeO、Fe2O3、Fe3O4中,Fe2O3是红棕色,其余都是黑色;FeO在空气中会很快被氧化成Fe2O3;只有Fe3O4有磁性。②二氧化碳可用作该反应的保护气。③铁的氧化物都能与酸溶液反应。
【猜想与假设】根据质量守恒定律,请你猜想铁和Fe2O3反应的产物:①只有FeO;②只有Fe3O4;③____ 。
【进行实验】(6)按下图装好药品(铁粉过量),连好仪器(装入药品前已检查装置的气密性)。

(7)轻推注射器活塞通入二氧化碳,估计玻璃管里空气_______ ,停止通入二氧化碳。
(8)点燃酒精喷灯加热药品,等到固体粉末全部变黑,再熄灭酒精喷灯。
(9)当长柄V形玻璃管冷却至室温时,检验黑色粉末成分。检验过程如下:
【探究结论】铁和Fe2O3能发生化合反应,有关的化学方程式是_______ 。
【反思评价】(10)本实验中的保护气,既能用二氧化碳气体,也能用_______ 。
(11)一氧化碳还原某铁的氧化物时,得到铁的质量为16.8克,同时生成13.2克的二氧化碳,则该铁的氧化物的化学式为_______ 。
Ⅰ.2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)建造航母用到了钛合金,构成金属钛的粒子是
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是
A.稀盐酸中加入足量铁粉后,再加入铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
Ⅱ.2020年12月,“嫦娥五号”返回器携带的月球土壤样品,对于全面科学探测月球地质、资源等方面的信息有重要意义。经分析土壤样品中含有金、银、铁、铝,现要从混合金属中回收金、银,将该混合金属放入一定量的硝酸银溶液中充分反应后过滤,得到滤渣和浅绿色溶液,向滤渣中加入一定量稀盐酸,有气泡产生。
(4)滤渣中一定含有的金属是
(5)硝酸银溶液和铁反应的化学方程式为
Ⅲ.铁不仅能与硝酸银溶液反应,还能与氧气、酸、CuSO4溶液等多种物质发生化学反应。化学兴趣小组在课外资料中发现,铁和Fe2O3竟然也能发生化学反应。
【提出问题】铁和Fe2O3反应的产物是什么?
【查阅资料】①在FeO、Fe2O3、Fe3O4中,Fe2O3是红棕色,其余都是黑色;FeO在空气中会很快被氧化成Fe2O3;只有Fe3O4有磁性。②二氧化碳可用作该反应的保护气。③铁的氧化物都能与酸溶液反应。
【猜想与假设】根据质量守恒定律,请你猜想铁和Fe2O3反应的产物:①只有FeO;②只有Fe3O4;③
【进行实验】(6)按下图装好药品(铁粉过量),连好仪器(装入药品前已检查装置的气密性)。

(7)轻推注射器活塞通入二氧化碳,估计玻璃管里空气
(8)点燃酒精喷灯加热药品,等到固体粉末全部变黑,再熄灭酒精喷灯。
(9)当长柄V形玻璃管冷却至室温时,检验黑色粉末成分。检验过程如下:
| 检验操作及现象 | 检验结果 | |
| a | 黑色粉末暴露在空气中不变色 | 黑色粉末中一定没有 |
| b | 用磁铁靠近,黑色粉末能完全被吸引。 | 黑色粉末中一定含有铁和 |
| c | 取少量的黑色粉末装入试管,滴加足量的 | 确认猜想 |
【反思评价】(10)本实验中的保护气,既能用二氧化碳气体,也能用
(11)一氧化碳还原某铁的氧化物时,得到铁的质量为16.8克,同时生成13.2克的二氧化碳,则该铁的氧化物的化学式为
您最近一年使用:0次



