将5%的NaOH溶液逐滴加入到10g稀硫酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
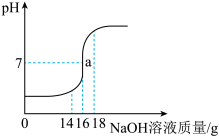
(1)a点的含义是_________________;
(2)当计入NaOH溶液的质量为18g时,溶液中存在的阴离子有_____________;
(3)稀硫酸中溶质的质量分数为____。

(1)a点的含义是_________________;
(2)当计入NaOH溶液的质量为18g时,溶液中存在的阴离子有_____________;
(3)稀硫酸中溶质的质量分数为____。
更新时间:2020-01-06 21:03:04
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某公司生产的新型融雪剂的成分是无水CaCl2和少量的氯化钠,为测定融雪剂中氯化钙的含量,化学兴趣小组的同学称取该样品15g,加水充分溶解,得到溶液50g,然后取一定质量分数的碳酸钠溶液100g平均分五次加入,充分振荡,实验数据见表。请你分析数据并进行有关计算。
(1)上表中x的数值为______ 。第______ 次加入的碳酸钠与氯化钙恰好完全反应。
(2)样品中氯化钙的质量分数是多少?
(3)恰好完全反应时过滤,所得不饱和溶液的溶质质量分数是多少?
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入碳酸钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成沉淀的质量/g | 2.5 | x | 7.5 | 10 | 10 |
(2)样品中氯化钙的质量分数是多少?
(3)恰好完全反应时过滤,所得不饱和溶液的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室用34g过氧化氢溶液和适量的二氧化锰混合制取氧气,生成氧气的质量与反应时间的关系如图所示。

(1)反应生成氧气的质量为_____g。
(2)实验所用的过氧化氢溶液的浓度为____。

(1)反应生成氧气的质量为_____g。
(2)实验所用的过氧化氢溶液的浓度为____。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10克,再用100克稀硫酸逐滴滴入样品中。实验情况如图所示。求:

(1)铜锌合金中,铜的质量是_____克。Zn的质量分数是_____。
(2)所用稀硫酸溶质的质量分数是多少?
(3)恰好完全反应时所得溶液溶质的质量分数是多少?(计算结果保留到0.1%)

(1)铜锌合金中,铜的质量是_____克。Zn的质量分数是_____。
(2)所用稀硫酸溶质的质量分数是多少?
(3)恰好完全反应时所得溶液溶质的质量分数是多少?(计算结果保留到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】图1是碳酸钙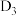 片标签的部分信息。化学社团为测定该药片中碳酸钙的量是否与标签相符,进行实验:取8片药片,研碎后逐渐加入质量分数为7.3%的稀盐酸,充分反应。实验相关数据如图2所示(假设其他成分不参加反应)。
片标签的部分信息。化学社团为测定该药片中碳酸钙的量是否与标签相符,进行实验:取8片药片,研碎后逐渐加入质量分数为7.3%的稀盐酸,充分反应。实验相关数据如图2所示(假设其他成分不参加反应)。______ (填一种仪器)。
(2)恰好完全反应时消耗稀盐酸的质量为______ g。
(3)计算每片药片中碳酸钙的质量并判断是否与标签相符。(写出计算过程)
(4)科学用药,健康生活。下列说法正确的有______(填序号,双选)。
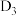 片标签的部分信息。化学社团为测定该药片中碳酸钙的量是否与标签相符,进行实验:取8片药片,研碎后逐渐加入质量分数为7.3%的稀盐酸,充分反应。实验相关数据如图2所示(假设其他成分不参加反应)。
片标签的部分信息。化学社团为测定该药片中碳酸钙的量是否与标签相符,进行实验:取8片药片,研碎后逐渐加入质量分数为7.3%的稀盐酸,充分反应。实验相关数据如图2所示(假设其他成分不参加反应)。
(2)恰好完全反应时消耗稀盐酸的质量为
(3)计算每片药片中碳酸钙的质量并判断是否与标签相符。(写出计算过程)
(4)科学用药,健康生活。下列说法正确的有______(填序号,双选)。
| A.钙是人体中的常量元素,故服用钙片越多越好 |
| B.钙片嚼食服用,可使碳酸钙与胃酸反应更充分 |
| C.钙片需密封保存,是因为室温下碳酸钙易分解 |
| D.饮用牛奶、豆浆,也可补充人体所需的钙元素 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】现有含CuSO4和H2SO4的混合溶液,向其中加入一定溶质质量分数的NaOH溶液实验过程中生成沉淀的质量与加入NaOH溶液的质量关系如图所示:
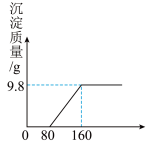
(1)恰好完全反应时,产生沉淀的质量 g;
(2)求该NaOH溶液的溶质质量分数。

(1)恰好完全反应时,产生沉淀的质量 g;
(2)求该NaOH溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某石化厂有一种石油产品含有溶质质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。计算:
(1)如果清洗100kg这种石油产品,要多少千克的NaOH?
(2)该石化厂的工人经过技术改造,采用Ca(OH)2来中和这些残余硫酸。如处理100kg这种石油产品,可以节约多少经费?
温馨提示:和市场价格如下表:
(1)如果清洗100kg这种石油产品,要多少千克的NaOH?
(2)该石化厂的工人经过技术改造,采用Ca(OH)2来中和这些残余硫酸。如处理100kg这种石油产品,可以节约多少经费?
温馨提示:和市场价格如下表:
名称 | NaOH | Ca(OH)2 |
价格(元/kg) | 24.00 | 6.00 |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
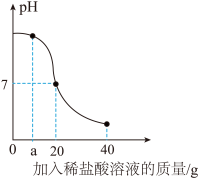
【推荐2】某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液 pH 的变化图像如图所示。______ (填“增大”或减小)。
(2)图中 a 点对应溶液中所含阴离子为______ (写微粒符号)。
(3)实验中有 20g 溶质质量分数为 4%的氢氧化钠溶液恰好完全参与反应,根据图示计算恰好完全反应时所得溶液中溶质氯化钠的质量分数。(写出计算过程,计算结果精确到 0.1%)
(2)图中 a 点对应溶液中所含阴离子为
(3)实验中有 20g 溶质质量分数为 4%的氢氧化钠溶液恰好完全参与反应,根据图示计算恰好完全反应时所得溶液中溶质氯化钠的质量分数。(写出计算过程,计算结果精确到 0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】实验室里有一瓶标签破损的硫酸溶液。为测定该瓶硫酸溶液中溶质的质量分数,小西同学在烧杯中加入50g该硫酸溶液,然后向烧杯中滴加溶质质量分数为10%的氢氧化钠溶液,边加边搅拌,随着氢氧化钠溶液的加入,溶液pH的变化情况如下表所示。
请分析并计算:
(1)a、b、c三种溶液中只含一种溶质的是__________________ (填字母)。
(2)该瓶硫酸溶液中溶质的质量分数。
| 氢氧化钠溶液的质量/g | 溶液的pH | 所得溶液 |
| 30 | pH<7 | a |
| 40 | pH=7 | b |
| 50 | pH>7 | c |
(1)a、b、c三种溶液中只含一种溶质的是
(2)该瓶硫酸溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取20g稀硫酸样品于烧杯中,将10%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示,回答下列问题:

(1)a点溶液中的溶质是_____(填化学式)。
(2)该反应的实质是_____。
(3)计算该稀硫酸的溶质质量分数。

(1)a点溶液中的溶质是_____(填化学式)。
(2)该反应的实质是_____。
(3)计算该稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某硫酸厂废水中含有少量硫酸,为达标排放,对废水中硫酸的含量进行检测.
(1)稀释浓硫酸的实验操作是______________ .
(2)取废水样品147g,向其中加入几滴酚酞试液,再逐滴加入NaOH溶液(假设废水中其它成分均不和NaOH反应)至恰好完全反应,恰好完全反应时现象是______________ .总共消耗6%的NaOH溶液20g.试计算废水中硫酸的质量分数(计算结果精确到0.1 % )._________ (写出计算过程)
(1)稀释浓硫酸的实验操作是
(2)取废水样品147g,向其中加入几滴酚酞试液,再逐滴加入NaOH溶液(假设废水中其它成分均不和NaOH反应)至恰好完全反应,恰好完全反应时现象是
您最近一年使用:0次




