某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
(1)上表中m的数值是多少?
(2)试计算这种石灰石矿中碳酸钙的质量分数。
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.54 | 3.08 | 4.5 | m |
(1)上表中m的数值是多少?
(2)试计算这种石灰石矿中碳酸钙的质量分数。
更新时间:2020-01-10 20:16:56
|
【知识点】 含杂质的化学方程式计算解读
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】有一包久置在空气中的生石灰,经测定已经变质(可能含有氧化钙、氢氧化钙和碳酸钙中的一种或几种)。现取该生石灰样品 15g,加入 200g7.3%的稀盐酸,恰好完全反应,得到二氧化碳 3.3g。试计算:
(1)15g样品中碳酸钙的质量。
(2)15g该样品未变质时的质量。
(1)15g样品中碳酸钙的质量。
(2)15g该样品未变质时的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某同学将12g大理石样品放入盛有50g稀盐酸的烧杯中,结果恰好完全反应(杂质不溶于水也不与盐酸反应)。经测定反应后烧杯中溶液质量为55.6g。
请计算:稀盐酸中溶质的质量分数
请计算:稀盐酸中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
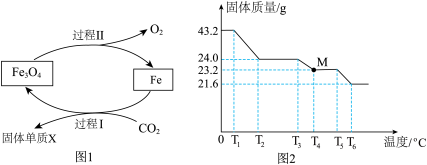
【推荐3】CO2作为最主要的温室气体,其低能耗捕集、转化和利用正受到世界的关注。科学家研究发现,在一定条件下可以将CO2转化为某固体单质X,反应原理如图1所示。_______ (填化学式)。
(2)过程Ⅱ的化学方程式为 ,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
(3)杭州亚运会生产电动车锂电池所用到的草酸亚铁(FeC2O4)在不同温度下分解能得到不同的铁的氧化物,同时放出气体。
i.FeC2O4中碳元素的化合价为_______ 。
ii.43.2gFeC2O4受热分解所得固体质量随温度的变化如图2所示。_______ °C时,固体M开始分解;请通过计算分析固体M的化学式_______ 。
(2)过程Ⅱ的化学方程式为
 ,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)
,若用1160t含Fe3O480%的磁铁矿,理论上可制得FeO的质量是多少?(写出计算过程)(3)杭州亚运会生产电动车锂电池所用到的草酸亚铁(FeC2O4)在不同温度下分解能得到不同的铁的氧化物,同时放出气体。
i.FeC2O4中碳元素的化合价为
ii.43.2gFeC2O4受热分解所得固体质量随温度的变化如图2所示。
您最近一年使用:0次



