某种手机电路板中含有Fe、Cu、Au、Ag、Ni(镍,银白色金属)等金属,如图是某工厂回收部分金属的流程图。已知:2Cu+O2+2H2SO4 2CuSO4+2H2O
2CuSO4+2H2O

(1)写出滤液②中金属阳离子符号_____ 。
(2)写出滤液③和铁粉发生反应的一个化学方程式_____ 。
(3)Fe、Cu、Ag、Ni在溶液中的活动性由强到弱的顺序依次是_____ 。
 2CuSO4+2H2O
2CuSO4+2H2O
(1)写出滤液②中金属阳离子符号
(2)写出滤液③和铁粉发生反应的一个化学方程式
(3)Fe、Cu、Ag、Ni在溶液中的活动性由强到弱的顺序依次是
更新时间:2020-01-19 22:20:07
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】金属及金属材料在生产、生活中有广泛的应用。近年来,我省多地纷纷开展文明城市创建工作,垃圾分类回收是其中一项重要举措。 某市街道垃圾桶如图所示,请回答下列问题:

(1)使用铝合金做内筒的优点是_______ (写出一点即可)
(2)某品牌饮料的空易拉罐应收入________ (填“可回收”或“不可回收”)筒中。
(3)铁制品锈蚀的过程,实际上是铁制品跟空气中的______ 发生化学反应的过程,除去铁制品表面的铁锈可用稀盐酸,反应的化学方程式为__________________ 。
(4)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中。 充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是_________ (填字母)。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3—
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+

(1)使用铝合金做内筒的优点是
(2)某品牌饮料的空易拉罐应收入
(3)铁制品锈蚀的过程,实际上是铁制品跟空气中的
(4)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中。 充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3—
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】将过量的锌粒逐渐加入到一定质量FeC12和CuC12的混合溶液中,如图所示为反应过程溶液中FeCl2的质量随加入锌的质量的变化情况。

(1)请写出B点时发生反应的化学方程式。
(2)C点溶液中的溶质是什么?(写化学式)
(3)反应后溶液的质量比反应前溶液的质量增大,请说明原因。

(1)请写出B点时发生反应的化学方程式。
(2)C点溶液中的溶质是什么?(写化学式)
(3)反应后溶液的质量比反应前溶液的质量增大,请说明原因。
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐3】已知A、B、C、D、E是初中化学常见的不同类别的物质。B是一种应用最广泛的金属;C溶液与B的反应是现代湿法冶金的先驱;D是一种氧化物。图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物生成物及反应条件省略)。请回答下列问题:

(1)A物质属于_______ (填物质类别)。
(2)E的化学式是_______ 。
(3)能比较两种金属活动性强弱的反应是_______ (填数字序号)。
(4)若B→D发生燃烧现象,写出D→B反应的化学方程式_______ 。

(1)A物质属于
(2)E的化学式是
(3)能比较两种金属活动性强弱的反应是
(4)若B→D发生燃烧现象,写出D→B反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】医学上经常用硫酸亚铁糖衣片给贫血患者补铁。某兴趣小组的同学对糖衣片中硫酸亚铁晶体的制备和组成产生了兴趣并对其进行探究。
探究:利用实验室的废水回收铜、制备硫酸亚铁晶体。

(1)步骤①的化学方程式是___________ 。
(2)固体甲中含有的物质是___________ (填化学式,下同);红色固体是__________ ;分离铁粉和铜粉最简易的物理方法是________________ 。
探究:利用实验室的废水回收铜、制备硫酸亚铁晶体。

(1)步骤①的化学方程式是
(2)固体甲中含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】锌是人体必需的微量元素之一,对儿童的生长发育及免疫力的提高起非常大的作用。回答下列与金属有关的问题:
(1)黄铜(铜锌合金)片和纯铜片相互刻画,有划痕的是______ 。
(2)我国古代将炉甘石(ZnCO3)和木炭粉混合后,加热到约800℃可得到锌。主要发生的化学反应:①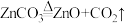 ②
② 下列说法不正确的是______。
下列说法不正确的是______。
(3)实验室常用锌粒与稀硫酸反应制取氢气。
①计算实验室用6.5g锌粒与稀硫酸完全反应,最多可生成氢气的质量为______ g。
②若验证锌粒与稀硫酸反应后的溶液中有硫酸剩余,取反应后的溶液加入下列试剂,合理的选择是______ 。
A.生锈的铁钉 B.氯化钡溶液
C.稀氢氧化钠溶液 D.锌粒
(1)黄铜(铜锌合金)片和纯铜片相互刻画,有划痕的是
(2)我国古代将炉甘石(ZnCO3)和木炭粉混合后,加热到约800℃可得到锌。主要发生的化学反应:①
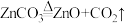 ②
② 下列说法不正确的是______。
下列说法不正确的是______。| A.X的化学式为CO2 |
| B.反应①和②所属的基本反应类型相同 |
| C.反应前后固体的质量不变 |
| D.反应②前后元素的化合价均未发生改变 |
①计算实验室用6.5g锌粒与稀硫酸完全反应,最多可生成氢气的质量为
②若验证锌粒与稀硫酸反应后的溶液中有硫酸剩余,取反应后的溶液加入下列试剂,合理的选择是
A.生锈的铁钉 B.氯化钡溶液
C.稀氢氧化钠溶液 D.锌粒
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】A为黑色固体,A、C、D、Y都是氧化物,E是单质,F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,如图是它们之间的相互转化关系。请回答:

(1)则B为______ E______ G______ (填化学式)
(2)X溶液中所含有的溶质为______ 、______ ,F溶液显浅绿色,其中所含有的溶质是______ 。
(3)写出反应③中生成无色气体的化学方程式______ ; 写出反应④中生成黑色固体的化学方程式______ ;
(4)指出物质G和A在加热条件下发生的化学反应的基本反应类型______ 。

(1)则B为
(2)X溶液中所含有的溶质为
(3)写出反应③中生成无色气体的化学方程式
(4)指出物质G和A在加热条件下发生的化学反应的基本反应类型
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图(小部分产物略去)。
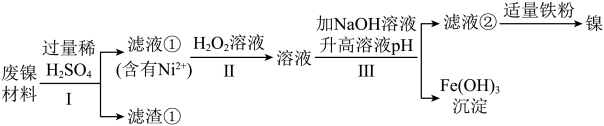
查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
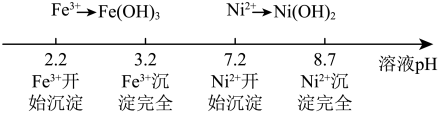
b.Fe3+ 、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图
(1)步骤Ⅰ的操作为______ 。
(2)滤渣①的成分为______ 。
(3)单质Fe参与反应的化学方程式为______ 。(任写一个)
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为______ (填序号)。
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为______ 。

查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe3+ 、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图

(1)步骤Ⅰ的操作为
(2)滤渣①的成分为
(3)单质Fe参与反应的化学方程式为
(4)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为
A.pH=1 B.pH=2 C.pH=6 D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】在实验课中,各小组作了如下实验。
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶液相同。
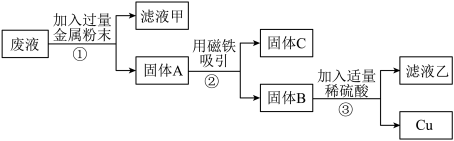
操作③的名称是_____ 实验中所加的过量金属粉末是_____ ,则固体C是_____ 。
| 实验编号 | 1 | 2 | 3 | 4 |
| 实验操作 | 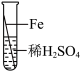 | 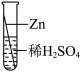 | 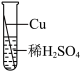 |  |

操作③的名称是
您最近一年使用:0次



