金属材料在生产、生活中有着广泛的应用。
(1)下列应用中使用金属材料的有_____ (填字母)。
(2)化学小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如图实验方案:

根据实验①判断出镁的金属活动性比铁强,依据的现象是_____ ,根据实验②的现象得出的结论是_____ 。
(3)向溶质为AgNO3、Cu(NO3)2、NaNO3的混合物溶液中,加入一定量的镁粉,充分反应后过滤,得到蓝色溶液,则所得蓝色溶液中一定含有的溶质是_____ 。
(4)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示。下列相关判断中,正确的是_____ 。
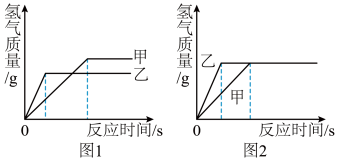
A 甲是锌,乙是铁
B 甲是铁,乙是锌
C 图1中消耗硫酸的质量甲>乙
D 图2中金属乙与硫酸充分反应后,金属乙一定有剩余
(1)下列应用中使用金属材料的有
 |  |  |  |
| A、用金、银、铜等制作奖牌 | B、用化学纤维制作毛绒玩具 | C、用新型钢材建造“鸟巢” | D、用聚氯乙烯制造“水立方”外层膜 |

根据实验①判断出镁的金属活动性比铁强,依据的现象是
(3)向溶质为AgNO3、Cu(NO3)2、NaNO3的混合物溶液中,加入一定量的镁粉,充分反应后过滤,得到蓝色溶液,则所得蓝色溶液中一定含有的溶质是
(4)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示。下列相关判断中,正确的是

A 甲是锌,乙是铁
B 甲是铁,乙是锌
C 图1中消耗硫酸的质量甲>乙
D 图2中金属乙与硫酸充分反应后,金属乙一定有剩余
更新时间:2020-01-20 11:14:33
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】铜是人类使用最早、应用广泛的金属.
(一)对古代铜制品认识
(1)下图为出土文物古代青铜铸件“雁鱼灯”。该文物能保存至今的原因可能是__________ (选填序号)。

a 铜的活泼性弱,不易生锈 b 深埋于地下,隔绝空气
(2)《吕氏春秋·别类篇》载有“金柔锡柔,合两柔则刚”(注:此处“金”指铜),表明我们的祖先已认识到铜合金的硬度比纯铜_____________ (填“大”或“小”)。
(3)镇江人葛洪《抱朴子内篇·黄白》中有“以曾青涂铁,铁赤色如铜高”的记载,其中蕴含化学含意的化学方程式为_______________ 。
(二)铜的化合物制备
辉铜矿主要成分为Cu2S、软锰矿主要成分为MnO2,均含有少量二氧化硅、氧化铁等杂质。工业上综合利用这两种矿物制备碱式碳酸铜的主要工艺流程如下:(已知:二氧化硅不溶于水,也不溶于酸)。
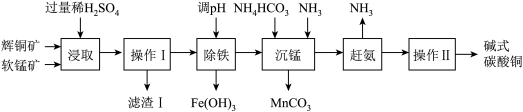
(1)“浸取”前将矿石粉碎成细颗粒的目的是____________ 。
(2)“浸取”时,氧化铁溶于稀硫酸的化学方程式为____________ 。除此之外,还会发生反应: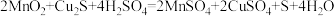 ,则“滤渣Ⅰ”中除了有S外,一定还有
,则“滤渣Ⅰ”中除了有S外,一定还有____________ (写化学式)。
(3)“沉锰”时温度不宜过高,其原因是____________ 。
(4)该流程中可循环利用的物质是____________ 。
(三)碱式碳酸铜的热分解实验
某碱式碳酸铜成分可表示为Cua(OH)b(CO3)c,兴趣小组为探究其性质和组成,用下图装置对34.6g样品进行热分解实验,观察到固体先变成黑色,然后出现红色固体。
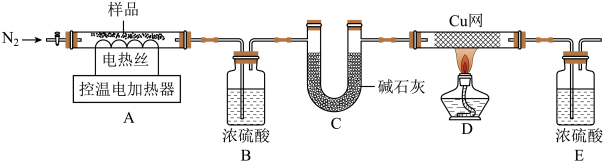
(1)装配好实验装置后,先要____________ ,再加入样品。
(2)E装置的作用是____________ 。
(3)停止加热后仍需继续通N2,可防止倒吸和____________ 。
(4)测得实验前后各装置的质量变化如下表。
①表格中x=____________ 。
②该碱式碳酸铜的化学式为____________ 。
③实验后装置A中固体的成分及质量为____________ 。
(一)对古代铜制品认识
(1)下图为出土文物古代青铜铸件“雁鱼灯”。该文物能保存至今的原因可能是

a 铜的活泼性弱,不易生锈 b 深埋于地下,隔绝空气
(2)《吕氏春秋·别类篇》载有“金柔锡柔,合两柔则刚”(注:此处“金”指铜),表明我们的祖先已认识到铜合金的硬度比纯铜
(3)镇江人葛洪《抱朴子内篇·黄白》中有“以曾青涂铁,铁赤色如铜高”的记载,其中蕴含化学含意的化学方程式为
(二)铜的化合物制备
辉铜矿主要成分为Cu2S、软锰矿主要成分为MnO2,均含有少量二氧化硅、氧化铁等杂质。工业上综合利用这两种矿物制备碱式碳酸铜的主要工艺流程如下:(已知:二氧化硅不溶于水,也不溶于酸)。

(1)“浸取”前将矿石粉碎成细颗粒的目的是
(2)“浸取”时,氧化铁溶于稀硫酸的化学方程式为
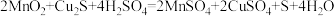 ,则“滤渣Ⅰ”中除了有S外,一定还有
,则“滤渣Ⅰ”中除了有S外,一定还有(3)“沉锰”时温度不宜过高,其原因是
(4)该流程中可循环利用的物质是
(三)碱式碳酸铜的热分解实验
某碱式碳酸铜成分可表示为Cua(OH)b(CO3)c,兴趣小组为探究其性质和组成,用下图装置对34.6g样品进行热分解实验,观察到固体先变成黑色,然后出现红色固体。

(1)装配好实验装置后,先要
(2)E装置的作用是
(3)停止加热后仍需继续通N2,可防止倒吸和
(4)测得实验前后各装置的质量变化如下表。
| 温度/℃ | 装置A | 装置B | 装置C | 装置D |
| 实验前/g | 234.6 | 200.0 | 200.0 | 100.0 |
| 实验后/g | 222.4 | 201.8 | 208.8 | x |
②该碱式碳酸铜的化学式为
③实验后装置A中固体的成分及质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】废旧干电池中含有锌皮,铜帽(含Cu、Zn),石墨、MnO2、NH4C1等物质,如果随意丢弃会造成水体污染和土壤污染,因此将废旧干电池进行回收利用尤为重要。已知: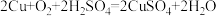 。请回答下列问题:
。请回答下列问题:
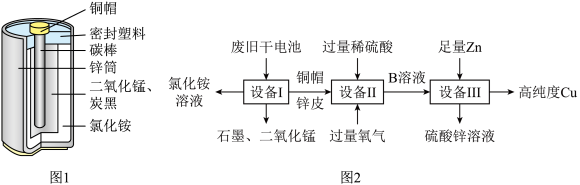
(1)图1中电池中使用铜帽和碳棒的主要是利用其______ 性。
(2)图2使回收废旧电池的工艺流程,图中设备I过滤得到的氯化铵溶液可以用来制作_____ 肥。
(3)加入过量氧气得作用是_______ ,B溶液的溶质有H2SO4、______ 和________ 。
(4)写出在设备Ⅲ中发生得两个化学反应方程式:_______ 、________ 。
(5)若要从硫酸锌溶液中得到硫酸锌晶体,主要包括蒸发浓缩、_______ 、过滤等操作。
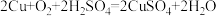 。请回答下列问题:
。请回答下列问题:
(1)图1中电池中使用铜帽和碳棒的主要是利用其
(2)图2使回收废旧电池的工艺流程,图中设备I过滤得到的氯化铵溶液可以用来制作
(3)加入过量氧气得作用是
(4)写出在设备Ⅲ中发生得两个化学反应方程式:
(5)若要从硫酸锌溶液中得到硫酸锌晶体,主要包括蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】人类的生产生活离不开金属材料,请用学过的知识回答下列问题
(1)“湿法炼铜”的原理是硫酸铜溶液与铁反应,其反应的化学方程式为_____ 。图1铜制品的用途中,利用金属导电性的是_____ (填字母)。
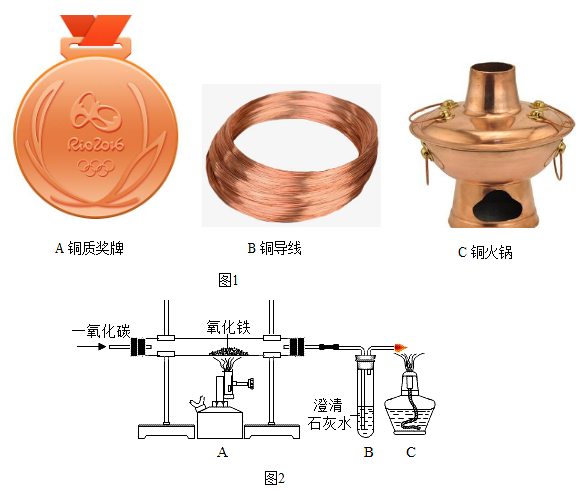
(2)工业上炼铁的原理是利用一氧化碳和氧化铁反应。某兴趣小组利用图2装置进行试验,请按要求填空:
①写出CO还原Fe2O3的化学方程式_____ ;实验过程中能观察到A装置中的现象为_____ ,右边导气管口放置点燃的酒精灯的目的是_____
②铁制品在一定条件下能生锈,疏松的铁锈不能阻碍里层的铁继续与_____ 反应生锈,因此铁制品可以进一步锈蚀。回收利用废旧金属制品的目的之一是_____ 。
(1)“湿法炼铜”的原理是硫酸铜溶液与铁反应,其反应的化学方程式为

(2)工业上炼铁的原理是利用一氧化碳和氧化铁反应。某兴趣小组利用图2装置进行试验,请按要求填空:
①写出CO还原Fe2O3的化学方程式
②铁制品在一定条件下能生锈,疏松的铁锈不能阻碍里层的铁继续与
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
名校
【推荐1】化学反应有的放出热量称为放热反应,有的吸收热量称为吸热反应。化学反应有快有慢,一般增大反应物浓度、接触面积、升高温度、使用催化剂均可加快反应速率
(1)下列过程是化学变化且是放热反应的是(填编号)_____
A 浓硫酸溶于水
B 生石灰加入水中
C NH4NO3 晶体溶于水
D 天然气燃烧
E 制水煤气
(2)实验室用锌粒与 10mL30%的稀 H2SO4反应制取 H2。
①下列措施不能加快反应速率的是(填编号)_______________________ 。
A 加热
B 将锌粒换成锌粉
C 将 30%的 H2SO4 换成 50%的 H2SO4
D 将 30%的 H2SO4,增加到 20mL
E加入适量 Na2SO4 固体
②反应速率v 随时间变化如图所示A→B 速率加快的原因是__________________________ ;B→C 速率减慢的原因是__________ 。

(3)实验室用 H2O2 制 O2,为加快反应速率常采取的措施是__________ ,反应方程式为_____ 。
(4)已知反应 Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,将一定量 Na2S2O3 溶液、稀 H2SO4 和H2O 同时混合,下列各组实验中最先出现浑浊的是(填编号)______________________ 。
(1)下列过程是化学变化且是放热反应的是(填编号)
A 浓硫酸溶于水
B 生石灰加入水中
C NH4NO3 晶体溶于水
D 天然气燃烧
E 制水煤气
(2)实验室用锌粒与 10mL30%的稀 H2SO4反应制取 H2。
①下列措施不能加快反应速率的是(填编号)
A 加热
B 将锌粒换成锌粉
C 将 30%的 H2SO4 换成 50%的 H2SO4
D 将 30%的 H2SO4,增加到 20mL
E加入适量 Na2SO4 固体
②反应速率v 随时间变化如图所示A→B 速率加快的原因是

(3)实验室用 H2O2 制 O2,为加快反应速率常采取的措施是
(4)已知反应 Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,将一定量 Na2S2O3 溶液、稀 H2SO4 和H2O 同时混合,下列各组实验中最先出现浑浊的是(填编号)
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O |
| A | 20 | 40% 20g | 40% 20g | 10g |
| B | 20 | 40% 25g | 40% 20g | 5g |
| C | 40 | 80% 10g | 40% 20g | 20g |
| D | 40 | 50% 10g | 60% 10g | 5g |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐2】小明同学取镁、铝、锌三种金属,分别放入盛有质量和质量分数都相等的稀盐酸的锥形瓶中,实验装置如图1,采集数据,得到如图2所示的气压变化曲线。
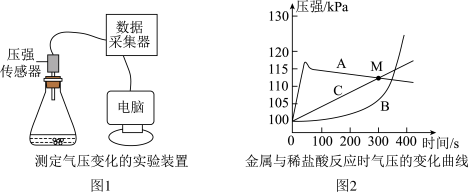
(1)镁、铝、锌与稀盐酸反应产生的相同气体是______ (填化学式)。
(2)铝对应的曲线是B,反应速率先慢后快,其主要原因是______ 。
(3)从图2分析,以下结论正确的是______ (填序号)。
①金属镁对应的气压变化曲线是A ②M点时参加反应的镁锌质量相等
③实验时取用的镁铝质量可能相等

(1)镁、铝、锌与稀盐酸反应产生的相同气体是
(2)铝对应的曲线是B,反应速率先慢后快,其主要原因是
(3)从图2分析,以下结论正确的是
①金属镁对应的气压变化曲线是A ②M点时参加反应的镁锌质量相等
③实验时取用的镁铝质量可能相等
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】碳是重要的生命元素,碳及其化合物的综合利用以及金属的使用使世界变得更加绚丽多彩。
(1)用化学用语填空
①3个碳原子______ ;
②3个一氧化碳分子______ ;
③3个碳酸根离子______ 。
(2)“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
①CO2的过度排放会造成______ 的加剧。
②工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。根据石灰水与二氧化碳反应的启发,写出NaOH溶液吸收CO2生成Na2CO3溶液的化学方程式______ 。
(3)将质量均为10克的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,完全反应后,生成氢气的质量关系可能是______。
(1)用化学用语填空
①3个碳原子
②3个一氧化碳分子
③3个碳酸根离子
(2)“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决全球气候问题的大国担当。
①CO2的过度排放会造成
②工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。根据石灰水与二氧化碳反应的启发,写出NaOH溶液吸收CO2生成Na2CO3溶液的化学方程式
(3)将质量均为10克的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,完全反应后,生成氢气的质量关系可能是______。
A.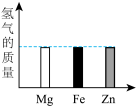 | B.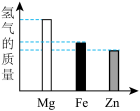 |
C.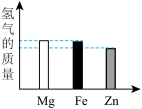 | D.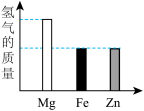 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】结合下列有关铁的实验,回答有关问题:
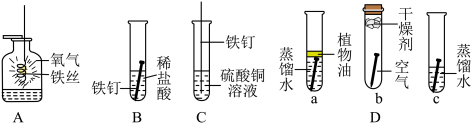
(1)图A是细铁丝在氧气中燃烧的实验,反应后生成___________ 色固体;
(2)图B所示实验中,发生反应的化学方程式为___________ ;
(3)图C所示实验,判断出Fe比Cu的活动性强,所依据最明显的实验现象是___________ ;
(4)图D是一组探究铁生锈条件的对比实验,其中b与c作对比的目的是___________ 。

(1)图A是细铁丝在氧气中燃烧的实验,反应后生成
(2)图B所示实验中,发生反应的化学方程式为
(3)图C所示实验,判断出Fe比Cu的活动性强,所依据最明显的实验现象是
(4)图D是一组探究铁生锈条件的对比实验,其中b与c作对比的目的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐2】在金属活动性顺序表里,金属的位置越靠前,它的活动性就越强,在化学反应中越容易失去电子。
(1)Ca、Mg、K三种金属在化学反应中失去电子的能力由强到弱的顺序是_____________ 。
(2) Ca、Mg、K三种金属的原子结构示意图如右图所示,
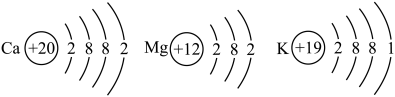
请根据这三种金属的原子结构示意图,结合已学过的有关原子结构的知识推测:金属单质失去电子能力的强弱主要与哪些因素有关?_____________ (任答两点)。
(3)能证明Cu的金属活动性比Ag强的方法是:___________ (用化学方程式表示)。
(4)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来。例如,在溶液中可发生以下反应: Cl2 +2NaBr =2NaCl+Br2; Br2 +2KI =2KBr +I2↓;I2 +Na2S =2NaI+S 由此可以判断硫(S)、溴( Br2)、碘(I2)、氯气(Cl2)四种非金属单质的活动性由弱到强的顺序的是_____________ 。
(1)Ca、Mg、K三种金属在化学反应中失去电子的能力由强到弱的顺序是
(2) Ca、Mg、K三种金属的原子结构示意图如右图所示,

请根据这三种金属的原子结构示意图,结合已学过的有关原子结构的知识推测:金属单质失去电子能力的强弱主要与哪些因素有关?
(3)能证明Cu的金属活动性比Ag强的方法是:
(4)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来。例如,在溶液中可发生以下反应: Cl2 +2NaBr =2NaCl+Br2; Br2 +2KI =2KBr +I2↓;I2 +Na2S =2NaI+S 由此可以判断硫(S)、溴( Br2)、碘(I2)、氯气(Cl2)四种非金属单质的活动性由弱到强的顺序的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】金属材料广泛应用于生产生活中。2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)建造航母用到了钛合金,构成金属钛的粒子是____________ (填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO4 4HF+2X+TiO2,X的化学式为
4HF+2X+TiO2,X的化学式为____________ 。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与______________ 接触而锈蚀,而金属铝在空气中更耐腐蚀的原因是______________________________ (用化学方程式表示)
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_________________ (填序号)。
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
(4)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是_____________________________ (写化学式)。
(1)建造航母用到了钛合金,构成金属钛的粒子是
 4HF+2X+TiO2,X的化学式为
4HF+2X+TiO2,X的化学式为(2)航母外壳用涂料覆盖,是为了防止钢铁材料与
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
(4)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是
您最近一年使用:0次



