现有一包白色固体可能含有CaO、CuSO4、 K2SO4、BaCl2、 K2CO3中的一种或几种。为确定其成分,进行如下实验:
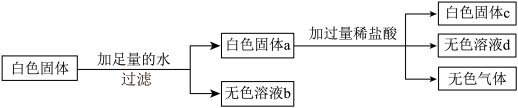
(1)上述实验过程中,产生的无色气体是__________________ ;
(2)原白色固体中可能有CaO,检验是否有CaO的操作是:取少量无色溶液b,______________ ;经检验原白色固体中确实不含有CaO;
(3)无色溶液b中溶质有______________ 种可能;
(4)下列设想合理的是______________ ;
A 用白色固体a除去氯化钡中少量的盐酸
B 用无色溶液d鉴别氢氧化钠溶液和碳酸钠溶液
C 在无色溶液b中,加适量的氯化钡溶液可制得纯净的氯化钾

(1)上述实验过程中,产生的无色气体是
(2)原白色固体中可能有CaO,检验是否有CaO的操作是:取少量无色溶液b,
(3)无色溶液b中溶质有
(4)下列设想合理的是
A 用白色固体a除去氯化钡中少量的盐酸
B 用无色溶液d鉴别氢氧化钠溶液和碳酸钠溶液
C 在无色溶液b中,加适量的氯化钡溶液可制得纯净的氯化钾
更新时间:2020-02-21 09:10:54
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
【推荐1】如图是模拟海水制盐的流程

(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若_____________ (填实验现象),则证明Ca(OH)2溶液已过量。
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的___________ .
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有___________ 和___________ .
【验证猜想】
【实验结论】经过兴趣小组的实验分析,推出猜想三是正确的.
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:___________________________________________ .

(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 滤液中还含有 | |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入 | 滤液中还含有氢氧化钠 |
【实验结论】经过兴趣小组的实验分析,推出猜想三是正确的.
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】2020年是北京故宫建成600周年。红墙黄瓦是故宫的标志,涂制故宫的红墙使用的是铁红颜料,其主要成分为Fe2O3。工业上以硫酸亚铁为原料生产铁红颜料和副产品K2SO4固体的主要工艺流程如下。
已知:①反应Ⅰ的化学方程式为 ;
;
②NH4HCO3的分解温度为35℃。

(1)反应Ⅰ需控制反应温度在35℃以下的目的是_________ 。
(2)反应Ⅲ中高温煅烧FeCO3的化学方程式为_________ 。
(3)反应Ⅳ中涉及到的物质在20℃时的溶解度如下表所示:
反应Ⅳ中发生反应的化学方程式为_________ 。
(4)滤液Ⅱ中的阴离子除含有 之外还含有
之外还含有_________ (填离子符号)。
已知:①反应Ⅰ的化学方程式为
 ;
;②NH4HCO3的分解温度为35℃。

(1)反应Ⅰ需控制反应温度在35℃以下的目的是
(2)反应Ⅲ中高温煅烧FeCO3的化学方程式为
(3)反应Ⅳ中涉及到的物质在20℃时的溶解度如下表所示:
| 物质 | (NH4)2SO4 | NH4Cl | K2SO4 | KCl |
| 溶解度/g | 75.4 | 37.2 | 11.1 | 34.2 |
(4)滤液Ⅱ中的阴离子除含有
 之外还含有
之外还含有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】为了确定一包粉末(可能含有Mg、Cu、CuO中的一种或几种)和一瓶溶液(Na2CO3、NaOH、Na2SO4中的一种或几种)的成分,做了如下实验:

(1)实验中生成气体的化学方程式为___________ ;
(2)分析固体a的所有可能的情况___________ ;
(3)向固体c中加入过量的稀盐酸,当观察到__________ 现象,则证明无色溶液A中一定含有Na2CO3和Na2SO4;
(4)为了确定溶液A可能含有的溶质,下列实验一定可行的是:____________ 。
A取少量溶液A,加酚酞溶液
B取少量溶液C,通入CO2气体
C取少量溶液D,加MgCl2溶液
D取少量固体d,加入过量的稀盐酸

(1)实验中生成气体的化学方程式为
(2)分析固体a的所有可能的情况
(3)向固体c中加入过量的稀盐酸,当观察到
(4)为了确定溶液A可能含有的溶质,下列实验一定可行的是:
A取少量溶液A,加酚酞溶液
B取少量溶液C,通入CO2气体
C取少量溶液D,加MgCl2溶液
D取少量固体d,加入过量的稀盐酸
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】金属材料在生活与科技发展中起着重要的作用。结合以下材料回答:
金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,镀金钼丝纤维常用在航天通信方面,只有头发丝四分之一细,其性能稳定。
我国的钼矿储量非常丰富,下图是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):(提示:无水硫酸铜遇水变蓝色)

(1)钼能制成细丝,是利用了钼的__________ 性。表面镀金,原因之一是利用了金的化学性质__________ 。
(2)完成图1过程①中反应的化学方程式:2MoS2+7O2 2MoO3+4
2MoO3+4__________ 。其中产物MoO3中钼元素的化合价为_______ 。
A -3 B +3 C +4 D +6
(3)步骤②和③反应完成后都要进行的操作是__________ ;用到的玻璃仪器除了玻璃棒、烧杯还有__________ 。
(4)步骤⑥吸收尾气生成铵盐和水的化学方程式为__________ ,检验该铵盐中阴离子所需要的试剂为__________ 。
(5)若选用下图装置按序连接完成步骤⑤的反应,同时检验该反应产生的氧化物。

①装置C中所盛的试剂是__________ (填试剂名称);证明装置B中已经发生反应的现象是__________ 。
②实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,_______ →______ →______ →________ 。(请按正确的先后顺序填入下列步骤的代号)
a收集气体并检验其纯度 b停止加热,充分冷却
c加热反应一段时间 d关闭分液漏斗活塞,停止通氢气
金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,镀金钼丝纤维常用在航天通信方面,只有头发丝四分之一细,其性能稳定。
我国的钼矿储量非常丰富,下图是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):(提示:无水硫酸铜遇水变蓝色)

(1)钼能制成细丝,是利用了钼的
(2)完成图1过程①中反应的化学方程式:2MoS2+7O2
 2MoO3+4
2MoO3+4A -3 B +3 C +4 D +6
(3)步骤②和③反应完成后都要进行的操作是
(4)步骤⑥吸收尾气生成铵盐和水的化学方程式为
(5)若选用下图装置按序连接完成步骤⑤的反应,同时检验该反应产生的氧化物。

①装置C中所盛的试剂是
②实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,
a收集气体并检验其纯度 b停止加热,充分冷却
c加热反应一段时间 d关闭分液漏斗活塞,停止通氢气
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】有一包固体混合物粉末,可能含有CaCO3,NaCl、NH4Cl、BaSO4、CuO中的两种或几种。研究小组为探究其成分,现按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。

(1)气体A为_______ (填化学式,下同),蓝色沉淀D为_____ 气体F的气味是_____ 。生成沉淀C的化学方程式_______
(2)请写出步骤③中发生的任意一个反应的化学方程式:_______ 。
(3)原固体混合物中肯定不存在的物质是_______ (填化学式),你的理由是_______ 。
(4)原固体混合物中可能存在的物质是_______ (填化学式),一定存在的物质有_______ 种。
(5)溶液E中一定存在的金属离子是_______ (填离子符号)。

(1)气体A为
(2)请写出步骤③中发生的任意一个反应的化学方程式:
(3)原固体混合物中肯定不存在的物质是
(4)原固体混合物中可能存在的物质是
(5)溶液E中一定存在的金属离子是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐3】某固体粉末中可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种,某科学兴趣小组为探究其成分,设计了如下实验流程。请分析并回答下列问题(①所加试剂均足量②硫酸钡在灼烧条件下不分解):

(1)操作Ⅰ的名称是_________ 。
(2)固体乙的成分是_________ (填化学式,下同)。
(3)该固体粉末中一定含有的物质是_________ 。
(4)上述流程中,固体甲中参加反应的物质的质量为_________ 。

(1)操作Ⅰ的名称是
(2)固体乙的成分是
(3)该固体粉末中一定含有的物质是
(4)上述流程中,固体甲中参加反应的物质的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐1】一包不纯的氯化钾粉末,杂质可能是硫酸钠、氢氧化钠、氯化钠、硝酸钡中的一种或几种。为确定其成分,某兴趣小组的同学进行如下实验:
实验一:取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得到无色澄清溶液,往溶液中通入CO2,产生白色沉淀。
实验二:取14.0g该粉末于烧杯中,加入蒸馏水完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后,产生28.7g白色沉淀。
根据以上信息,回答下列问题:
(1)杂质中一定没有___________ ,一定有__________ 。
(2)实验一中产生白色沉淀的化学方程式为_____________ 。
实验一:取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得到无色澄清溶液,往溶液中通入CO2,产生白色沉淀。
实验二:取14.0g该粉末于烧杯中,加入蒸馏水完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后,产生28.7g白色沉淀。
根据以上信息,回答下列问题:
(1)杂质中一定没有
(2)实验一中产生白色沉淀的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】某混合溶液可能含Na2SO4、Na2CO3、NaOH中的一种或几种溶质,为验证其组成,实验如下:

(1)混合溶液的溶质中一定有_________________ 、________________ 。
(2)按该加入试剂的顺序,不能验证的物质是_________________ ,写出验证过程中②所发生的反应方程式_______________________________ ;
(3)改变上述三步骤中所用三种试剂的滴加顺序,可以验证是否有这种物质,则这三种试剂滴加的顺序依次为__________________ (填写序号)
(4)步骤①中加入的盐酸为什么要“过量”____________ ;

(1)混合溶液的溶质中一定有
(2)按该加入试剂的顺序,不能验证的物质是
(3)改变上述三步骤中所用三种试剂的滴加顺序,可以验证是否有这种物质,则这三种试剂滴加的顺序依次为
(4)步骤①中加入的盐酸为什么要“过量”
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】某化学兴趣小组做了如图1所示的三个实验:(提示:BaC12溶液呈中性)

(1)小组同学向试管I中慢慢滴入MgC12溶液,并不断振荡,直至观察到______ 现象时,证明二者恰好完全反应,试管I中发生的反应的化学方程式______ ;继续完成试管Ⅱ和Ⅲ中的两个实验。
(2)同学们继续实验,设计了图2的实验方案进行探究。

解释溶液B呈红色的原因______ ,滤液C的溶质是______ (填化学式)。小组同学对沉淀N的成分进行分析,认为沉淀成分有两种可能:
猜想一:碳酸钡
猜想二:______ 。
请设计实验方案证明猜想二成立:______ 。

(1)小组同学向试管I中慢慢滴入MgC12溶液,并不断振荡,直至观察到
(2)同学们继续实验,设计了图2的实验方案进行探究。

解释溶液B呈红色的原因
猜想一:碳酸钡
猜想二:
请设计实验方案证明猜想二成立:
您最近一年使用:0次



