海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港海水资源丰富。
(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是溶解→过滤→蒸发→计算产率等。
①过滤操作中玻璃棒的末端要轻轻的斜靠在______ 一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作______ ;
②下列操作可能导致精盐产率偏高的是______ (填字母)。
a 食盐没有完全溶解即过滤
b 过滤时液面高于滤纸边缘
c 器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。下图是从海水中获得氯化镁溶液的流程。

①在海水中加入石灰乳后,发生反应的化学方程式是______ ;
②上述过程中试剂A与沉淀B发生的是中和反应,则试剂A是(填名称)______ 。
(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是溶解→过滤→蒸发→计算产率等。
①过滤操作中玻璃棒的末端要轻轻的斜靠在
②下列操作可能导致精盐产率偏高的是
a 食盐没有完全溶解即过滤
b 过滤时液面高于滤纸边缘
c 器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。下图是从海水中获得氯化镁溶液的流程。

①在海水中加入石灰乳后,发生反应的化学方程式是
②上述过程中试剂A与沉淀B发生的是中和反应,则试剂A是(填名称)
更新时间:2020-02-24 23:06:13
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】复分解反应存在这样一个规律:较强酸可制取较弱酸。中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应。盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解。
已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH:
(1)请根据上述信息判断下列反应不能发生的是_____ (填编号)。
A
B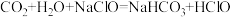
C
D
E
F
(2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KC1和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为_____ 。
(3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是_____ (填编号)。
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO⑤H2SO4
(4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且 ,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是
,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____ 。
已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)请根据上述信息判断下列反应不能发生的是
A

B
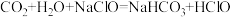
C

D

E

F

(2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KC1和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为
(3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO⑤H2SO4
(4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且
 ,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是
,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】如图是探究盐酸和氢氧化钠反应过程中溶液的pH变化规律。

(1)该反应的化学方程式是_______ ,反应的实质是______ 。
(2)B处溶液中存在的离子是______ 。(填离子符号)
(3)C处溶液显_______ 性。

(1)该反应的化学方程式是
(2)B处溶液中存在的离子是
(3)C处溶液显
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】归纳总结是学习化学的一种方法。请结合小明同学对碱的四点化学性质的归纳图完成下列问题。(箭头上方的物质是指与碱反应的物质)
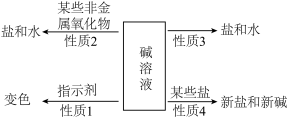
(1)碱溶液能使无色酚酞溶液变____________
(2)根据性质 2可知,NaOH 如果密封不好,久置后会变质,检验 NaOH 是否变质的一种盐溶液是__________
(3)性质 3 的化学反应从离子角度分析,实质是____________ 生成水分子
(4)工业上制备氢氧化钠可以利用性质 4 的反应,写出相关化学方程式____________

(1)碱溶液能使无色酚酞溶液变
(2)根据性质 2可知,NaOH 如果密封不好,久置后会变质,检验 NaOH 是否变质的一种盐溶液是
(3)性质 3 的化学反应从离子角度分析,实质是
(4)工业上制备氢氧化钠可以利用性质 4 的反应,写出相关化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】从海水得到的粗盐往往含有可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活.实验室模拟工业粗盐提纯的流程如图,请回答:

(1)步骤①和②的目的是________ ,步骤③的主要目的是________ .
(2)操作X的名称是________ ,该操作中用到的玻璃仪器有烧杯、玻璃棒和________ .向溶液C中加入适量盐酸,控制盐酸用量的操作方法是________ .
(3)本实验从滤液C得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度数据分析原因________ .
(4)下表提供了两种物质的溶解度数据,读取信息后回答:

看图判断,氯化钠的溶解度曲线是上图________ (填数字编号),40℃时,将60g硝酸钾溶于100g水中,降温至10℃时可析出硝酸钾晶体________ g.

(1)步骤①和②的目的是
(2)操作X的名称是
(3)本实验从滤液C得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度数据分析原因
(4)下表提供了两种物质的溶解度数据,读取信息后回答:
| 温度℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |

看图判断,氯化钠的溶解度曲线是上图
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】潍坊海水资源丰富,从海水得到的粗盐往往含有可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。实验室模拟工业粗盐提纯的流程如图,请回答:

(1)操作X的名称是_____ ,该操作中用到的玻璃仪器有烧杯、玻璃棒和______ 。
(2)加适量盐酸的目的是____________________________________________ 。
(3)生成沉淀D的化学方程式为_____________________________ 。
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。

①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数___ (填“>”“<”或“=”)碳酸钠溶液的溶质质量分数。
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是_____ 。

(1)操作X的名称是
(2)加适量盐酸的目的是
(3)生成沉淀D的化学方程式为
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。

①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
【推荐3】请回答下列问题。
(1)实验室除去粗盐中泥沙等难溶性杂质的实验步骤如下

①操作I的名称是________ 。
②在蒸发过程中,当蒸发皿中出现____ 时,停止加热。利用蒸发皿的余热使滤液蒸干。
(2)工业上制备粗盐时,通过晒盐或煮盐的方法,可以蒸发盐溶液中水分使之浓缩结晶,理由是_____________ 。
(3)由于粗盐中含有少量CaCl2等杂质,不能满足化工生产的要求。因此必须将粗盐进行精制。若要除去粗盐中的CaCl2,所用的试剂为________ 。
(1)实验室除去粗盐中泥沙等难溶性杂质的实验步骤如下

①操作I的名称是
②在蒸发过程中,当蒸发皿中出现
(2)工业上制备粗盐时,通过晒盐或煮盐的方法,可以蒸发盐溶液中水分使之浓缩结晶,理由是
(3)由于粗盐中含有少量CaCl2等杂质,不能满足化工生产的要求。因此必须将粗盐进行精制。若要除去粗盐中的CaCl2,所用的试剂为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】海水是宝贵的资源,海水晒盐产生的粗盐中含有杂质MgCl2、CaCl2、Na2SO4经提纯后得到精盐,母液可以提纯金属镁,以下是海水综合利用的流程图:

(1)粗盐提纯过程中NaOH溶液、BaCl2溶液、Na2CO3溶液的加入顺序还可以是______。
(2)已知NaCl和MgCl2的溶解度受温度的影响较小,则操作I的名称为______ ,该操作过程中需要用到玻璃棒,其作用是______ 。
(3)粗盐提纯过程中加入过量Na2CO3的目的是______ 。
(4)试剂X的名称为______ ,其与Mg(OH)2反应的化学方程式为______ ,该反应的基本反应类型为______ 。
(5)电解熔融MgCl2可得到金属镁和另一种单质,该反应的化学方程式为______ 。

(1)粗盐提纯过程中NaOH溶液、BaCl2溶液、Na2CO3溶液的加入顺序还可以是______。
| A.BaCl2溶液、NaOH溶液、Na2CO3溶液 |
| B.Na2CO3溶液、BaCl2溶液、NaOH溶液 |
| C.BaCl2溶液、Na2CO3溶液、NaOH溶液 |
(3)粗盐提纯过程中加入过量Na2CO3的目的是
(4)试剂X的名称为
(5)电解熔融MgCl2可得到金属镁和另一种单质,该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】我市莱州湾盐场盛产食盐。请回答下列问题。
(1)如图1,请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。

①操作Ⅰ所用的玻璃仪器有:_____ 。
②在蒸发过程中,待_____ 时,停止加热。该过程中玻璃棒的作用是_____ 。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如图2。
①加入稍过量的Na2CO3溶液除了能除去粗盐中_____ 的外,它还有一个作用是_____ (用化学方程式表示)。
②操作Ⅳ加入一定量盐酸的作用是除去_____ (写离子符号)。
③假设除杂过程中氯化钠没有损失,则理论上除杂后获得食盐的质量_____ 除杂前食盐的质量(填“>““<“或“=”),其理由是_____ 。
(3)食盐是人体进行正常新陈代谢的必需品,在生活中可以做_____ (写一点即可)。
(1)如图1,请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。

①操作Ⅰ所用的玻璃仪器有:
②在蒸发过程中,待
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如图2。
①加入稍过量的Na2CO3溶液除了能除去粗盐中
②操作Ⅳ加入一定量盐酸的作用是除去
③假设除杂过程中氯化钠没有损失,则理论上除杂后获得食盐的质量
(3)食盐是人体进行正常新陈代谢的必需品,在生活中可以做
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐3】氯化钡是一种可溶性重金属盐。工业上用毒重石(主要成分是BaCO3)制备氯化钡晶体。某实验小组模拟工业上制备氯化钡晶体的流程,设计了实验室中制备氯化钡晶体的方案,实验流程如图所示。(该毒重石样品所含杂质难溶于水,不与酸反应。)

(1)步骤①中发生反应的化学方程式为_____ 。
(2)滤液Ⅱ是30℃时氯化钡的_____ 溶液(选填“饱和”或“不饱和”);洗涤氯化钡晶体最适宜的洗涤剂是_____ (填字母序号)。
A 30℃水 B 30℃饱和氯化钠溶液 C 30℃饱和氯化钡溶液
(3)关于上述实验方案的相关内容,下列说法不正确的是_____ (填字母序号)。
A 氯化钡是一种有毒的物质,使用时应注意安全
B 该实验流程中得到的副产品二氧化碳是重要的化工原料
C 可用重晶石(主要成分是硫酸钡)代替该实验流程中的毒重石,制备氯化钡晶体
D 步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+对环境的污染
(4)某同学提出,步骤③将滤液Ⅰ浓缩时会产生气体污染物,其化学式为_____ 。为防止污染,需要对滤液Ⅰ处理后再浓缩。处理滤液Ⅰ用到稍过量甲试剂,该试剂是_____ (填字母序号)。
A Ba(OH)2 B BaCl2 C Ba(NO3)2 D BaCO3
(5)实验室有一份混有碳酸钙杂质的碳酸钡样品。分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):

①高温灼烧碳酸钡和碳酸钙的混合物,直至完全分解。碳酸钡和碳酸钙化学性质相似,写出碳酸钡高温分解的化学方程式_____ 。
②将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液。为减少Ba(OH)2的损失并除去不溶物应进行的操作是_____ (选填字母);
A 冷却过滤 B 趁热过滤
③将“②”中滤液冷却结晶并过滤,得到的Ba(OH)2固体中不会含Ca(OH)2,因为_____ 。
④将“③”中制得的固体溶于水制成溶液。并向制得的溶液中滴加酚酞试剂,再通入二氧化碳。当观察到_____ 时,Ba(OH)2恰好全部生成BaCO3沉淀,即可停止通二氧化碳。
⑤滤出碳酸钡沉淀,经_____ (填一种操作)、干燥后即得到纯净的碳酸钡。

(1)步骤①中发生反应的化学方程式为
(2)滤液Ⅱ是30℃时氯化钡的
A 30℃水 B 30℃饱和氯化钠溶液 C 30℃饱和氯化钡溶液
(3)关于上述实验方案的相关内容,下列说法不正确的是
A 氯化钡是一种有毒的物质,使用时应注意安全
B 该实验流程中得到的副产品二氧化碳是重要的化工原料
C 可用重晶石(主要成分是硫酸钡)代替该实验流程中的毒重石,制备氯化钡晶体
D 步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+对环境的污染
(4)某同学提出,步骤③将滤液Ⅰ浓缩时会产生气体污染物,其化学式为
A Ba(OH)2 B BaCl2 C Ba(NO3)2 D BaCO3
(5)实验室有一份混有碳酸钙杂质的碳酸钡样品。分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):

①高温灼烧碳酸钡和碳酸钙的混合物,直至完全分解。碳酸钡和碳酸钙化学性质相似,写出碳酸钡高温分解的化学方程式
②将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液。为减少Ba(OH)2的损失并除去不溶物应进行的操作是
A 冷却过滤 B 趁热过滤
③将“②”中滤液冷却结晶并过滤,得到的Ba(OH)2固体中不会含Ca(OH)2,因为
④将“③”中制得的固体溶于水制成溶液。并向制得的溶液中滴加酚酞试剂,再通入二氧化碳。当观察到
⑤滤出碳酸钡沉淀,经
您最近一年使用:0次



