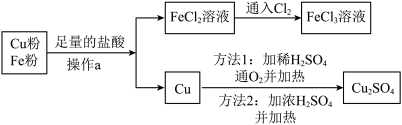
粗盐的主要成分是NaCl,下面是除去粗盐中MgCl2、Na2SO4、CaCl2等杂质的流程图(提示:微溶物不形成沉淀)
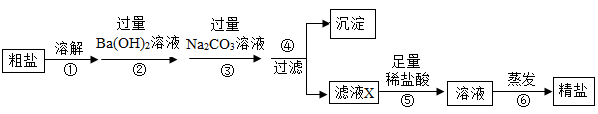
(1)写出操作②中发生的化学反应方程式(写出一个即可)
_______________ 。
(2)写出加入过量Na2CO3溶液的目的。
_______________ 。
(3)滤波X中含有几种溶质?
_______________ 。

(1)写出操作②中发生的化学反应方程式(写出一个即可)
(2)写出加入过量Na2CO3溶液的目的。
(3)滤波X中含有几种溶质?
更新时间:2020-02-27 14:51:59
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】在宏观、微观和符号之间建立联系,是化学学科独特的思维方式。
我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式的书写一般按以下步骤:(以K2SO4与Ba(NO3)2反应为例)

①写出K2SO4与Ba(NO3)2反应的化学方程式(在下面填写):
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成: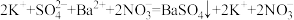
③删去方程式两边不参加反应的离子: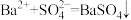
④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:
(1)K2SO4与Ba(NO3)2反应的化学方程式:______ 。
(2)下列各组离子在指定的溶液中,能大量共存的是______。
(3)写出稀盐酸滴在难溶固体碳酸钡上所发生反应的离子方程式______ 。
(4)写出一个与离子方程式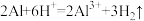 相对应的化学方程式
相对应的化学方程式______ 。
(5)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或______ 生成,反应就能发生。
我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式的书写一般按以下步骤:(以K2SO4与Ba(NO3)2反应为例)

①写出K2SO4与Ba(NO3)2反应的化学方程式(在下面填写):
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:
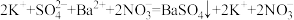
③删去方程式两边不参加反应的离子:
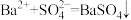
④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:
(1)K2SO4与Ba(NO3)2反应的化学方程式:
(2)下列各组离子在指定的溶液中,能大量共存的是______。
A.无色溶液中:K+、Na+、 、Fe2+ 、Fe2+ |
B.酸性溶液中:Mg2+、Na+、 、Cl- 、Cl- |
C.pH=11的溶液中:、Ba2+、Al3+、 、Cl- 、Cl- |
D.能使紫色石蕊溶液变蓝的溶液中:Na+、Ba2+、 、Cl- 、Cl- |
(4)写出一个与离子方程式
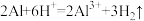 相对应的化学方程式
相对应的化学方程式(5)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】归纳总结是学习化学的重要方法,小明同学用图1总结了碱的四条化学性质。

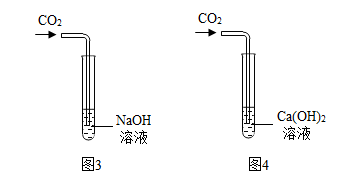
(1)为了验证图1中的反应①,将紫色石蕊试液滴入NaOH溶液和Ca(OH)2溶液中,观察到溶液都变______ 色。
(2)用微观示意图(图2)来说明反应②的发生,反应后“〇”表示的微粒符号为______ 。
(3)为了验证反应③能够发生,你不可能选择的是______。
为了验证图1中的反应④,小明同学进行了系列实验:
(4)向Ca(OH)2溶液和NaOH溶液中分别吹气(如图3、4),从图4中的实验现象可以得出的结论______ (用化学方程式表示)。但图3实验无明显现象。
(5)探究氢氧化钠溶液是否和CO2发生了反应:小明向盛有CO2软塑料瓶中倒入NaOH溶液(如图5)观察到塑料瓶变瘪,得出氢氧化钠与CO2反应的结论。但同组同学小李质疑该实验并不能证明氢氧化钠与CO2发生了反应,你认为他的理由是______ ;小明再向瓶内加______ (试剂名称),观察到______ 现象,从而确定氢氧化钠与CO2发生了反应。



(1)为了验证图1中的反应①,将紫色石蕊试液滴入NaOH溶液和Ca(OH)2溶液中,观察到溶液都变
(2)用微观示意图(图2)来说明反应②的发生,反应后“〇”表示的微粒符号为
(3)为了验证反应③能够发生,你不可能选择的是______。
A. | B. |
C. | D. |
为了验证图1中的反应④,小明同学进行了系列实验:
(4)向Ca(OH)2溶液和NaOH溶液中分别吹气(如图3、4),从图4中的实验现象可以得出的结论
(5)探究氢氧化钠溶液是否和CO2发生了反应:小明向盛有CO2软塑料瓶中倒入NaOH溶液(如图5)观察到塑料瓶变瘪,得出氢氧化钠与CO2反应的结论。但同组同学小李质疑该实验并不能证明氢氧化钠与CO2发生了反应,你认为他的理由是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空:
(1)为了更好掌握物质的性质规律,对物质的分类是经常用到的学习方法,不同物质有不同的分类标准。纯净物可按组成元素异同分为两类;单质可以按照性质的差异分为两类。现有下列四种单质,按性质的差异可以将A与_______ 分为一类,分类标准是_______________ 。
(2)La(镧)是一种活动性比锌强的金属,其氧化物为La2O3,氯化镧、硝酸镧都易溶于水,而对应的碱难溶于水,写出氧化镧与稀盐酸反应生成的盐的化学式____________ 。 根据复分解反应特点,下列各组物质间在水中能发生反应的是_______________ 。
A. 氢氧化镧与氯化镁 B.氯化镧与氢氧化钠 C. 氯化钙与硝酸镧
(1)为了更好掌握物质的性质规律,对物质的分类是经常用到的学习方法,不同物质有不同的分类标准。纯净物可按组成元素异同分为两类;单质可以按照性质的差异分为两类。现有下列四种单质,按性质的差异可以将A与
 银白色的镁条 |  切割玻璃的金刚石 |  还原出的金属铜 |  用于磁悬浮的氮气 |
| A | B | C | D |
A. 氢氧化镧与氯化镁 B.氯化镧与氢氧化钠 C. 氯化钙与硝酸镧
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E 是初中化学常见的物质,它们的转化关系如图所示(“→”表示物质间转化关系,部分反应物、生成物及反应条件已略去)。其中 A是最常用的溶剂,B的固体俗称干冰且 B、E组成元素相同,C是单质,B→C叫做光合作用,D属于化合物。
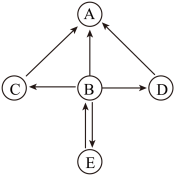
(1)B的化学式为是______ 。
(2)E的一种用途为______ 。
(3)写出B→A的化学方程式______ 。
(4)D→A的基本反应类型可能是______ (填一种即可)。

(1)B的化学式为是
(2)E的一种用途为
(3)写出B→A的化学方程式
(4)D→A的基本反应类型可能是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】纯净的过氧化钙(CaO2)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。其制备方法如下:以氢氧化钙和氯化铵为原料,制取CaO2·8H2O(搅拌时发生的化学反应方程式为:CaCl2+H2O2+2NH3·H2O+6H2O=CaO2·8H2O↓+2NH4Cl),再经脱水制得CaO2。
其流程如下:
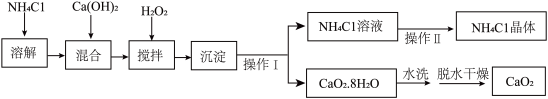
(1)操作Ⅰ的名称是__________ ,该操作中需要用到玻璃棒,其作用是_____________ 。
(2)“沉淀”时需控制温度在0~2℃,比较简单易行的方法是将反应容器放置在________ 中,制备CaO2·8H2O时反应温度不宜过高,原因一是防止因温度过高导致氨水挥发,原因二是防止__________________________________ 。(用化学方程式表示)
(3)为检验“水洗”是否合格,可取最后一次洗涤液少量于试管中,再滴加_________ (填试剂),若无白色沉淀产生说明“水洗”合格。
(4)该流程中除水外可循环利用的物质是____________ (填化学式)。
其流程如下:

(1)操作Ⅰ的名称是
(2)“沉淀”时需控制温度在0~2℃,比较简单易行的方法是将反应容器放置在
(3)为检验“水洗”是否合格,可取最后一次洗涤液少量于试管中,再滴加
(4)该流程中除水外可循环利用的物质是
您最近一年使用:0次
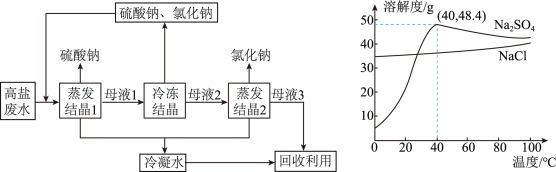
【推荐1】为研究溶解度曲线的应用,学习小组查得资料:某钢铁厂处理高盐废水(含氯化钠、硫酸钠及微量的其他盐)的流程、相关物质的溶解度曲线如图所示。请和小组同学一起研究。______ 。
(2)当温度高于______  时,硫酸钠的溶解度随温度升高而降低。
时,硫酸钠的溶解度随温度升高而降低。
(3) 时,将
时,将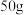 硫酸钠固体加入
硫酸钠固体加入 水中,充分搅拌后所得溶液的溶质质量分数为
水中,充分搅拌后所得溶液的溶质质量分数为______ (列出计算式即可)。
(4)降温至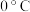 的“冷冻结晶”过程,析出的两种物质中较多的是
的“冷冻结晶”过程,析出的两种物质中较多的是______ (写名称)。
(5)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是______ 。
(6)粗盐中含有泥沙及少量可溶性 等杂质,为获得精盐进行如图实验。下列叙述正确的是______。
等杂质,为获得精盐进行如图实验。下列叙述正确的是______。
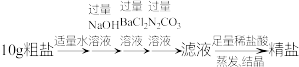
(2)当温度高于
 时,硫酸钠的溶解度随温度升高而降低。
时,硫酸钠的溶解度随温度升高而降低。(3)
 时,将
时,将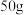 硫酸钠固体加入
硫酸钠固体加入 水中,充分搅拌后所得溶液的溶质质量分数为
水中,充分搅拌后所得溶液的溶质质量分数为(4)降温至
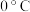 的“冷冻结晶”过程,析出的两种物质中较多的是
的“冷冻结晶”过程,析出的两种物质中较多的是(5)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是
(6)粗盐中含有泥沙及少量可溶性
 等杂质,为获得精盐进行如图实验。下列叙述正确的是______。
等杂质,为获得精盐进行如图实验。下列叙述正确的是______。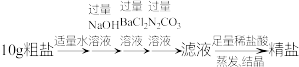
A.根据 的溶解度,可计算出溶解 的溶解度,可计算出溶解 粗盐所需水的最少质量 粗盐所需水的最少质量 |
B.只调换“过量的 溶液”与“过量的 溶液”与“过量的 溶液”的顺序,也能达到实验目的 溶液”的顺序,也能达到实验目的 |
C.加入过量 溶液的目的是除尽 溶液的目的是除尽 |
D.若称得精盐的质量为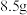 ,则该粗盐样品中氯化钠的纯度是 ,则该粗盐样品中氯化钠的纯度是 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】从海水中得到的粗盐中往往含有泥沙和氯化钙、氯化镁、硫酸钠等杂质,某化学兴趣小组进行了如下操作:

(1)图中3个操作都用到了玻璃棒,其中未使用玻璃棒搅拌的操作是______ (填序号)
(2)请用化学方程式表示加入氯化钡的作用:________ 。
(3)按照上图所示流程,能否用价格更便宜的熟石灰代替氢氧化钠来提纯氯化钠?请说明理由。

(1)图中3个操作都用到了玻璃棒,其中未使用玻璃棒搅拌的操作是
(2)请用化学方程式表示加入氯化钡的作用:
(3)按照上图所示流程,能否用价格更便宜的熟石灰代替氢氧化钠来提纯氯化钠?请说明理由。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐3】广西有较长的海岸线,海水综合利用对促进广西经济发展有重要意义。如图是海水综合利用的一种流程示意图,请回答相关问题。
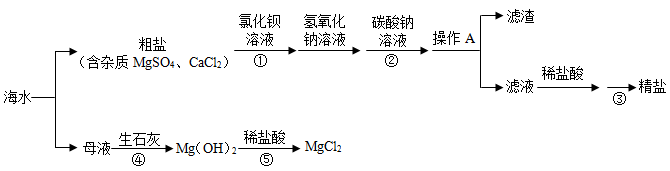
(1)从海水中获得粗盐的化学原理是________ ,操作A为________ 。
(2)在除杂过程中,为保证将杂质完全除去,加入的除杂试剂常需略过量。流程中加入氯化钡溶液应该在碳酸钠溶液之前,其目的是____________________________________ 。
(3)流程中⑤加入稀盐酸时发生反应的化学方程式为______________________________ 。

(1)从海水中获得粗盐的化学原理是
(2)在除杂过程中,为保证将杂质完全除去,加入的除杂试剂常需略过量。流程中加入氯化钡溶液应该在碳酸钠溶液之前,其目的是
(3)流程中⑤加入稀盐酸时发生反应的化学方程式为
您最近一年使用:0次