生活中处处有化学。
(1)市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等。所谓“加碘盐”是指在一定量的食盐中加入一定量的碘酸钾(化学式为KIO3),请写出碘酸钾中碘元素的化合价______ 。
(2)煤、石油和_________ 常被称为化石燃料,大量燃煤(含杂质硫、氮等)造成的主要环境问题有_______ (答出一点即可)。
(3)在含有硫酸镁、硫酸铜的工业废水中加入过量的锌粉,充分反应后过滤,所得滤渣是(填写化学式)____________ 。
(4)氢化钙(CaH2)固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气。请写出每千克该物质的能够制取的氢气质量为____________ g(保留到0.1g)。
(1)市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等。所谓“加碘盐”是指在一定量的食盐中加入一定量的碘酸钾(化学式为KIO3),请写出碘酸钾中碘元素的化合价
(2)煤、石油和
(3)在含有硫酸镁、硫酸铜的工业废水中加入过量的锌粉,充分反应后过滤,所得滤渣是(填写化学式)
(4)氢化钙(CaH2)固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气。请写出每千克该物质的能够制取的氢气质量为
更新时间:2020-03-05 18:09:39
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】根据如图所示装置回答有关问题。

(1)写出a仪器名称__________ ;
(2)利用A装置制取氧气的化学方程式为______ ;若用C装置来收集氧气,待集气瓶中的水排完以后,应当___________________ ;
(3)实验室通常利用B、D装置的组合来制取并收集二氧化碳,需要的药品为__________________ (填名称);
(4)实验室通常利用E装置检验二氧化碳的存在,若二氧化碳过量,会进一步与碳酸钙、水反应生成易溶于水的碳酸氢钙【CaCO3+H2O+CO2=Ca(HCO3)2】。若向含有Ca(OH)214.8g的澄清石灰水里缓缓通入一定量的二氧化碳,反应后若生成10g沉淀,则通入二氧化碳的质量可能为____ (填字母)。
A 4. 4g B 8. 8g C 13. 2g D 17. 6g

(1)写出a仪器名称
(2)利用A装置制取氧气的化学方程式为
(3)实验室通常利用B、D装置的组合来制取并收集二氧化碳,需要的药品为
(4)实验室通常利用E装置检验二氧化碳的存在,若二氧化碳过量,会进一步与碳酸钙、水反应生成易溶于水的碳酸氢钙【CaCO3+H2O+CO2=Ca(HCO3)2】。若向含有Ca(OH)214.8g的澄清石灰水里缓缓通入一定量的二氧化碳,反应后若生成10g沉淀,则通入二氧化碳的质量可能为
A 4. 4g B 8. 8g C 13. 2g D 17. 6g
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下列科普短文,回答问题。
新能源汽车已经走进了我们的生活。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示。其中能量密度表示单位体积的电池所具有的能量;氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物。氢气可通过电解水(原理如图2)等多种方式获得。据测算, 氢气完全燃烧可释放
氢气完全燃烧可释放 的热量,
的热量, 汽油完全燃烧可释放
汽油完全燃烧可释放 的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。
的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。______ 。
(2) 氢气完全燃烧,消耗氧气的质量为
氢气完全燃烧,消耗氧气的质量为______ 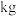 。
。
(3)依据测算数据可知,氢内燃车与汽油车相比的优势是______ 。
(4)乙醇燃烧的化学方程式______ 。
(5)下列说法正确的是______(填序号)。
(6)太阳能电池需要大量的单质硅,单质硅是由石英固体 与碳在高温条件下反应制得的,其中
与碳在高温条件下反应制得的,其中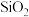 与
与 的化学计量数比为
的化学计量数比为 ,该反应的化学方程式为
,该反应的化学方程式为______ 。
新能源汽车已经走进了我们的生活。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示。其中能量密度表示单位体积的电池所具有的能量;氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物。氢气可通过电解水(原理如图2)等多种方式获得。据测算,
 氢气完全燃烧可释放
氢气完全燃烧可释放 的热量,
的热量, 汽油完全燃烧可释放
汽油完全燃烧可释放 的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。
的热量;乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取;太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。我国新能源汽车发展迅速,未来可期。
(2)
 氢气完全燃烧,消耗氧气的质量为
氢气完全燃烧,消耗氧气的质量为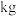 。
。(3)依据测算数据可知,氢内燃车与汽油车相比的优势是
(4)乙醇燃烧的化学方程式
(5)下列说法正确的是______(填序号)。
| A.依据图1可知,提供相同能量时,铝空电池的体积最小 |
B.图2中, 口产生的气体为氢气 口产生的气体为氢气 |
| C.农业大国盛产甘蔗和玉米,有利于推广乙醇汽车 |
| D.报废的电动汽车电池,要及时用土进行掩埋处理 |
(6)太阳能电池需要大量的单质硅,单质硅是由石英固体
 与碳在高温条件下反应制得的,其中
与碳在高温条件下反应制得的,其中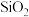 与
与 的化学计量数比为
的化学计量数比为 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
【推荐3】甲、乙、丙均为初中化学常见物质,其转化关系如图所示(“→”表示反应能一步实现,部分反应物、生成物和反应条件均已略去),请回答:

(1)若甲、乙组成元素相同且常温下为液态,反应皆为分解反应,则丙的用途之一是_____ 。
(2)若甲是黑色固体单质,乙、丙组成元素相同且常温下为气态,乙的相对分子质量大于丙,则甲的化学式为_____ ;乙→丙的化学方程式为_____ ;若12g甲与ag某单质反应同时生成乙和丙,则a的取值范围是_____ 。

(1)若甲、乙组成元素相同且常温下为液态,反应皆为分解反应,则丙的用途之一是
(2)若甲是黑色固体单质,乙、丙组成元素相同且常温下为气态,乙的相对分子质量大于丙,则甲的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】用数字和化学符号填空:
(1)氮分子___________ ;
(2)2个亚铁离子___________ ;
(3)8个干冰分子___________ ;
(4)氧化铝中铝元素的化合价___________ ;
(5)保持水的化学性质的最小粒子___________ 。
(1)氮分子
(2)2个亚铁离子
(3)8个干冰分子
(4)氧化铝中铝元素的化合价
(5)保持水的化学性质的最小粒子
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】超氧化钾( )常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾和过氧化氢。
)常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾和过氧化氢。
(1)画出氧原子结构示意图:______ 。
(2)写出氢氧化钾的化学式:______ 。
(3)标出过氧化氢中氧元素的化合价:______ 。
(4)写出超氧化钠的化学式:______ 。
 )常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾和过氧化氢。
)常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾和过氧化氢。(1)画出氧原子结构示意图:
(2)写出氢氧化钾的化学式:
(3)标出过氧化氢中氧元素的化合价:
(4)写出超氧化钠的化学式:
您最近一年使用:0次
【推荐3】据报道我国率先试采可燃冰取得成功。可燃冰主要含有甲烷水合物。甲烷在一定条件下与氯气反应的微观示意图如图所示。请回答下列问题。

(1)碳原子核外电子总数为________________ 。
(2)左上图中的“12.01”表示碳原子的________________ 。
(3)CH4中碳元素的化合价为________________ ,氢元素的质量分数是________________ %。
(4)请尝试写出上述反应的化学方程式________________ 。

(1)碳原子核外电子总数为
(2)左上图中的“12.01”表示碳原子的
(3)CH4中碳元素的化合价为
(4)请尝试写出上述反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属及金属材料在生产、生活中应用广泛。
(1)铝抗腐蚀性能较强,原因是______ (用化学方程式表示)。
(2)小明在学习金属的化学性质时,做了如下探究实验,如图所示(金属片已打磨):
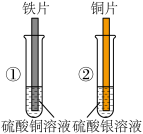
图①中,铁片表面的现象是______ ;
图②中,铜片插入硝酸银溶液中,反应的化学方程式是______ 。
(3)此探究实验的目的是______ 。
(1)铝抗腐蚀性能较强,原因是
(2)小明在学习金属的化学性质时,做了如下探究实验,如图所示(金属片已打磨):

图①中,铁片表面的现象是
图②中,铜片插入硝酸银溶液中,反应的化学方程式是
(3)此探究实验的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】把一定质量的锌粉投入到硫酸亚铁和硫酸铜的混合溶液A中,充分搅拌,过滤。回答下列问题。

(1)若向滤渣C中加入适量稀硫酸,有气体生成。滤渣C中一定有_____ ,滤液B中除水外,一定有_____ 。
(2)若向溶液A中加入过量的锌粉,写出向滤渣C中加入足量硫酸,发生的反应的化学方程式为_____ 、_____ 。

(1)若向滤渣C中加入适量稀硫酸,有气体生成。滤渣C中一定有
(2)若向溶液A中加入过量的锌粉,写出向滤渣C中加入足量硫酸,发生的反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】人类的生活和生产都离不开金属,铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。
(1)生活中的菜刀用铁制作而不用铝制作,理由是_____________ 。
(2)铝制品具有良好的抗腐蚀性能的原因是_____________ 。
(3)请写出一条保护金属资源的有效途径:_____________ 。
(4)化学兴趣小组同学进行了如下废液处理:

①操作I的名称是____ ;实验室进行操作I时,能起到引流作用的仪器是____ 。
②滤渣中含有的物质是_____________ 。
(1)生活中的菜刀用铁制作而不用铝制作,理由是
(2)铝制品具有良好的抗腐蚀性能的原因是
(3)请写出一条保护金属资源的有效途径:
(4)化学兴趣小组同学进行了如下废液处理:

①操作I的名称是
②滤渣中含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】煤的综合利用有利于保护自然环境和社会的可持续发展。
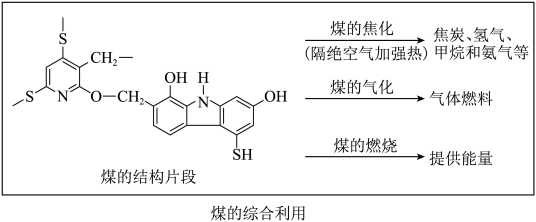
(1)由煤的结构片段可知:煤燃烧会产生大气污染,其中_____ 排放到空气中会导致酸雨。
(2)煤的焦化属于_____ 变化;焦化获得的焦炭可用于高炉炼铁,高炉内CO和Fe2O3反应的化学方程式为 _____ 。焦化获得的氨气可用于制取氮肥,区分(NH4)2SO4和NH4Cl两种化肥可选用的试剂是 _____ (填对应选项的字母)。
A 熟石灰 B 氯化钡 C 盐酸
(3)焦化获得的焦炭可用于制取水煤气。我国科学家研究出碳化钼(Mo2C)负载金原子组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如下图所示。
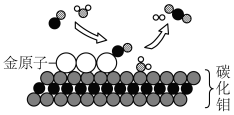
①从反应微观模型看,金原子对反应物_____ (填化学式)起吸附催化作用。
②反应的化学方程式为_____ 。

(1)由煤的结构片段可知:煤燃烧会产生大气污染,其中
(2)煤的焦化属于
A 熟石灰 B 氯化钡 C 盐酸
(3)焦化获得的焦炭可用于制取水煤气。我国科学家研究出碳化钼(Mo2C)负载金原子组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如下图所示。

①从反应微观模型看,金原子对反应物
②反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】我国承诺2030年前实现“碳达峰”,2060年前实现“碳中和”,体现大国担当。
(1)减少CO2排放,可以减缓________________________ 。
(2)“碳中和”是指在规定时期内实现排放多少CO2就做多少抵消措施来达到平衡,实现CO2“净零”排放。自然界中消耗二氧化碳的主要途径是__________________ 。
(3)“碳达峰”是指CO2排放量达到最高值。下列有利于控制二氧化碳排放的是 。
(4)科技人员将二氧化碳在催化剂的作用下与氢气反应,转化为一种液体燃料甲醇(CH3OH)和水,该反应的化学方程式为_________________________________ 。
(1)减少CO2排放,可以减缓
(2)“碳中和”是指在规定时期内实现排放多少CO2就做多少抵消措施来达到平衡,实现CO2“净零”排放。自然界中消耗二氧化碳的主要途径是
(3)“碳达峰”是指CO2排放量达到最高值。下列有利于控制二氧化碳排放的是 。
| A.少使用一次性餐具 | B.使用清洁能源 | C.推广电动汽车 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源。煤气化和液化流程示意图如下图所示,请结合图像回答问题:

(1)精炼煤中主要成分是碳,步骤②中发生反应的化学方程式为_____ 。
(2)步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为_____ 。
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为_____ ,该反应的基本类型是_____ 。
(4)循环气的主要成分是_____ 和少量未完全分离出去的甲醇。

(1)精炼煤中主要成分是碳,步骤②中发生反应的化学方程式为
(2)步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为
(4)循环气的主要成分是
您最近一年使用:0次



