19. 某化学兴趣小组通过探究活动学习和理解化学知识。请你一起研究学习,并回答有关问题。
研究问题:水溶液中复分解反应的微观实质
相关信息:
(Ⅰ)电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。
(Ⅱ)相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)
2溶液中滴加2-3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。

①写出Ba(OH)
2与H
2SO
4反应的化学方程式
____________。
②M点时电导率为零,离子浓度也几乎为零,此时混合液体静置后呈
____________色;
③通过对甲曲线的分析,下列说法错误的是
____________(填序号)。
A.M点前曲线下滑的过程中,H
+和OH
-结合成H
2O,Ba
2+和SO
42-结合成BaSO
4B.M点后溶液电导率逐渐增大,仅由于溶液中H
+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)
2溶液中滴加2-3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na
2SO
4溶液,测得溶液的电导率变化如上图乙曲线所示。
①通过对乙曲线的分析,下列说法正确的是
____________(填序号)。
A.实际参加反应的是Ba
2+和SO
42-结合成了BaSO
4,Na
+和OH
-还是以离子形式存在于溶液中
B.溶液红色只会变浅,但不会褪去
②N点时,溶液中大量含有的离子是
___________(填离子符号)。
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度
____________(填“增大”或“减小”)。
(3)拓展:
①请根据示例仿写离子方程式。
示例
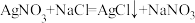
离子方程式:

仿写:

离子方程式:
____________________。
②向一定量饱和澄清石灰水中持续通入过量的CO
2气体,溶液先变浑浊后浑浊逐渐消失。请推测此过程的溶液中Ca
2+的浓度变化情况
_________________。