实验室加热氯酸钾与二氧化锰的混合物制取氧气,完全反应后的剩余固体中含有氯化钾和二氧化锰,兴趣小组同学用图所示流程回收提纯氯化钾和二氧化锰。
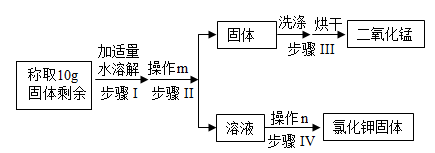
(1)步骤 I 中需要控制水的用量不宜过多原因是_ (填标号)。
A 节约实验时间 B 保证固体混合物全部溶解 C 节约能源
(2)写出图中中仪器 a、b 的名称:a___ ,b__ 。
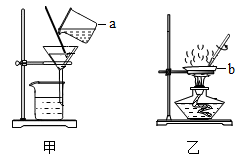
(3)组装图中的甲装置时,折叠滤纸的情形如图所示,其中错误是_ (填标号)。
A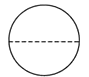 B
B 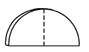 C
C  D
D 
(4)步骤 II 中的操作 m 应选择上图中的__ 装置(填标号),该操作中玻璃棒的作用是__ 。
(5)步骤 IV 中的操作 n 应选择上图中的__ 装置(填标号),该操作中玻璃棒的作用是___ 。
(6)实验结束后,称得回收到的氯化钾与二氧化锰的总质量小于 10 g,可能的原因是__ (写一点)。

(1)步骤 I 中需要控制水的用量不宜过多原因是
A 节约实验时间 B 保证固体混合物全部溶解 C 节约能源
(2)写出图中中仪器 a、b 的名称:a

(3)组装图中的甲装置时,折叠滤纸的情形如图所示,其中错误是
A
 B
B  C
C  D
D 
(4)步骤 II 中的操作 m 应选择上图中的
(5)步骤 IV 中的操作 n 应选择上图中的
(6)实验结束后,称得回收到的氯化钾与二氧化锰的总质量小于 10 g,可能的原因是
更新时间:2020-03-17 22:39:20
|
相似题推荐
填空与简答-简答题
|
较难
(0.4)
【推荐1】请结合下列实验常用装置,回答有关问题。

(1)图中仪器a的名称是______ 。
(2)实验室用A装置制取氧气,反应的化学方程式是______ 。
(3)实验室制取二氧化碳的药品为______ ;如果用E装置收集该气体,则气体从______ 端进入(填“b”或“c”),若要用E装置检验二氧化碳,瓶中需装的试剂为______ 。
(4)实验室常用装置C代替装置B制取气体,该装置的优点是______ ,下列反应适用于该装置的是______ (填序号)。
a.加热高锰酸钾制氧气
b.锌粒与稀硫酸制氢气
c.过氧化氢溶液与二氧化锰粉末混合制氧气
(5)小明查阅资料得知:除二氧化锰外,许多水果对过氧化氢分解也有催化作用。为了探究苹果质量对过氧化氢分解速度的影响,用如图甲所示装置(固定装置未画出)进行以下实验:

①检查装置气密性。
②称取1g苹果,切成小块放入烧瓶中,量取10mL溶质质量分数为5%的过氧化氢溶液倒入烧瓶中,迅速塞紧塞子,当液滴移至A点时开始计时。
②观察到液滴恰好移至B点时(AB间玻璃管容积为6mL),记录所需时间。
③依次用不同质量的苹果重复步骤②和③,记录并处理数据,结果如图乙。
根据上述实验记录回答:本实验可得出的结论是______ 。若用20mL5%的过氧化氢溶液与6g苹果重复上述实验,预测实验中步骤③记录的时间是______ 秒。

(1)图中仪器a的名称是
(2)实验室用A装置制取氧气,反应的化学方程式是
(3)实验室制取二氧化碳的药品为
(4)实验室常用装置C代替装置B制取气体,该装置的优点是
a.加热高锰酸钾制氧气
b.锌粒与稀硫酸制氢气
c.过氧化氢溶液与二氧化锰粉末混合制氧气
(5)小明查阅资料得知:除二氧化锰外,许多水果对过氧化氢分解也有催化作用。为了探究苹果质量对过氧化氢分解速度的影响,用如图甲所示装置(固定装置未画出)进行以下实验:

①检查装置气密性。
②称取1g苹果,切成小块放入烧瓶中,量取10mL溶质质量分数为5%的过氧化氢溶液倒入烧瓶中,迅速塞紧塞子,当液滴移至A点时开始计时。
②观察到液滴恰好移至B点时(AB间玻璃管容积为6mL),记录所需时间。
③依次用不同质量的苹果重复步骤②和③,记录并处理数据,结果如图乙。
根据上述实验记录回答:本实验可得出的结论是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A是暗紫色固体,B是人体生命活动离不开的气体,E是淡黄色固体,F是一种有害气体,实验室可用水来吸收少量的F,其中G和H是白色固体,请根据下图回答问题。它们之间有如下图所示的转化关系,请回忆所学内容,回答下列问题:

(1)写出物质C、F的名称:C______ ,F______ 。物质G的化学式:______ 。
(2)反应①涉及的化学符号表达式:______ ;属______ 反应(填基本反应类型)。
(3)检验B物质的方法______ 。
(4)反应②的实验现象:______ 。
(5)反应②涉及的化学反应的符号表达式:______ 。

(1)写出物质C、F的名称:C
(2)反应①涉及的化学符号表达式:
(3)检验B物质的方法
(4)反应②的实验现象:
(5)反应②涉及的化学反应的符号表达式:
您最近一年使用:0次
【推荐1】掌握科学的研究方法,探索化学世界的奥秘。
(1)分类是学习化学的重要方法之一,生活中,常会接触到下列物质:
A 钢丝 B 甲烷 C 生石灰 D 碘酒
其中属于混合物的是_____ (填字母,下同),属于氧化物的是_____ 。
(2)实验室中可用KClO3在MnO2催化下受热分解制取氧气,化学方程式为_____ ,将反应后的混合物进行分离。实验操作如图所示:

①图A中试管口略向下倾斜的原因是_____ ;
图B操作中玻璃棒的作用是_____ ;
图C操作中的一处明显错误是_____ 。
(3)质量守恒定律是帮助我们认识化学反应实质的重要理论。①下列表述正确的是_____ 。
A 蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B 每32gS和32gO2完全反应后,生成64gSO2
C 在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如表:
若参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是_____ 。
(1)分类是学习化学的重要方法之一,生活中,常会接触到下列物质:
A 钢丝 B 甲烷 C 生石灰 D 碘酒
其中属于混合物的是
(2)实验室中可用KClO3在MnO2催化下受热分解制取氧气,化学方程式为

①图A中试管口略向下倾斜的原因是
图B操作中玻璃棒的作用是
图C操作中的一处明显错误是
(3)质量守恒定律是帮助我们认识化学反应实质的重要理论。①下列表述正确的是
A 蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B 每32gS和32gO2完全反应后,生成64gSO2
C 在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如表:
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
若参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】p型透明导电化合物CuAlO2具有良好的热电性能,在热电转换领域具有广阔的应用前景。银铜合金广泛用于航空工业,如图为从航空切割废料中回收银并制备CuAlO2的工艺流程。

【资料】Ⅰ、难溶性碱受热易分解为两种氧化物,Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃;
Ⅱ、CuAlO2高温易分解、受热易氧化;银在空气中不易被氧化。
请回答下列问题:
(1)操作Ⅰ的名称是_____ ,此操作不用玻璃棒的后果_____ 滤液A中的溶质为_____ 。
(2)煮沸过程中蓝色固体发生分解反应的化学方程式为_____ 。
(3)“煅烧”时温度须控制在1042-1085℃范围内且在氩气中进行,其原因是_____ 。

【资料】Ⅰ、难溶性碱受热易分解为两种氧化物,Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃;
Ⅱ、CuAlO2高温易分解、受热易氧化;银在空气中不易被氧化。
请回答下列问题:
(1)操作Ⅰ的名称是
(2)煮沸过程中蓝色固体发生分解反应的化学方程式为
(3)“煅烧”时温度须控制在1042-1085℃范围内且在氩气中进行,其原因是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】我国化工专家侯德榜发明了“联合制碱法”,其生产过程中发生的反应主要是:其工业生产纯碱的工艺流程示意图如下所示,其中向粗盐水中加入的沉淀剂A、B分别为氧化钙和碳酸钠.
① NH3 + CO2 + H2O = NH4HCO3 ② NH4HCO3 + NaCl = NaHCO3↓ + NH4Cl ③ 2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑

请回答下列问题:
(1)实验室提纯粗盐的实验操作依次为:取样、溶解、沉淀、过滤、蒸发结晶.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出一种可能的原因:______ .
(2)实验室中,用提纯得到的氯化钠配制100g 0.9%的生理盐水,使用的仪器除药匙、玻璃棒、托盘天平、胶头滴管、烧杯外,还需要适当的仪器是_________ .
(3)生产纯碱的工艺流程中,碳酸化时析出NaHCO3晶体,没有析出Na2CO3晶体的原因是____ 。
(4)本工艺流程中氨(氨气)是循环使用的,为此,向滤液D中加入石灰水产生氨(氨气).写出该反应的化学方程式_________ 。
① NH3 + CO2 + H2O = NH4HCO3 ② NH4HCO3 + NaCl = NaHCO3↓ + NH4Cl ③ 2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
请回答下列问题:
(1)实验室提纯粗盐的实验操作依次为:取样、溶解、沉淀、过滤、蒸发结晶.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出一种可能的原因:
(2)实验室中,用提纯得到的氯化钠配制100g 0.9%的生理盐水,使用的仪器除药匙、玻璃棒、托盘天平、胶头滴管、烧杯外,还需要适当的仪器是
(3)生产纯碱的工艺流程中,碳酸化时析出NaHCO3晶体,没有析出Na2CO3晶体的原因是
(4)本工艺流程中氨(氨气)是循环使用的,为此,向滤液D中加入石灰水产生氨(氨气).写出该反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】杂卤石属于“呆矿”,主要成分有K2SO4、MgSO4、CaSO4、不溶性成分等,可作为一种钾资源。实验室模拟工厂用杂卤石溶浸液制备硫酸钾,流程如下:(假设不溶性成分不参加反应)

(1)在实验流程中,“加过量的石灰乳”的目的是除去溶浸液中的___________ ,用石灰乳而不用澄清石灰水的原因是__________________________________________ 。
(2)X溶液中的溶质是______________ (写名称)。
(3)固体B含有杂卤石中的不溶性成分和加试剂时所产生的_______________ (写化学式)。
(4)向溶液A中加稀硫酸时,所发生中和反应的化学方程式为_________________ 。
(5)操作b的名称是___________ ,需要用到的仪器有铁架台、酒精灯、玻璃棒和________ 。

(1)在实验流程中,“加过量的石灰乳”的目的是除去溶浸液中的
(2)X溶液中的溶质是
(3)固体B含有杂卤石中的不溶性成分和加试剂时所产生的
(4)向溶液A中加稀硫酸时,所发生中和反应的化学方程式为
(5)操作b的名称是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】提纯含少量泥沙的粗盐样品,实验过程和氯化钠的溶解度数据如下:

(1)该实验操作Ⅰ名称是________ ;
(2)蒸发时,一般有如下操作:①放置酒精灯,②放置蒸发皿,③加热并搅拌,④固定铁圈位置,⑤停止加热,用余热蒸干。正确的操作顺序是_______________ ;
(3)经称量,未溶解的粗盐质量为1.2g,得到精盐的质量为2.7g。则粗盐的产率是________ 。(结果保留一位小数)下列因素会导致获得的精盐质量偏小的是________ (填序号)
A蒸发时液滴溅出 B过滤时,滤纸破损
(4)由于粗盐中含有少量 、
、 、
、 等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
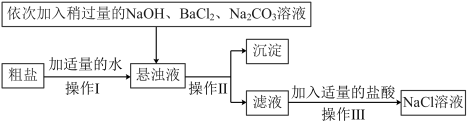
①加入稍过量的 溶液能除去粗盐中的
溶液能除去粗盐中的 ,反应的化学方程式为
,反应的化学方程式为_____________________ 。
②通过操作Ⅱ所得滤液中的溶质有____________________ (用化学式表示)。

(1)该实验操作Ⅰ名称是
(2)蒸发时,一般有如下操作:①放置酒精灯,②放置蒸发皿,③加热并搅拌,④固定铁圈位置,⑤停止加热,用余热蒸干。正确的操作顺序是
(3)经称量,未溶解的粗盐质量为1.2g,得到精盐的质量为2.7g。则粗盐的产率是
A蒸发时液滴溅出 B过滤时,滤纸破损
(4)由于粗盐中含有少量
 、
、 、
、 等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图:
①加入稍过量的
 溶液能除去粗盐中的
溶液能除去粗盐中的 ,反应的化学方程式为
,反应的化学方程式为②通过操作Ⅱ所得滤液中的溶质有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室有氯化钾样品,其中含有少量的CaCl2、MgCl2、K2SO4等杂质,将其进行精制的流程如图:

(1)操作Ⅲ名称是___________ ,在操作Ⅱ中玻璃棒的作用是:___________ 。
(2)流程图中加入稍过量的KOH、BaCl2、K2CO3时顺序___________ (填“可以”或“不可以”)改变,若可以,你认为顺序还可以是___________ (填一种即可,若填不可以,此空可不填)
(3)写出流程图中加入KOH生成沉淀的化学方程式:___________ 。
(4)请设计实验证明滤液中除了氯化钾外还含有的溶质(简要写出实验步骤、现象和结论)___________ 。

(1)操作Ⅲ名称是
(2)流程图中加入稍过量的KOH、BaCl2、K2CO3时顺序
(3)写出流程图中加入KOH生成沉淀的化学方程式:
(4)请设计实验证明滤液中除了氯化钾外还含有的溶质(简要写出实验步骤、现象和结论)
您最近一年使用:0次




