盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化如图。
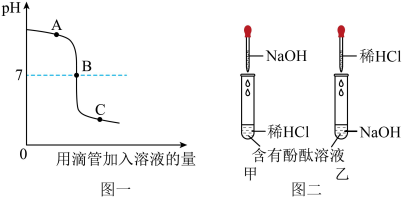
(1)盐酸和氢氧化钠溶液反应的化学方程式为_____ 。
(2)实验中滴入酚酞溶液的目的是_____ 。
(3)根据pH变化图象判断,该反应的实验过程是按照_____ (填“甲”或“乙”)图进行。
(4)图象上A、B、C 三点表示的溶液中,表示反应物二者恰好完全反应的是_____ (填“A、B或C”)点的溶液,呈现无色的是_____ (填“A、B或C”)点的溶液。C点所对应的溶液中溶质的主要成分是_____ (填化学式)。
(5)向C点所对应的溶液中加入一种药品,便能确定溶质组成。这种药品可能是_____ (填字母)。
A CuO B Cu C 紫色石蕊溶液

(1)盐酸和氢氧化钠溶液反应的化学方程式为
(2)实验中滴入酚酞溶液的目的是
(3)根据pH变化图象判断,该反应的实验过程是按照
(4)图象上A、B、C 三点表示的溶液中,表示反应物二者恰好完全反应的是
(5)向C点所对应的溶液中加入一种药品,便能确定溶质组成。这种药品可能是
A CuO B Cu C 紫色石蕊溶液
更新时间:2020-03-26 19:40:03
|
相似题推荐
实验题
|
适中
(0.65)
真题
解题方法
【推荐1】为判断某物质存在或某物质恰好完全反应,通常以特定物质的显色达到目,能显色的物质就称“指示剂”。如:用蓝色的石蕊试纸变红判断待测液显酸性;用淀粉溶液变蓝判断单质碘(I2)的存在:
已知:SO2+I2+2H2O═H2SO4+2HI(无色溶液);
常温下,碘微溶入水;
5SO2+2H2O+KMnO4═K2SO4+2H2SO4+2MnSO4(无色溶液)。
(1)工业上测量SO2,N2,O2混合气体的SO2含量用如图吸收装置(量气装置省略)。

①混合气体通过图示吸收装置一定时间后,当溶液颜色由蓝色变为_______ 色时即可停止通气。此法适宜测SO2含量较______ (选填“低”或“高”)的混合气体。
②吸收装置内的I2的淀粉溶液一也可以用_______ 溶液代替作为指示剂。因为________ 。
(2)若用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应。
①原盐酸中溶质的质量分数为________ 。
②试列式计算说明将该反应后的溶液转化为20℃时饱和溶液的一种简单方法_______ (计算结果精确到0.1g)。已知:20℃时氯化钠的溶解度为36g。
已知:SO2+I2+2H2O═H2SO4+2HI(无色溶液);
常温下,碘微溶入水;
5SO2+2H2O+KMnO4═K2SO4+2H2SO4+2MnSO4(无色溶液)。
(1)工业上测量SO2,N2,O2混合气体的SO2含量用如图吸收装置(量气装置省略)。

①混合气体通过图示吸收装置一定时间后,当溶液颜色由蓝色变为
②吸收装置内的I2的淀粉溶液一也可以用
(2)若用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应。
①原盐酸中溶质的质量分数为
②试列式计算说明将该反应后的溶液转化为20℃时饱和溶液的一种简单方法
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】根据实验,回答问题。

(1)稀盐酸和稀硫酸都能使紫色石蕊溶液变红的原因是溶液中都含有___ 。
(2)甲乙图中能证明CO2与NaOH溶液发生化学反应的现象是___________ 。
(3)点燃氢气前,需要进行的操作是__________ 。
(4)电解水实验得出的结论是水由_________ 组成。

(1)稀盐酸和稀硫酸都能使紫色石蕊溶液变红的原因是溶液中都含有
(2)甲乙图中能证明CO2与NaOH溶液发生化学反应的现象是
(3)点燃氢气前,需要进行的操作是
(4)电解水实验得出的结论是水由
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
【推荐1】某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如下面图一所示,溶液的温度变化如图二所示(不考虑反应过程中热量损失)。请回答下列问题:
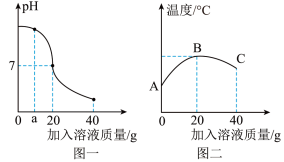
⑴图一:该变化对应的实验操作是将______ 滴加到另一种溶液中。当滴入溶液的质量为ag时,溶液中的溶质为_________ (填化学式)。当溶液的pH=7时,溶液中的主要离子是______________ (填离子符号)。当加入溶液的质量为40g时,向所得溶液中滴加紫色石蕊试液,溶液呈_______ 色。
⑵图二:表示酸碱恰好完全反应的点是____ ,说明该反应伴随_____ 现象(填“放热”或“吸热”)。
⑶如果实验中用去了20g溶质质量分数为4%的氢氧化钠溶液,根据图示计算稀盐酸中溶质的质量分数为_________________ 。

⑴图一:该变化对应的实验操作是将
⑵图二:表示酸碱恰好完全反应的点是
⑶如果实验中用去了20g溶质质量分数为4%的氢氧化钠溶液,根据图示计算稀盐酸中溶质的质量分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】某实验小组为探究稀硫酸性质,依次进行以下3组实验。如下图所示:

(1)写出图A中反应的化学方程式_______ 。
(2)图B开始加入NaOH无明显现象,继续滴加后产生红褐色沉淀。反应开始没有明显现象的原因:___ 。
(3)由图实验可知,稀硫酸能与金属氧化物、_______ (填物质类别)反应。
(4)稀硫酸和浓硫酸性质不同,设计实验鉴别两种酸:_______ (提示:从试剂或材料、操作、现象角度简要说明)。
(5)电动自行车常用铅酸电池,正极材料是二氧化铅(PbO2),负极是铅板(Pb),稀硫酸做电解质溶液,反应后生成水、硫酸铅(PbSO4)。写出反应的化学方程式:_______ 。

(1)写出图A中反应的化学方程式
(2)图B开始加入NaOH无明显现象,继续滴加后产生红褐色沉淀。反应开始没有明显现象的原因:
(3)由图实验可知,稀硫酸能与金属氧化物、
(4)稀硫酸和浓硫酸性质不同,设计实验鉴别两种酸:
(5)电动自行车常用铅酸电池,正极材料是二氧化铅(PbO2),负极是铅板(Pb),稀硫酸做电解质溶液,反应后生成水、硫酸铅(PbSO4)。写出反应的化学方程式:
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】实验是进行科学探究的重要方式.请填写下列空格:

(1)取两支相同的木条,将其中一支的一端浸入酒精中约10秒,将另一支的一端浸入水中约10秒,然后将两支木条的浸入端分别靠近酒精灯火焰片刻.此实验的目的是探究物质的燃烧与____________ 的关系.
(2)图A进行的实验是某同学取甲、乙两个完全相同的装满二氧化碳的塑料瓶,向甲、乙两瓶中分别倒入相同体积的蒸馏水和氢氧化钠溶液,然后将两瓶迅速拧紧瓶盖,振荡,观察现象.该实验的探究目的是_____________ .
(3)用图B所示方法,把二氧化碳气体慢慢倒入放有燃着蜡烛的烧杯中,下层蜡烛的火焰先熄灭,上层蜡烛的火焰后熄灭.本实验中,放置高低不同的两支蜡烛的目的是________________ .
(4)向一定量的稀盐酸中滴加氢氧化钠溶液,得到溶液的pH变化曲线如图C所示.曲线上a点所表示的意义是______________ .

(1)取两支相同的木条,将其中一支的一端浸入酒精中约10秒,将另一支的一端浸入水中约10秒,然后将两支木条的浸入端分别靠近酒精灯火焰片刻.此实验的目的是探究物质的燃烧与
(2)图A进行的实验是某同学取甲、乙两个完全相同的装满二氧化碳的塑料瓶,向甲、乙两瓶中分别倒入相同体积的蒸馏水和氢氧化钠溶液,然后将两瓶迅速拧紧瓶盖,振荡,观察现象.该实验的探究目的是
(3)用图B所示方法,把二氧化碳气体慢慢倒入放有燃着蜡烛的烧杯中,下层蜡烛的火焰先熄灭,上层蜡烛的火焰后熄灭.本实验中,放置高低不同的两支蜡烛的目的是
(4)向一定量的稀盐酸中滴加氢氧化钠溶液,得到溶液的pH变化曲线如图C所示.曲线上a点所表示的意义是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组为探究化学反应中的能量变化,进行盐酸与碳酸氢钠溶液的反应实验。如图是丁同学在20℃、基本隔热条件下利用温度传感器,分别测定向20ml水和20ml饱和碳酸氢钠溶液中各倒入20ml,浓度为13.7%盐酸的温度与时间变化曲线。曲线①为水+13.7%盐酸温度变化曲线,曲线②为饱和碳酸氢钠溶液+13.7%盐酸温度变化曲线。实验测得饱和碳酸氢钠溶液稀释时温度变化不大,可忽略不计。据此回答下列问题:

①写出盐酸与碳酸氢钠反应的化学方程式_________ ;
②18秒后,曲线①逐渐下降的原因是________ ;
③比较曲线①和曲线②,你认为13.7% 盐酸与饱和碳酸氢钠溶液的反应是_____ (填“放热”或“吸热”)反应,其理由是_________ 。

①写出盐酸与碳酸氢钠反应的化学方程式
②18秒后,曲线①逐渐下降的原因是
③比较曲线①和曲线②,你认为13.7% 盐酸与饱和碳酸氢钠溶液的反应是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】小徐为判断酸碱中和反应是否进行完全,往20g10%的氢氧化钠溶液中滴加10%的盐酸,装置如图1。
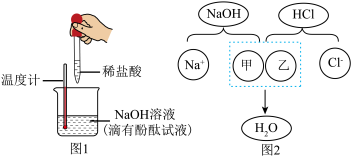
图1实验中温度变化如表所示。
(1)判断方法一:
利用指示剂颜色变化判断。溶液红色消失,因为中和反应的结果是酸和碱各自的特性都消失,图2描述的是氢氧化钠与盐酸反应的微观实质,请用符号或文字表示酸碱反应的实质:______ 。
(2)根据表格数据分析,当温度为______ ℃时表明中和反应完全进行。由此得出判断方法二:利用______ 变化来判断是否完全中和。

图1实验中温度变化如表所示。
| 加入盐酸的体积V/mL | 5 | 11 | 18 | 23 | 29 |
| 溶液温度t/℃ | 28.7 | 34.1 | 37.8 | 35.3 | 33.4 |
利用指示剂颜色变化判断。溶液红色消失,因为中和反应的结果是酸和碱各自的特性都消失,图2描述的是氢氧化钠与盐酸反应的微观实质,请用符号或文字表示酸碱反应的实质:
(2)根据表格数据分析,当温度为
您最近一年使用:0次

 并验证它的性质,某同学设计并进行了下图所示的实验,请根据要求回答有关问题。
并验证它的性质,某同学设计并进行了下图所示的实验,请根据要求回答有关问题。



