从CuSO4溶液、BaCl2溶液、NaOH溶液、稀H2SO4、K2CO3溶液中,选出两种溶液,按题目要求,完成下列方程式:
(1)生成蓝色沉淀的反应____________ ;
(2)酸与盐反应生成白色沉淀____________ ;
(3)有气体产生的反应____________ ;
(4)发生了中和反应____________ ;
(5)盐与盐反应生成白色沉淀____________ 。
(1)生成蓝色沉淀的反应
(2)酸与盐反应生成白色沉淀
(3)有气体产生的反应
(4)发生了中和反应
(5)盐与盐反应生成白色沉淀
更新时间:2020-03-30 11:56:58
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】分类法是学习化学的重要思想方法。现有下列三组物质:
A.空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3.H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
(2)请仿照检验CO2的反应原理,写出SO2与NaOH溶液反应的化学反应方程式________________________ 。
(3)NH4Cl溶液与KOH溶液能够反应,实质是因为它们在水中解离出来的 和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的
和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的________________ 结合生成了________________ 。
(4)请依据(3)中获得的启示,判断下列在水溶液中能大量共同存在的一组离子是________ 。
A.H+、OH- B.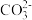 、H+
、H+
C.Cu2+、OH- D.Na+、Cl-
(5)在实验室有一些常识,如:氢氧化钠固体必须密封保存,原因是:__________________________ ,浓硫酸必须密封保存,原因是:__________________ ,如果溅到皮肤上应该先_____________ ,然后再____________________ 。打开浓盐酸瓶盖,瓶口有白雾,原因是:___________________________ 。
A.空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3.H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组 别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | |
| 不属于上述分类标准的物质 | 空气 | ② | SO2 |
(3)NH4Cl溶液与KOH溶液能够反应,实质是因为它们在水中解离出来的
 和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的
和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的(4)请依据(3)中获得的启示,判断下列在水溶液中能大量共同存在的一组离子是
A.H+、OH- B.
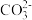 、H+
、H+C.Cu2+、OH- D.Na+、Cl-
(5)在实验室有一些常识,如:氢氧化钠固体必须密封保存,原因是:
您最近一年使用:0次
【推荐2】甲、乙两厂分布如图所示,箭头代表水流方向。两厂排放的废水中含有 、
、 、
、 、
、 、
、 、
、 六种离子,两厂分别含有其中不同的三种离子。如果在a处取水样进行检测,废水的pH大于7;两厂废水按适当比例混合,可将废水中的某些离子转化成沉淀,这样处理后c处的废水就可以达到排放标准。
六种离子,两厂分别含有其中不同的三种离子。如果在a处取水样进行检测,废水的pH大于7;两厂废水按适当比例混合,可将废水中的某些离子转化成沉淀,这样处理后c处的废水就可以达到排放标准。

(1)a处废水中一定含有的离子有____________
(2)b处废水中一定含有的离子有____________
(3)c处废水中只含有一种溶质的化学式____________ 。
 、
、 、
、 、
、 、
、 、
、 六种离子,两厂分别含有其中不同的三种离子。如果在a处取水样进行检测,废水的pH大于7;两厂废水按适当比例混合,可将废水中的某些离子转化成沉淀,这样处理后c处的废水就可以达到排放标准。
六种离子,两厂分别含有其中不同的三种离子。如果在a处取水样进行检测,废水的pH大于7;两厂废水按适当比例混合,可将废水中的某些离子转化成沉淀,这样处理后c处的废水就可以达到排放标准。
(1)a处废水中一定含有的离子有
(2)b处废水中一定含有的离子有
(3)c处废水中只含有一种溶质的化学式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水是生命之源,与生活生产关系密切。保护水环境、珍爱水资源,是每个公民应尽的责任和义务。
(1)已知含负一价的氢的化合物(如:NaH与水接触生成相应的碱和氢气),试写出CaH2与Na2CO3水溶液反应的化学方程式_______ 。
(2)在化学实验和科学研究中,水也是一种常用的试剂。水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______。
(3)要检验硬水需要用到肥皂水。肥皂的主要成分为硬脂酸钠(C17H35COONa),它是一种有机酸的钠盐,在肥皂水中滴入盐酸会发生复分解反应出现白色沉淀,这沉淀物是_______ (写化学式);若在肥皂水中加入硬水(含Ca2+、Mg2+)也会出现白色沉淀,此沉淀主要是_______ (写名称)。某城市滨临长江,将长江水净化处理可成为居民生活用水。
(4)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换后的水仍然呈电中性。_______ 个Na+。
②阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见物质检验阳离子交换柱已失效的方法是_______ 。
(1)已知含负一价的氢的化合物(如:NaH与水接触生成相应的碱和氢气),试写出CaH2与Na2CO3水溶液反应的化学方程式
(2)在化学实验和科学研究中,水也是一种常用的试剂。水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______。
| A.氧元素发生了改变 |
| B.微粒的组成发生了改变 |
| C.微粒的化学性质发生了改变 |
| D.与水分子比水合离子的电子数发生了改变 |
(3)要检验硬水需要用到肥皂水。肥皂的主要成分为硬脂酸钠(C17H35COONa),它是一种有机酸的钠盐,在肥皂水中滴入盐酸会发生复分解反应出现白色沉淀,这沉淀物是
(4)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换后的水仍然呈电中性。

②阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见物质检验阳离子交换柱已失效的方法是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F是初中化学常见的六种物质。A、B、D、E、F均由三种元素组成;A、B属于同类别的物质;C物质在固态时俗称干冰;A、E均含有入体中含量最多的金属元素;F可用于玻璃、造纸、纺织、洗涤剂的生产,部分反应物和产物已经略去,其中“—”表示两种物质间会反应,“→”表示一种物质会一步转化成另一种物质。请回答下列问题。

(1)写出化学式:E______ ,F______ 。
(2)D物质类别______ (填“酸”或“碱”或“盐”)。
(3)A与C的反应的化学方程式______ 。

(1)写出化学式:E
(2)D物质类别
(3)A与C的反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国动力锂电池生产、使用和出口均居世界前列。锂电回收和循环利用对解决环境污染有举足轻重的意义。如图钴酸锂废极片【主要成分为钴酸锂(LiCoO2)】的回收工艺。
②过氧化氢受热易分解。
(1)将废极片粉碎的目的是_______ 。
(2)酸浸时加入稀硫酸和过氧化氢,反应温度要控制在40℃以下,原因是_______ ,溶液的pH_______ 7,(填“<”或“>”)操作I的名称是_______ 。
(3)反应①中,CoC2O4与空气的O2反应生成的Co2O3和CO2的微粒个数比为_______ 。反应②发生的是复分解反应,该反应方程式为:_______ 。
(4)判断Li2CO3是否洗涤干净时,取最后一次洗涤液,向其中滴加_______ (写化学式)溶液,无白色沉淀生成。Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明它的溶解度随温度的升高而_______ (填“增大”或“减小”)。

②过氧化氢受热易分解。
(1)将废极片粉碎的目的是
(2)酸浸时加入稀硫酸和过氧化氢,反应温度要控制在40℃以下,原因是
(3)反应①中,CoC2O4与空气的O2反应生成的Co2O3和CO2的微粒个数比为
(4)判断Li2CO3是否洗涤干净时,取最后一次洗涤液,向其中滴加
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[ Al2(SO4)x( OH )6-2x]溶液,并用于烟气脱硫研究,工艺流程如下:

已知:SiO2不溶于水,常温下不与硫酸、碳酸钙反应;CaSO4微溶于水。
(1)酸浸时反应的化学方程式为_____________ 。
(2)滤渣I的主要成分为___________ (填化学式)。
(3)加CaCO3调节溶液的pH至3.6,其目的是与溶液中的过量的硫酸反应,并使Al2(SO4)3转化为Al2(SO4)x( OH )6-2x。滤渣Ⅱ的主要成分为_____ ( 填化学式),若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是__________ 。
(4)上述流程中经完全热分解放出的SO2量小于吸收的SO2量,达到脱硫的目的。除去二氧化硫还可以用石灰乳吸收,写出石灰乳吸收二氧化硫的化学方程式:_________ 。 比较这两种方法,碱式硫酸铝吸收二氧化硫的优点是___________ 。

已知:SiO2不溶于水,常温下不与硫酸、碳酸钙反应;CaSO4微溶于水。
(1)酸浸时反应的化学方程式为
(2)滤渣I的主要成分为
(3)加CaCO3调节溶液的pH至3.6,其目的是与溶液中的过量的硫酸反应,并使Al2(SO4)3转化为Al2(SO4)x( OH )6-2x。滤渣Ⅱ的主要成分为
(4)上述流程中经完全热分解放出的SO2量小于吸收的SO2量,达到脱硫的目的。除去二氧化硫还可以用石灰乳吸收,写出石灰乳吸收二氧化硫的化学方程式:
您最近一年使用:0次
【推荐2】某工业园区甲、乙两化工厂排放的废水中含有K+、 Cu2+、Fe3+、C1- 、OH-、NO3-六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质带来产重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水星碱性。
(1)甲厂废水中定含有的离子是_______ ,可能含有的离子是_______ ;
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是_______ (填离子符号),过滤后的废水中主要含有______ 两种物质(填化学式),处理后的废水符合排放标准。
(1)甲厂废水中定含有的离子是
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是
您最近一年使用:0次




