盐酸、硫酸、氢氧化钠是重要的化工原料。
(1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具有___________ 性。
(2)稀盐酸和稀硫酸都可以用于金属除锈,是因为它们的溶液中都含有___________ 。
(3)氢氧化钠暴露在空气中,容易潮解,同时吸收空气中的___________ 而变质。为检验氢氧 化钠溶液是否部分变质,分别取少量样品于试管中进行如下实验,其中能达到实验目的的是___________ (填序号)。
A滴加稀盐酸 B滴加氢氧化钡溶液
C滴加 1-2 滴酚酞溶液 D滴加适量的氯化钙溶液、静置、再滴加酚酞溶液
(4)我国对江河的管理实施了河长制,某条河的附近有一硫酸厂,欲检验该厂废水呈酸性,一般可选用下列药品中的___________ (填字母序号)。
ACa(OH)2 BMg CCaO DAgNO3 ENa2CO3
(1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具有
(2)稀盐酸和稀硫酸都可以用于金属除锈,是因为它们的溶液中都含有
(3)氢氧化钠暴露在空气中,容易潮解,同时吸收空气中的
A滴加稀盐酸 B滴加氢氧化钡溶液
C滴加 1-2 滴酚酞溶液 D滴加适量的氯化钙溶液、静置、再滴加酚酞溶液
(4)我国对江河的管理实施了河长制,某条河的附近有一硫酸厂,欲检验该厂废水呈酸性,一般可选用下列药品中的
ACa(OH)2 BMg CCaO DAgNO3 ENa2CO3
更新时间:2020-04-04 20:26:05
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】氨(NH3)用于制造氮肥、复合肥料、硝酸、纯碱等,广泛应用于化工、轻工、化肥制药、合成纤维等领域。
Ⅰ、工业制氨是以哈伯法通过氮气和氢气在高温高压和催化剂的作用下化合生成。实验室模拟合成氨气的流程如下:
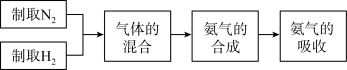
(1)获取氮气:在特定装置内将空气液化,然后升温,先出来的气体就是氮气。该方法利用的原理是液氮和液氧的______ 不同。但在实验室条件下空气不易液化,以下 A—C 是实验室获取氮气的方法及装置,其中得到氮气较纯的是______ (填字母)。
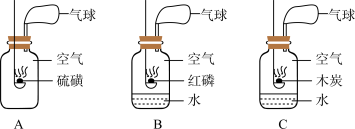
(2)合成氨气:上述流程中氮气与氢气混合时最佳的质量比为______ 。
Ⅱ、1898 年德国人首次发现空气中的氮能被碳化钙固定而生成氰氨化钙(CaCN2),为合成氨工业奠定了基础,从而促进了氨碱工业的全面发展,工业上制取纯碱的部分流程如图所示。
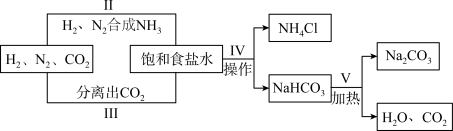
(3)氰氨化钙与水蒸气反应生成氨气和碳酸钙,该反应的化学方程式是______ 。
(4)碳酸氢钠只有在固态时,加热才会分解,则第Ⅳ步中操作的名称是______ 。
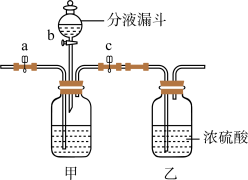
(5)实验室从 H2、N2、CO2的混合气体中分离出 CO2的实验装置如图所示。广口瓶甲和分液漏斗中盛放的药品分别是______ 溶液(填化学式)、稀硫酸。实验时先关闭活塞 b,打开止水夹 a 和 c,一段时间后,______ (填具体操作),就可以分离得到干燥的二氧化碳气体。
Ⅰ、工业制氨是以哈伯法通过氮气和氢气在高温高压和催化剂的作用下化合生成。实验室模拟合成氨气的流程如下:

(1)获取氮气:在特定装置内将空气液化,然后升温,先出来的气体就是氮气。该方法利用的原理是液氮和液氧的

(2)合成氨气:上述流程中氮气与氢气混合时最佳的质量比为
Ⅱ、1898 年德国人首次发现空气中的氮能被碳化钙固定而生成氰氨化钙(CaCN2),为合成氨工业奠定了基础,从而促进了氨碱工业的全面发展,工业上制取纯碱的部分流程如图所示。

(3)氰氨化钙与水蒸气反应生成氨气和碳酸钙,该反应的化学方程式是
(4)碳酸氢钠只有在固态时,加热才会分解,则第Ⅳ步中操作的名称是
(5)实验室从 H2、N2、CO2的混合气体中分离出 CO2的实验装置如图所示。广口瓶甲和分液漏斗中盛放的药品分别是

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量其他杂质)生产医药级二水合氯化钙的主要流程如下:
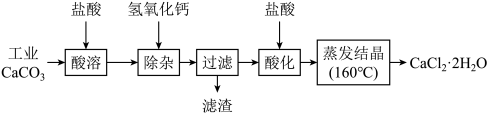
(1)写出“酸溶”发生反应的化学方程式__________________ 。
(2)“除杂”时氢氧化钙不能加入过多,原因是___________________ 。
(3)“过滤”和“蒸发”都需要用的玻璃仪器是__________ 。
(4)CaCl2和浓硫酸都具有吸水性,从安全.环保角度,生活中选择_________ (写物质名称)做除湿剂。

(1)写出“酸溶”发生反应的化学方程式
(2)“除杂”时氢氧化钙不能加入过多,原因是
(3)“过滤”和“蒸发”都需要用的玻璃仪器是
(4)CaCl2和浓硫酸都具有吸水性,从安全.环保角度,生活中选择
您最近一年使用:0次
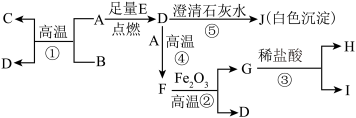
【推荐3】实验是学习化学的一条重要途径。请回答问题:
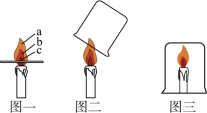
(1)如图一,观察到蜡烛燃烧时火焰分为a、b、c三层,其中温度最高的是_______ (填字母序号)。
(2)如图二,取一个冷而干燥的小烧杯罩在火焰上方,观察到烧杯内壁出现____ ,快速倒转烧杯,倒入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊。由此可知,蜡烛燃烧后的产物一定有H2O和____ (填化学式)。
(3)如果用一个大烧杯扣住蜡烛(如图三),一段时间后,观察到蜡烛熄灭,说明燃烧需要_______ 
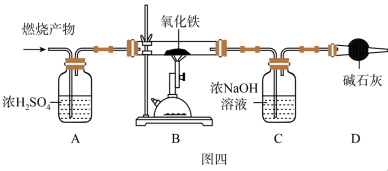
(4)为测定某有机物的组成(如图四),往装置中先通入一段时间干燥的氮气,再将6.4g样品在氧气中燃烧后的产物(样品无剩余)依次通过装置A、B、C、D(装置中涉及的每步反应均反应完全),结果发现装置A增重7.2g,装置C增重8.8g。试分析:
①装置A中利用了浓硫酸的_______ 。
②装置B中红色粉末变成黑色的原因是_______ (用化学方程式表示)。
③装置C中反应的化学方程式为_______ 。


(1)如图一,观察到蜡烛燃烧时火焰分为a、b、c三层,其中温度最高的是
(2)如图二,取一个冷而干燥的小烧杯罩在火焰上方,观察到烧杯内壁出现
(3)如果用一个大烧杯扣住蜡烛(如图三),一段时间后,观察到蜡烛熄灭,说明燃烧需要

(4)为测定某有机物的组成(如图四),往装置中先通入一段时间干燥的氮气,再将6.4g样品在氧气中燃烧后的产物(样品无剩余)依次通过装置A、B、C、D(装置中涉及的每步反应均反应完全),结果发现装置A增重7.2g,装置C增重8.8g。试分析:
①装置A中利用了浓硫酸的
②装置B中红色粉末变成黑色的原因是
③装置C中反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】乙炔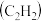 是有机合成的重要原料。以电石
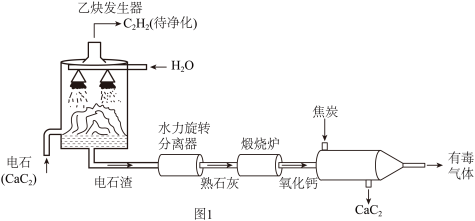
是有机合成的重要原料。以电石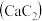 为原料制取乙炔,并对电石渣综合处理的生产流程如图1所示:
为原料制取乙炔,并对电石渣综合处理的生产流程如图1所示:
 电石
电石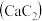 中碳元素的化合价是
中碳元素的化合价是______ 。
 乙炔发生器内发生反应的化学方程式为
乙炔发生器内发生反应的化学方程式为______ 。
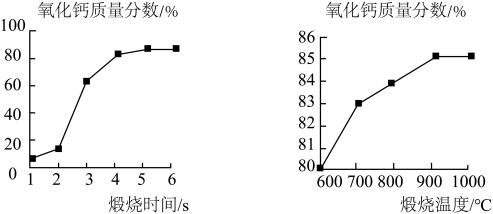
 研究煅烧炉内氧化钙含量的变化有如图2所示的结果,如果你是工作人员,你对煅烧条件的把控是
研究煅烧炉内氧化钙含量的变化有如图2所示的结果,如果你是工作人员,你对煅烧条件的把控是______ 。
 该生产过程的尾气不能直接排放,你的建议是
该生产过程的尾气不能直接排放,你的建议是______ 。
 流程图中能循环利用的物质是
流程图中能循环利用的物质是______ 。
 若将电石长期露置于空气中,会发生一系列变化,最终所得固体中一定含有的物质是
若将电石长期露置于空气中,会发生一系列变化,最终所得固体中一定含有的物质是______ 。
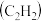 是有机合成的重要原料。以电石
是有机合成的重要原料。以电石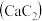 为原料制取乙炔,并对电石渣综合处理的生产流程如图1所示:
为原料制取乙炔,并对电石渣综合处理的生产流程如图1所示:

 电石
电石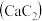 中碳元素的化合价是
中碳元素的化合价是 乙炔发生器内发生反应的化学方程式为
乙炔发生器内发生反应的化学方程式为 研究煅烧炉内氧化钙含量的变化有如图2所示的结果,如果你是工作人员,你对煅烧条件的把控是
研究煅烧炉内氧化钙含量的变化有如图2所示的结果,如果你是工作人员,你对煅烧条件的把控是 该生产过程的尾气不能直接排放,你的建议是
该生产过程的尾气不能直接排放,你的建议是 流程图中能循环利用的物质是
流程图中能循环利用的物质是 若将电石长期露置于空气中,会发生一系列变化,最终所得固体中一定含有的物质是
若将电石长期露置于空气中,会发生一系列变化,最终所得固体中一定含有的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】 久置的苛性钠溶液易发生变质,反应的化学方程式为:_______________________ 。如果要检验苛性钠溶液是否变质,可取出少量溶液于试管,向其中滴加 _____________________ ,则证明已经变质。此反应的化学方程式为:_______________________ 。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】实验室有一瓶含有难溶性杂质的粗盐样品,其中还含有少量的氯化镁和氯化钙。为了得到较纯净的食盐晶体,同学们先将粗盐加水制成粗盐水,后设计如下实验方案:
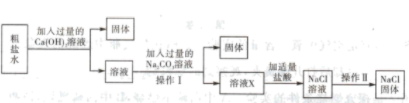
(1)写出加入过量的Ca(OH)2溶液时发生反应的化学方程式:___________ 。
(2)操作Ⅱ进行的操作是___________ 。
(3)向溶液中加入过量的碳酸钠溶液的目的是___________ 。
(4)向溶液X中加入过量的盐酸是否可以?
(5)设计实验证明溶液X混有的杂质成分。

(1)写出加入过量的Ca(OH)2溶液时发生反应的化学方程式:
(2)操作Ⅱ进行的操作是
(3)向溶液中加入过量的碳酸钠溶液的目的是
(4)向溶液X中加入过量的盐酸是否可以?
(5)设计实验证明溶液X混有的杂质成分。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】实验小组发现,隔段时间做实验用的澄清石灰水表面产生了一层“白膜”。
(1)此“白膜”的主要成分是______ ;
(2)对该溶液是否全部变质,同学们提出的假设有:
假设一:该溶液部分变质 假设二:该溶液全部变质
请你设计实验方案进行探究(需要写出实际步骤和现象,得出结论)____ 。
(1)此“白膜”的主要成分是
(2)对该溶液是否全部变质,同学们提出的假设有:
假设一:该溶液部分变质 假设二:该溶液全部变质
请你设计实验方案进行探究(需要写出实际步骤和现象,得出结论)
您最近一年使用:0次