铜生锈后所得物质为碱式碳酸铜[Cu2(OH)2CO3].受热分解生成氧化铜、水和二氧化碳,反应的化学方程式为______ ; 充分加热30g含氧化铜的碱式碳酸铜固体。若反应前后固体中铜元素的质量分数之比为5:6,则该反应生成水和二氧化碳的质量之和为______g。
更新时间:2020-04-08 10:26:32
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】食品加工厂在制作馒头等面食时,经常会用到食用小苏打。与工业制取碳酸氢钠不同,食用小苏打是由纯碱溶液和二氧化碳反应制得:CO2 + H2O + Na2CO3=2NaHCO3。某温度下,向121.2g碳酸钠溶液中通入一定量的CO2至碳酸钠恰好完全反应,反应后的溶液中有碳酸氢钠析出,过滤,分别得到23.96g固体和106.04 g溶液。请计算:
(1)参与反应的CO2质量。
(2)过滤后的溶液中,碳酸氢钠与水的质量比。
(1)参与反应的CO2质量。
(2)过滤后的溶液中,碳酸氢钠与水的质量比。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100g溶液,将其全部加入到100g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部溢出后,所得溶液质量是195.6g,将溶液蒸干,得到15.6g硫酸钠.请你计算:
(1)生成气体的质量为 ;
(2)加入的硫酸溶液的溶质质量分数;
(3)原碳酸钠样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%).
(1)生成气体的质量为 ;
(2)加入的硫酸溶液的溶质质量分数;
(3)原碳酸钠样品中碳酸钠的质量分数(写出计算过程,计算结果精确到0.1%).
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】阳春鱼产丰富,鱼骨可用于补钙和做饲料。某项目化学习小组准备用图甲实验装置测定鱼骨中的碳酸钙含量,进而测定其中钙的含量。其操作如下:
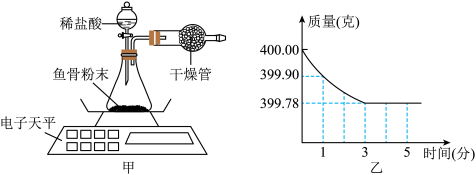
提示:假设鱼骨中只有碳酸钙与盐酸反应产生的气体;生成的二氧化碳气体全部逸出锥形瓶;空气成分对实验的影响忽略不计。
碳酸钙和盐酸反应的化学方程式为: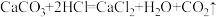 。
。
I.加入药品:在锥形瓶中加入40克鱼骨粉末,往分液漏斗中加足量的稀盐酸;
Ⅱ.记录数据:打开活塞加入稀盐酸,每隔10秒记录天平读数,并将测得的数据绘制成图(图乙)。
Ⅲ.计算:
(1)根据上述数据可知,在分钟时,实验恰好完全反应,放出气体质量为_____________ 克。
(2)根据上述实验数据计算鱼骨样品中碳酸钙的质量。(写出计算过程)
(3)鱼骨样品中Ca元素的质量分数为_______________ 。
(4)查资料得:鱼骨中钙元素的质量分数为14%-25%。而按照上述实验计算出来的结果远小于资料中的14%-25%,请你写出可能的一种原因_______________ 。

提示:假设鱼骨中只有碳酸钙与盐酸反应产生的气体;生成的二氧化碳气体全部逸出锥形瓶;空气成分对实验的影响忽略不计。
碳酸钙和盐酸反应的化学方程式为:
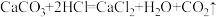 。
。I.加入药品:在锥形瓶中加入40克鱼骨粉末,往分液漏斗中加足量的稀盐酸;
Ⅱ.记录数据:打开活塞加入稀盐酸,每隔10秒记录天平读数,并将测得的数据绘制成图(图乙)。
Ⅲ.计算:
(1)根据上述数据可知,在分钟时,实验恰好完全反应,放出气体质量为
(2)根据上述实验数据计算鱼骨样品中碳酸钙的质量。(写出计算过程)
(3)鱼骨样品中Ca元素的质量分数为
(4)查资料得:鱼骨中钙元素的质量分数为14%-25%。而按照上述实验计算出来的结果远小于资料中的14%-25%,请你写出可能的一种原因
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】如图为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:___________ ;
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式___________ ﹔
(3)钙片中钙元素的质量分数___________ ;
(4)若工厂要生产含杂质44%的生石灰200t,理论上需要碳酸钙的质量为___________ 。
(5)若有碳酸钙和碳酸钠的固体混合物75g,使之与含HCl173g的盐酸充分反应,将反应后的溶液蒸干得到82.7g固体。则混合物中金属元素的质量分数为________
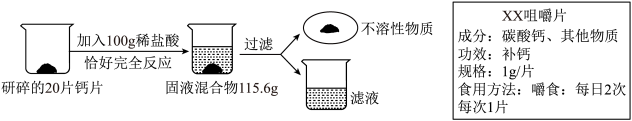
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式
(3)钙片中钙元素的质量分数
(4)若工厂要生产含杂质44%的生石灰200t,理论上需要碳酸钙的质量为
(5)若有碳酸钙和碳酸钠的固体混合物75g,使之与含HCl173g的盐酸充分反应,将反应后的溶液蒸干得到82.7g固体。则混合物中金属元素的质量分数为________
| A.40% | B.44% | C.50% | D.55% |
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】某同学为了研究生石灰CaO露置于空气中变质情况,设计如下实验:
取10克生石灰 粉末A质量为12克
粉末A质量为12克 气体B
气体B 沉淀质量为2.5克。请通过分析计算:
沉淀质量为2.5克。请通过分析计算:
(1)生成气体B的质量为_____.
(2)粉末A中CaCO3的质量为_____,这些CaCO3是由_____克CaO转化而来的.
(3)粉末A的成分除CaO外还有_____.(写化学式)
(4)粉末A中CaO的质量分数是多少_____?
取10克生石灰
 粉末A质量为12克
粉末A质量为12克 气体B
气体B 沉淀质量为2.5克。请通过分析计算:
沉淀质量为2.5克。请通过分析计算:(1)生成气体B的质量为_____.
(2)粉末A中CaCO3的质量为_____,这些CaCO3是由_____克CaO转化而来的.
(3)粉末A的成分除CaO外还有_____.(写化学式)
(4)粉末A中CaO的质量分数是多少_____?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】水垢可以看作由多种物质组成的混合物,化学组成可表示为aCaCO3·bMg(OH)2·nH2O或aCaCO3·bMg(OH)2·cMgCO3·nH2O。为研究某锅炉水所形成水垢的化学组成,取水垢6.32g,加热使其失去结晶水,得到5.78g剩余固体A。高温灼烧A至恒重,放出的气体若用过量的Ba(OH)2溶液吸收,得到11.82g沉淀;若被碱石灰完全吸收,碱石灰增重2.82克。
(1)写出高温灼烧固体A时所发生反应的化学方程式:___________ ;__________ (写出任意正确的两个)
(2)通过计算判断该水垢中是否含有MgCO3______________ (填“有”或“无”)。
(3)计算固体A中Mg(OH)2的质量是_______ g。
(1)写出高温灼烧固体A时所发生反应的化学方程式:
(2)通过计算判断该水垢中是否含有MgCO3
(3)计算固体A中Mg(OH)2的质量是
您最近一年使用:0次



