真题
解题方法
1 . 如图为金属钠与氯气反应生成氯化钠的示意图,下列说法错误 的是

| A.每个氯离子带一个单位负电荷 |
| B.钠原子在该反应中形成了阴离子 |
| C.氯化钠是由钠离子和氯离子构成的 |
| D.钠离子和氯离子的结构都相对稳定 |
您最近一年使用:0次
真题
解题方法
2 . 为测定某过氧化氢溶液的溶质质量分数,实验中记录的相关数据如表。
请计算:
(1)表中氧气的质量为_______ g。
(2)该过氧化氢溶液的溶质质量分数。(温馨提示: )
)
| 反应前物质的质量 | 完全反应后物质的质量 | ||
| 过氧化氢溶液质量 | 二氧化锰质量 | 固体与液体混合物质量 | 氧气质量 |
| 34.0g | 0.1g | 33.3g | _______g |
(1)表中氧气的质量为
(2)该过氧化氢溶液的溶质质量分数。(温馨提示:
 )
)
您最近一年使用:0次
真题
解题方法
3 . 新能源的开发和利用促进了能源结构向多元、清洁和低碳转变。
(1)目前,人类利用的能量大多来自化石燃料,如石油、天然气和______ 。在有石油的地方,一般都有天然气存在,天然气的主要成分是甲烷,其化学式为______ 。
(2)做饭时,天然气燃烧不充分,锅底易出现黑色物质,此时可调______ (填“小”或“大”)燃气灶的进风口,使燃料充分燃烧,节约能源。
(3)我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。______ 不变。
②过程I中反应生成的另外一种物质为生活中常见的氧化物,该反应的化学方程式为______ 。
(4)随着科学技术的发展,氢能源的开发利用已取得很大进展。氢气作为燃料的优点是______ (答一点即可)。
(1)目前,人类利用的能量大多来自化石燃料,如石油、天然气和
(2)做饭时,天然气燃烧不充分,锅底易出现黑色物质,此时可调
(3)我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。
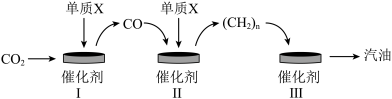
②过程I中反应生成的另外一种物质为生活中常见的氧化物,该反应的化学方程式为
(4)随着科学技术的发展,氢能源的开发利用已取得很大进展。氢气作为燃料的优点是
您最近一年使用:0次
真题
解题方法
4 . 某同学自制的简易净水器如图所示,下列说法错误 的是
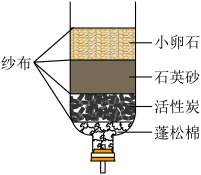
| A.活性炭可吸附水中的色素和异味 |
| B.该装置可除去泥沙等难溶性杂质 |
| C.该装置净水过程发生了化学变化 |
| D.河水经该装置净化后仍是混合物 |
您最近一年使用:0次
真题
5 . 在课外实践活动中,同学们学习了豆腐的制作,主要流程如图。
(1)黄豆是制作豆腐的主要原料,表中是某黄豆的主要营养成分信息,其中含量最高的是_______(填序号)。
【反思总结】同学们经过多次实验,发现以下因素会影响豆腐出品率(制得豆腐与所用黄豆的质量百分比)。
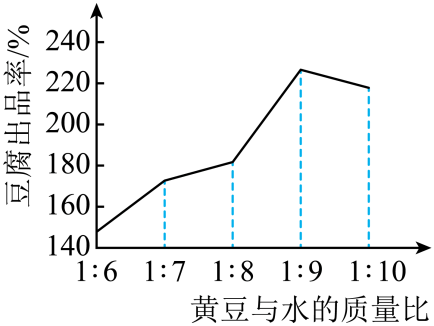
(2)磨浆时黄豆与水的质量比
实验后,同学们绘制如图图像。由图可知,磨浆时黄豆与水的质量比为_______ 时,豆腐出品率最高。
①有同学认为“凝固剂与黄豆的质量百分比越大,豆腐出品率越高”,根据表中数据分析,这一观点______ (填“正确”或“错误”)。
②把卤水(凝固剂与水的混合物)均匀分散到豆浆中,需进行的操作是_______ 。
【拓展延伸】实践基地的凝固剂有CaSO4和MgCl2,本次实践使用的是哪一种?
【查阅资料】20℃时,CaSO4的溶解度是0.255g,MgCl2的溶解度是54.6g。
【进行实验】20℃时,取1g凝固剂于试管中,加入10g水,充分振荡,完全溶解。
【实验结论】
(4)本次使用的凝固剂是_______ (填化学式)。请写出一个能生成该凝固剂的化学方程式______ 。
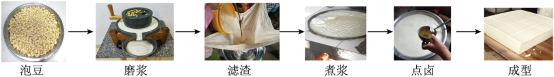
(1)黄豆是制作豆腐的主要原料,表中是某黄豆的主要营养成分信息,其中含量最高的是_______(填序号)。
| 营养成分 | 糖类 | 蛋白质 | 油脂 | 水 |
| 每100g含 | 37.3g | 33.1g | 15.9g | 9.2g |
| A.糖类 | B.蛋白质 | C.油脂 | D.水 |
【反思总结】同学们经过多次实验,发现以下因素会影响豆腐出品率(制得豆腐与所用黄豆的质量百分比)。
(2)磨浆时黄豆与水的质量比
实验后,同学们绘制如图图像。由图可知,磨浆时黄豆与水的质量比为
| 实验序号 | 凝固剂与黄豆的质量百分比 | 豆腐出品率 |
| 1 | 1.5% | 点卤后形成豆花少,豆腐压制不成型 |
| 2 | 2.0% | 豆腐出品率270% |
| 3 | 2.5% | 豆腐出品率217% |
| 4 | 3.0% | 豆腐出品率213% |
| 5 | 3.5% | 点卤后形成豆花较碎,豆腐不易压制成型 |
②把卤水(凝固剂与水的混合物)均匀分散到豆浆中,需进行的操作是
【拓展延伸】实践基地的凝固剂有CaSO4和MgCl2,本次实践使用的是哪一种?
【查阅资料】20℃时,CaSO4的溶解度是0.255g,MgCl2的溶解度是54.6g。
【进行实验】20℃时,取1g凝固剂于试管中,加入10g水,充分振荡,完全溶解。
【实验结论】
(4)本次使用的凝固剂是
您最近一年使用:0次
真题
解题方法
6 . 氨气(NH3)是制取硝酸的主要原料,其中H的化合价为+1价,则N的化合价为
| A.-3 | B.-1 | C.+1 | D.+3 |
您最近一年使用:0次
7 . 某溶液可能含有HCl、CuCl2、CuSO4中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列说法正确的是
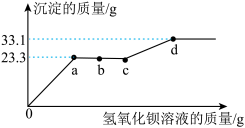
| A.d点后,溶液的pH保持不变 |
| B.b点对应的溶液中有三种溶质 |
| C.c点到d点的过程中,溶液中溶质总质量在减少 |
| D.原溶液含有HCl、CuCl2和CuSO4 |
您最近一年使用:0次
真题
解题方法
8 . 铜是重要的金属资源,它对于改善人类生活、促进人类文明起着重要作用。
(1)铜的认识:生活中常用铜作导线,体现了铜的延展性和______ 性。
(2)铜的冶炼:黄铜矿的主要成分是CuFeS2,根据其主要成分的组成元素,推断用黄铜矿炼铜过程中产生形成酸雨的空气污染物是_______ (填化学式)。
(3)铜的加工:青铜是金属冶铸史上最早的合金,其主要成分是铜和锡。表中的A和B分别表示铜和青铜中的一种。《吕氏春秋》记载:“金(铜)柔锡柔,合两柔则刚”,据此判断A是_______ 。
注:硬度以金刚石的硬度为10作标准,1表示很软,10表示很硬
(4)铜的锈蚀:铜在潮湿的空气中锈蚀的反应为2Cu+O2+H2O+X=Cu2(OH)2CO3,X的化学式为_______ 。
(5)铜的回收:某工厂的废水经预处理后得到含FeSO4和CuSO4的溶液。为了减少污染并促进废物利用,工厂设计以下流程回收Cu和FeSO4。_______ 。
②溶液C中的溶质是_______ 。
(1)铜的认识:生活中常用铜作导线,体现了铜的延展性和
(2)铜的冶炼:黄铜矿的主要成分是CuFeS2,根据其主要成分的组成元素,推断用黄铜矿炼铜过程中产生形成酸雨的空气污染物是
(3)铜的加工:青铜是金属冶铸史上最早的合金,其主要成分是铜和锡。表中的A和B分别表示铜和青铜中的一种。《吕氏春秋》记载:“金(铜)柔锡柔,合两柔则刚”,据此判断A是
| 物质 | A | B |
| 硬度 | 2.5-3 | 5-6.6 |
(4)铜的锈蚀:铜在潮湿的空气中锈蚀的反应为2Cu+O2+H2O+X=Cu2(OH)2CO3,X的化学式为
(5)铜的回收:某工厂的废水经预处理后得到含FeSO4和CuSO4的溶液。为了减少污染并促进废物利用,工厂设计以下流程回收Cu和FeSO4。
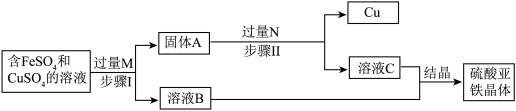
②溶液C中的溶质是
您最近一年使用:0次
真题
解题方法
9 . 酸、碱、盐是几类重要化合物,与人类日常生活和生产关系十分密切。
(1)现有以下三种物质:
A.盐酸 B.氢氧化钠 C.氯化钠
①可用于金属表面除锈的是______ (填序号,下同);可用作调味品的是_______ ;可用作某些气体的干燥剂的是______ 。
②分别取上述三种物质的溶液于三支试管中,用一种试剂分别滴加到试管中就能将三种物质鉴别出来,这种试剂是______ 。
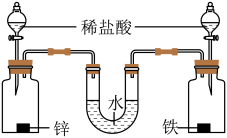
(2)兴趣小组按如图所示装置(气密性良好)进行实验。两个广口瓶中分别放有0.2g锌和铁,U形管两端液面相平,将等体积的足量稀盐酸同时加入广口瓶中,关闭活塞。反应结束,恢复至室温,U形管两端液面_______ (填“左高右低”“左低右高”或“相平”)。_______ ,于是增加如下对照实验:重复上述实验①,再加入2mL_______ ,充分振荡,观察到_______ ,最终证明了稀盐酸能和氢氧化钙发生反应。
(1)现有以下三种物质:
A.盐酸 B.氢氧化钠 C.氯化钠
①可用于金属表面除锈的是
②分别取上述三种物质的溶液于三支试管中,用一种试剂分别滴加到试管中就能将三种物质鉴别出来,这种试剂是
(2)兴趣小组按如图所示装置(气密性良好)进行实验。两个广口瓶中分别放有0.2g锌和铁,U形管两端液面相平,将等体积的足量稀盐酸同时加入广口瓶中,关闭活塞。反应结束,恢复至室温,U形管两端液面
您最近一年使用:0次
真题
解题方法
10 . 密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表所示。下列说法错误 的是
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 2.8 | 1 | 16 | 10 |
| 反应后的质量/g | 0 | 9.8 | 6.4 | a |
| A.a=13.6 | B.甲和丙为反应物 |
| C.该反应是化合反应 | D.甲、乙发生改变的质量比为7:22 |
您最近一年使用:0次



