名校
解题方法
1 . 化学是在分子、原子的层次上研究物质的组成、结构、性质以及变化规律的科学。运用比较、归类等方法学习化学,可以起到事半功倍的作用。
(1)现有“二氧化碳、氧气、铜、过氧化氢、氖气、氯化氢”六种物质,请根据物质的类别将它们平均分为两类。选出的物质有:___________ (填化学符号),分类依据___________ ;
(2)氯化钠是由带相反电荷的___________ 相互作用形成的化合物,它属于离子化合物。而氯化氢的形成过程则不同,氢原子和氯原子都趋向于得到电子,氢原子和氯原子先构成氯化氢分子,很多氯化氢分子聚集成氯化氢。像氯化氢这样的化合物属于共价化合物。根据以上信息分析,下列物质中属于共价化合物的是___________ (填字母)。
A.NaF B.SO2 C.LiCl
(1)现有“二氧化碳、氧气、铜、过氧化氢、氖气、氯化氢”六种物质,请根据物质的类别将它们平均分为两类。选出的物质有:
(2)氯化钠是由带相反电荷的
A.NaF B.SO2 C.LiCl
您最近一年使用:0次
2022-12-05更新
|
35次组卷
|
2卷引用:黑龙江省哈尔滨市南岗区第十七中学校2020-2021学年九年级上学期12月月考化学试题
名校
2 . 中美贸易战之际,5月17日华为公司宣布“备胎”芯片转正,正式回击了美国的打压,有力地佐证了我国在科技、文化等方面的创新与发展魄力。
(1)硅是计算机芯片的基体材料,但其导热性不好,而金刚石(C)在导热性方面远超过硅。
①从物质分类上看,金刚石和硅都属于_____ ;硅与金刚石结构相似,则构成硅的粒子是_____ (填粒子名称);下面四种粒子的结构示意图中,与硅化学性质相似的是_____ (填序号)

②天然金刚石资源稀少,人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨(C)为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷等为原料制造金刚石薄膜。下列判断不正确的是_____ (写字母序号)。
A 一种元素可以组成多种性质不同的单质
B 石墨与金刚石物理性质不同是因为原子排列方式不同
C 石墨合成金刚石发生的是物理变化
D 物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
(2)高纯硅的制备以石英砂(主要是硅的氧化物)为原料,生产过程示意图如下:

上述四个步骤中生成的M是一种化合物,其化学式为_____ 。
(1)硅是计算机芯片的基体材料,但其导热性不好,而金刚石(C)在导热性方面远超过硅。
①从物质分类上看,金刚石和硅都属于

②天然金刚石资源稀少,人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨(C)为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷等为原料制造金刚石薄膜。下列判断不正确的是
A 一种元素可以组成多种性质不同的单质
B 石墨与金刚石物理性质不同是因为原子排列方式不同
C 石墨合成金刚石发生的是物理变化
D 物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
(2)高纯硅的制备以石英砂(主要是硅的氧化物)为原料,生产过程示意图如下:

上述四个步骤中生成的M是一种化合物,其化学式为
您最近一年使用:0次
3 . 科学方法对化学学习起着事半功倍的作用.
(1)分类归纳是研究化学物质的重要方法.如图1是某同学整理的铁及其化合物的知识网络图.
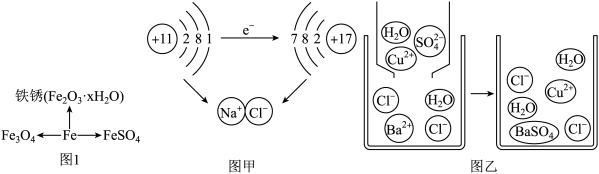
①铁丝燃烧生成Fe3O4的过程中___ (选填“放出”或“吸收”)热量.
②铁制品的锈蚀过程,实际上是铁与空气中的___ 等发生化学反应的过程.
③与FeSO4中铁元素化合价相同的铁氧化物的化学式是___ .
(2)微观粒子模型化是研究化学变化的重要方法. ①图甲是钠与氯气反应生成氯化钠的示意图.该图说明在化学反应过程中一定发生变化的是___ . (填字母)
a.原子核 b.原子核最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应示意图.从粒子角度分析该化学反应能发生的原因是___ .
(3)控制变量、设计对比实验是实验探究的重要方法.
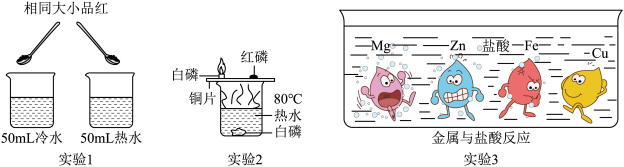
①实验1中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水闭冷水短.这是因为___ .
②实验2中使用铜片是为了对比___ 不同.
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体.下列结论不正确的是___ (填字母).
a.铜不能发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe多.
(1)分类归纳是研究化学物质的重要方法.如图1是某同学整理的铁及其化合物的知识网络图.

①铁丝燃烧生成Fe3O4的过程中
②铁制品的锈蚀过程,实际上是铁与空气中的
③与FeSO4中铁元素化合价相同的铁氧化物的化学式是
(2)微观粒子模型化是研究化学变化的重要方法. ①图甲是钠与氯气反应生成氯化钠的示意图.该图说明在化学反应过程中一定发生变化的是
a.原子核 b.原子核最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应示意图.从粒子角度分析该化学反应能发生的原因是
(3)控制变量、设计对比实验是实验探究的重要方法.

①实验1中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水闭冷水短.这是因为
②实验2中使用铜片是为了对比
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体.下列结论不正确的是
a.铜不能发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe多.
您最近一年使用:0次
名校
解题方法
4 . 化学是一门富有创造性的科学。含氟物质的合成,对推动社会进步发挥着巨大作用.
(1)如图是氟元素在元素周期表中的相关信息,画出氟元素的原子结构示意图______ ,由氟原子的结构示意图知,氟原子在化学反应中易_______ (填“失”或“得”)电子。

(2)氟化钠常用作牙膏添加剂,能有效预防龋齿。氟化钠和氯化钠一样,都是由______ (填“分子”、“原子”或“离子”)构成。
(3)被誉为“塑料王”的聚四氟乙烯,常用不粘锅锅底涂层,它的化学性质非常稳定,不与油、盐、醋等反应.从材料分类角度看,塑料是一类______ 材料,从人体所需营养素角度看,油、盐、醋中的“盐”指的是______ 。
(1)如图是氟元素在元素周期表中的相关信息,画出氟元素的原子结构示意图

(2)氟化钠常用作牙膏添加剂,能有效预防龋齿。氟化钠和氯化钠一样,都是由
(3)被誉为“塑料王”的聚四氟乙烯,常用不粘锅锅底涂层,它的化学性质非常稳定,不与油、盐、醋等反应.从材料分类角度看,塑料是一类
您最近一年使用:0次
解题方法
5 . 在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。图是元素周期表的一部分,根据表格回答问题 :
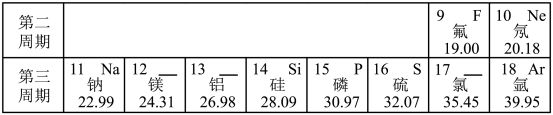
(1)地壳中含量最多的金属元素是______ (写元素符号),该原子最外层电子数为______ 。
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为______ 。
(3)第三周期中具有相对稳定结构的原子的原子序数为______ 。
(4)当11号元素与17号元素组成物质时,构成此物质的阳离子的符号为______ 。
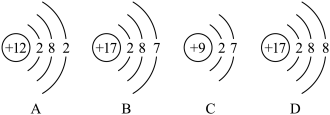
(5)图所示的微粒中,属于同种元素的是______ (填序号),元素的化学性质相似的是______ (填序号)。

(1)地壳中含量最多的金属元素是
(2)地壳中硅元素的含量仅次于氧元素,硅元素的相对原子质量为
(3)第三周期中具有相对稳定结构的原子的原子序数为
(4)当11号元素与17号元素组成物质时,构成此物质的阳离子的符号为
(5)图所示的微粒中,属于同种元素的是

您最近一年使用:0次
解题方法
6 . 下图是元素周期表的一部分,请回答相关问题:
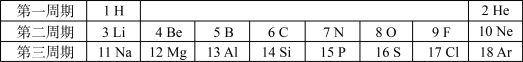
(1)碳元素与硅元素位于同一纵行的原因是____ 。铝元素与氯元素形成化合物的化学式是____ 。
(2)在化学反应中,锂元素的原子容易___ (填“得到”或“失去”,下同)电子,氟元素的原子容易____ 电子,二者形成化合物时,化学式是____ ,该物质常被用于核工业、搪瓷工业和光学玻璃制造业等。推测该化合物的构成微粒是____ 。(写出微粒符号)
(3)M2-与Ne核外电子排布相同,则M元素的名称为___ 。已知M元素的相对原子质量为a,则M元素原子核内的中子数为___ (用含a的代数式表示)。
(4)电镀行业中经常用到钛、钌(Ru)等贵金属。现有5种含钌元素的物质:Ru、RuO2、Ru2O3、RuCl3、K2RuO4.回答下列问题:
①RuO2读作____ 。
②从物质分类角度来看,K2RuO4属于___ 。(填选项)
A 化合物 B 单质 C 纯净物 D 混合物

(1)碳元素与硅元素位于同一纵行的原因是
(2)在化学反应中,锂元素的原子容易
(3)M2-与Ne核外电子排布相同,则M元素的名称为
(4)电镀行业中经常用到钛、钌(Ru)等贵金属。现有5种含钌元素的物质:Ru、RuO2、Ru2O3、RuCl3、K2RuO4.回答下列问题:
①RuO2读作
②从物质分类角度来看,K2RuO4属于
A 化合物 B 单质 C 纯净物 D 混合物
您最近一年使用:0次
解题方法
7 . 阅读下面科普短文。
钠是一种活泼金属,其原子结构示意图为: 。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物;可以制造合金,其中钠与汞的合金钠齐可用作有机合成的还原剂;还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生产钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物;可以制造合金,其中钠与汞的合金钠齐可用作有机合成的还原剂;还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生产钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)在钠的原子结构中,与钠元素化学性质密切相关的是_______ 。
(2)钠具有的物理性质有_______ 。
(3)从物质分类角度看,合金钠汞齐属于_______ (填“纯净物”或“混合物”)。
(4)金属钠通常保存在煤油中,目的是隔绝_______ 。
(5)写出用钠制取钾的化学方程式_______ 。
钠是一种活泼金属,其原子结构示意图为:
 。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物;可以制造合金,其中钠与汞的合金钠齐可用作有机合成的还原剂;还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生产钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物;可以制造合金,其中钠与汞的合金钠齐可用作有机合成的还原剂;还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生产钾和氯化钠,生成的钾能以蒸汽的形式分离出来。依据文章内容,回答下列问题:
(1)在钠的原子结构中,与钠元素化学性质密切相关的是
(2)钠具有的物理性质有
(3)从物质分类角度看,合金钠汞齐属于
(4)金属钠通常保存在煤油中,目的是隔绝
(5)写出用钠制取钾的化学方程式
您最近一年使用:0次
解题方法
8 . “宏观---微观---符号”三重表征是化学独特的表示物质及其变化的方法。
(1)锂电池是日常生活中常用的一种电池,如图是元素周期表中锂元素的相关信息。请回答下列问题:

①该元素原子最外层电子数为_____ , 在化学反应中容易___ (填“得到”或“失去”)电子成为锂离子。
②该元素与地壳中含量最多的元素组成的化合物的化学式是__________________ 。
③钠元素的原子结构示意图为 。钠与锂具有相似的化学性质,但钠更活泼。试分析解释其可能的原因:
。钠与锂具有相似的化学性质,但钠更活泼。试分析解释其可能的原因:
(2)某化学反应的微观示意图如下图所示:

①从微观构成看,四种物质均由___________ 构成。
②从物质分类看,该反应涉及到___________ 种氧化物。
③从表示方法看,该反应的化学方程式为______________ 。
(1)锂电池是日常生活中常用的一种电池,如图是元素周期表中锂元素的相关信息。请回答下列问题:

①该元素原子最外层电子数为
②该元素与地壳中含量最多的元素组成的化合物的化学式是
③钠元素的原子结构示意图为
 。钠与锂具有相似的化学性质,但钠更活泼。试分析解释其可能的原因:
。钠与锂具有相似的化学性质,但钠更活泼。试分析解释其可能的原因:(2)某化学反应的微观示意图如下图所示:

①从微观构成看,四种物质均由
②从物质分类看,该反应涉及到
③从表示方法看,该反应的化学方程式为
您最近一年使用:0次
解题方法
9 . 图1是部分元素的离子结构示意图和元素周期表的一部分,图2是某元素的相关信息。请回答:

(1)图1中属于阴离子的是___________ (填“①”或“②”),该元素的质子数为 ___________ 。13号元素原子的最外层电子数为 ___________ 。8号元素易 ___________ (填“得到”或“失去”)电子,所形成的离子符号是 ___________ 。
(2)13号元素位于第___________ 周期、它和5号元素的化学性质相似是因为 ___________ 。
(3)铱(Ir)是处于第六周期的一种元素,制笔行业中经常用到铱(Ir)等贵金属,现有六种含铱元素的物质Ir2O3、IrO2、Ir(OH)3、Ir(OH)4、IrCl3和IrCl4,请回答下列问题:
①Ir2O3读作___________ ;从物质分类角度来看,IrCl4属于 ___________ (填选项)
a.氧化物b.单质c.化合物d.混合物
②IrO2可在如热条件下被H2还原得到Ir,写出反应的化学反应方程式:___________ ;

(1)图1中属于阴离子的是
(2)13号元素位于第
(3)铱(Ir)是处于第六周期的一种元素,制笔行业中经常用到铱(Ir)等贵金属,现有六种含铱元素的物质Ir2O3、IrO2、Ir(OH)3、Ir(OH)4、IrCl3和IrCl4,请回答下列问题:
①Ir2O3读作
a.氧化物b.单质c.化合物d.混合物
②IrO2可在如热条件下被H2还原得到Ir,写出反应的化学反应方程式:
您最近一年使用:0次
解题方法
10 . 下列涉及学科观点的有关说法正确的是( )
| A.分类观:按物质组成成分的多少可以分为纯净物、混合物和化合物 |
| B.转化观:一氧化碳和二氧化碳在一定条件下可相互转化 |
| C.结构观:氖原子和氯离子最外层电子数相同,化学性质相同 |
| D.守恒观:化学反应前后分子数不变 |
您最近一年使用:0次



