解题方法
1 . 在疫情期间,人们很注重食品的营养搭配。鸡蛋中含有丰富的蛋白质,蛋白质是由丙氨酸(C3H7NO2)等多种氨基酸构成的。根据丙氨酸的化学式计算:
(1)丙氨酸的相对分子质量______。
(2)丙氨酸中碳、氢两种元素的质量比______。(写最简比)
(3)丙氨酸中______元素的质量分数最大。
(1)丙氨酸的相对分子质量______。
(2)丙氨酸中碳、氢两种元素的质量比______。(写最简比)
(3)丙氨酸中______元素的质量分数最大。
您最近一年使用:0次
解题方法
2 . 食用醋是厨房必备的调味品,其中约含4%的乙酸(CH3COOH)。按要求计算:
(1)乙酸中碳、氢、氧原子个数最简比为___________;
(2)乙酸的相对分子质量是___________;
(3)10 g乙酸中所含碳元素的质量为___________ g;
(4)一瓶500 mL的食用醋(密度为1 g/mL)中含乙酸的质量为___________ g。
(1)乙酸中碳、氢、氧原子个数最简比为___________;
(2)乙酸的相对分子质量是___________;
(3)10 g乙酸中所含碳元素的质量为___________ g;
(4)一瓶500 mL的食用醋(密度为1 g/mL)中含乙酸的质量为___________ g。
您最近一年使用:0次
解题方法
3 . 变化与守恒是化学学科的核心素养之一、结合下列相关内容回答问题。
(1)下列变化遵循质量守恒定律的是___________ 。
A 干冰升华后固体质量减轻
B 镁燃烧后所的固体质量增重
C 蔗糖溶液质量等于蔗糖质量与水的质量总和
D 锌放入稀硫酸中反应片刻后,烧杯内物质质量减轻
(2)在化学反应3Cu + 8HNO3 = 3Cu(NO3)2 + 4R + 2NO中,R的化学式为___________ 。
(3)某有机物6.0 g在空气中完全燃烧,生成17.6 g二氧化碳和10.8 g水,则:
① 该有机物中氢元素的质量为___________ ;
② 该有机物中一定含有的元素为___________ ;
③ 反应生成的二氧化碳和水的分子个数比为___________ 。
(4)二氧化碳和氢气在催化剂和加热的条件下生成乙烯(C2H4)和水。试写出该反应的化学方程式___________ 。
(1)下列变化遵循质量守恒定律的是
A 干冰升华后固体质量减轻
B 镁燃烧后所的固体质量增重
C 蔗糖溶液质量等于蔗糖质量与水的质量总和
D 锌放入稀硫酸中反应片刻后,烧杯内物质质量减轻
(2)在化学反应3Cu + 8HNO3 = 3Cu(NO3)2 + 4R + 2NO中,R的化学式为
(3)某有机物6.0 g在空气中完全燃烧,生成17.6 g二氧化碳和10.8 g水,则:
① 该有机物中氢元素的质量为
② 该有机物中一定含有的元素为
③ 反应生成的二氧化碳和水的分子个数比为
(4)二氧化碳和氢气在催化剂和加热的条件下生成乙烯(C2H4)和水。试写出该反应的化学方程式
您最近一年使用:0次
解题方法
4 . 红枣醋中含有一种酸(C4H6O5),具有解酒护肝健胃的作用。下列说法正确的是
| A.该酸中氢元素的质量分数最大 |
| B.该酸中氢、氧原子个数比为6:4 |
| C.该酸中碳、氢元素的质量比为8:1 |
| D.该酸是由碳、氢、氧元素组成的混合物 |
您最近一年使用:0次
解题方法
5 . 次氯酸钠(NaClO)和过氧化氢常用作消毒剂。下图和表是84消毒液的标签(部分)和过氧化氢消毒剂对循环冷却水中菌类杀菌效力的实验研究数据。

(1)84消毒液中,“有效氯含量”中的氯是指___________ (填“氯气”或“氯元素”)。
(2)NaClO中,质量分数最小的元素是___________ 。
(3)根据注意事项,说出一条84消毒液中物质的性质___________ 。
(4)NaClO和H2O2均属于___________ (填序号)。
A 单质 B 化合物 C 氧化物
(5)分析过氧化氢消毒剂杀菌实验数据,得出的结论是___________ 。
| 过氧化氢溶液浓度/mol▪L-1 | 3 | 5 | 10 | 10 | 10 |
| 时间/h | 0.5 | 1 | 0.5 | 1 | 2 |
| 真菌存活率/% | 85 | 63 | 38 | 13 | 3 |
| 亚硝菌存活率/% | 67 | 53 | 15 | 7 | 4 |

(1)84消毒液中,“有效氯含量”中的氯是指
(2)NaClO中,质量分数最小的元素是
(3)根据注意事项,说出一条84消毒液中物质的性质
(4)NaClO和H2O2均属于
A 单质 B 化合物 C 氧化物
(5)分析过氧化氢消毒剂杀菌实验数据,得出的结论是
您最近一年使用:0次
解题方法
6 . 偏二甲肼(C2H8N2)常做为液体火箭燃料,可在常温下保存、使用,具有更便捷的用途。计算:
(1)偏二甲肼的相对分子质量为______。
(2)偏二甲肼中碳、氢元素的质量比为______(写最简比);
(3)偏二甲肼中碳元素的质量分数为______。
(1)偏二甲肼的相对分子质量为______。
(2)偏二甲肼中碳、氢元素的质量比为______(写最简比);
(3)偏二甲肼中碳元素的质量分数为______。
您最近一年使用:0次
解题方法
7 . 科学家发现,利用催化剂可有效消除室内装修材料释放的有害气体甲醛(CH2O),其反应的微观示意图如下。下列说法中,正确的是( )
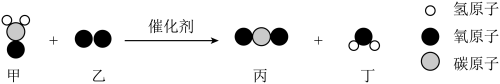

A.甲中碳元素的质量分数计算式为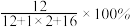 |
| B.丙中碳、氧元素质量比为1:2 |
| C.该反应属于置换反应 |
| D.反应前后分子个数改变 |
您最近一年使用:0次
解题方法
8 . 抗癌新药紫杉醇的化学式为C47H51NO4,回答下列问题:
(1)紫杉醇物质中含有_______种元素;
(2)紫杉醇物质中原子个数比为_______。
(3)紫杉醇中氮元素与氧元素的质量之比为_______(写出最简整数比);
(4)67.9g中紫杉醇中氢元素的质量为_______g。
(1)紫杉醇物质中含有_______种元素;
(2)紫杉醇物质中原子个数比为_______。
(3)紫杉醇中氮元素与氧元素的质量之比为_______(写出最简整数比);
(4)67.9g中紫杉醇中氢元素的质量为_______g。
您最近一年使用:0次
2021-04-30更新
|
179次组卷
|
3卷引用:2022年中考风向标-天津-化学计算
解题方法
9 . 甲醇(CH3OH)是一种重要的化工原料,利用废气中的二氧化碳可以制备甲醇。其原理:CO2 + 3H2 CH3OH + H2O
CH3OH + H2O
(1)H2O中氢元素的质量分数为11.1%,其计算式为_______。
(2)配制100 g质量分数为15%的甲醇溶液,需要甲醇的质量是_______g。
(3)计算制备32 kg甲醇,至少需要二氧化碳的质量是多少?(写出计算过程)
 CH3OH + H2O
CH3OH + H2O(1)H2O中氢元素的质量分数为11.1%,其计算式为_______。
(2)配制100 g质量分数为15%的甲醇溶液,需要甲醇的质量是_______g。
(3)计算制备32 kg甲醇,至少需要二氧化碳的质量是多少?(写出计算过程)
您最近一年使用:0次
名校
解题方法
10 . 无色硫酸铜为白色固体,硫酸铜晶体俗称胆矾或蓝矾(CuSO4·5H2O),为蓝色晶体,具有催吐,祛腐,解毒的作用。试计算:
(1)胆矾中原子个数比:Cu:S:O= 。
(2)胆矾的相对分子质量为 。
(3)若将25g胆矾溶于175g水中,得到溶液的溶质质量分数是 。
(1)胆矾中原子个数比:Cu:S:O= 。
(2)胆矾的相对分子质量为 。
(3)若将25g胆矾溶于175g水中,得到溶液的溶质质量分数是 。
您最近一年使用:0次



