2024·福建·模拟预测
解题方法
1 . 海水是宝贵的自然资源,实验小组以“海水”为主题展开项目式学习活动。
【任务一】海水淡化
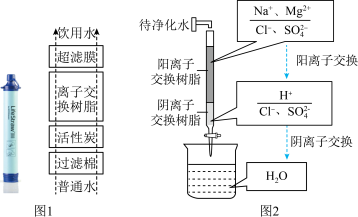
(1)某生命吸管可淡化海水,内部结构如图1,活性炭除去色素和异味利用了其___________ 性。___________ (填序号)。
a.降低 b.升高 c.不变
【任务二】深海固碳
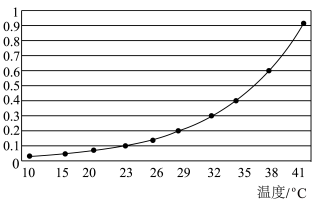
(3)海水吸收大量CO2,图3为北太平洋不同深度的海水中二氧化碳分压pCO2(CO2含量的一种表示方法),请分析在0~1000m水深范围内,pCO2随海水深度增加而增大的原因是___________ 。
中国工程院院士谢和平团队研制出了海水直接制氢新技术,原理如图4。
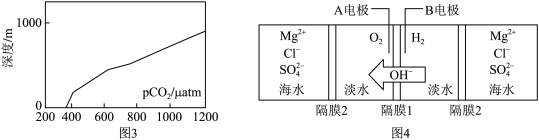
(4)海水制氢是将电能转化为___________ 能。
(5)A电极应与电源的___________ (填“正”或“负”)极相连。
【任务四】海水提镁
工业上从海水中提取单质镁的过程如图。___________ 。
(7)某工厂获得10吨含氯化镁95%的中间产品,理论上可获得单质镁的质量为___________ (结果精确到0.1)。
【任务一】海水淡化
(1)某生命吸管可淡化海水,内部结构如图1,活性炭除去色素和异味利用了其
a.降低 b.升高 c.不变
【任务二】深海固碳
(3)海水吸收大量CO2,图3为北太平洋不同深度的海水中二氧化碳分压pCO2(CO2含量的一种表示方法),请分析在0~1000m水深范围内,pCO2随海水深度增加而增大的原因是
中国工程院院士谢和平团队研制出了海水直接制氢新技术,原理如图4。
(4)海水制氢是将电能转化为
(5)A电极应与电源的
【任务四】海水提镁
工业上从海水中提取单质镁的过程如图。
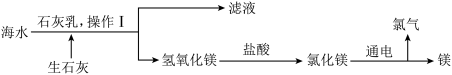
(7)某工厂获得10吨含氯化镁95%的中间产品,理论上可获得单质镁的质量为
您最近一年使用:0次
2024·福建·模拟预测
解题方法
2 . 阅读下面科普短文,依据短文回答问题
甲醛(HCHO),无色气体,有特殊的刺激气味,对人眼、鼻等有刺激作用。它是装修中不可避免的装修污染,它广泛存在于板材的粘合剂和其他的家具中,然后不断地挥发,给家居空间造成不同程度的污染。甲醛是原浆毒物,能与蛋白质中的胺基-NH2结合,使蛋白质性质发生改变,或称变性。当甲醛浓度在空气中达到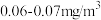 时,儿童就会发生轻微气喘;达到
时,儿童就会发生轻微气喘;达到 时,就有异味和不适感;达到
时,就有异味和不适感;达到 时,可刺激眼睛,引起流泪;达到
时,可刺激眼睛,引起流泪;达到 时,可引起咽喉不适或疼痛。浓度更高时,可引起恶心呕吐,咳嗽胸闷,气喘甚至肺水肿;达到
时,可引起咽喉不适或疼痛。浓度更高时,可引起恶心呕吐,咳嗽胸闷,气喘甚至肺水肿;达到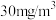 时,会立即致人死亡。因此,我国早已制定并执行着民用建筑环境污染物限量的标准(见表1)。
时,会立即致人死亡。因此,我国早已制定并执行着民用建筑环境污染物限量的标准(见表1)。
为减少甲醛等有害物质的伤害,首先要从控制污染源做起,减少接触甲醛的机会,由于甲醛释放时间非常久,最长能够达到15年,把控好建材和家具的品质至关重要。其次,释放甲醛。最有效的方法就是开窗通风,甲醛的挥发受温度影响很大(表2所示),因此,正确的做法是把门窗先关后开,关窗有利于升温,几天后再开窗会更好的让甲醛的气味消散出去。第三,吸收甲醛。利用绿萝、吊兰、常春藤等植物吸收;利用活性炭其内部发达的孔隙结构能够捕捉甲醛分子,降低室内空气中的甲醛浓度;利用央视推荐的紫加黑除甲醛,其氧化分解原理对甲醛较为有效,能够把甲醛分解为二氧化碳和水。
甲醛超标对家人的危害很大,装修新房时尽量简装修降低复合板材的使用度,根据甲醛的基本性质和合理除甲醛方法治理甲醛,只有室内甲醛低于国家标准才能够入住。
(1)甲醛由___________ 种元素组成。
(2)装修材料中的甲醛,由于具有___________ 性,弥漫在空气中,成为不可避免的家居装修污染物。
(3)甲醛对儿童、老人等影响最大,即使检测部门检测已达标的房间,儿童进入后也会发生轻微气喘,其原因___________ 。
(4)利用活性炭捕捉甲醛分子是利用了活性炭的___________ 性;活性炭和紫加黑除甲醛的本质区别是___________ (从微观角度进行说明)。
(5)下列有关甲醛的说法正确的是______。
甲醛(HCHO),无色气体,有特殊的刺激气味,对人眼、鼻等有刺激作用。它是装修中不可避免的装修污染,它广泛存在于板材的粘合剂和其他的家具中,然后不断地挥发,给家居空间造成不同程度的污染。甲醛是原浆毒物,能与蛋白质中的胺基-NH2结合,使蛋白质性质发生改变,或称变性。当甲醛浓度在空气中达到
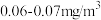 时,儿童就会发生轻微气喘;达到
时,儿童就会发生轻微气喘;达到 时,就有异味和不适感;达到
时,就有异味和不适感;达到 时,可刺激眼睛,引起流泪;达到
时,可刺激眼睛,引起流泪;达到 时,可引起咽喉不适或疼痛。浓度更高时,可引起恶心呕吐,咳嗽胸闷,气喘甚至肺水肿;达到
时,可引起咽喉不适或疼痛。浓度更高时,可引起恶心呕吐,咳嗽胸闷,气喘甚至肺水肿;达到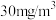 时,会立即致人死亡。因此,我国早已制定并执行着民用建筑环境污染物限量的标准(见表1)。
时,会立即致人死亡。因此,我国早已制定并执行着民用建筑环境污染物限量的标准(见表1)。| 民用建筑建筑工程室内环境污染物浓度限量 | |||
| 污染物 | I类 民用建筑工程 | II类民用建筑工程 |
|
| 氡(mg/m3) | ≦200 | ≦400 | |
| 甲醛(mg/m3) | ≦0.08 | ≦0.1 | |
| 苯(mg/m3) | ≦0.09 | ≦0.09 | |
| 氨(mg/m3) | ≦0.2 | ≦0.2 | |
| TVOC(mg/m3) | ≦0.5 | ≦0.6 | |
| 表1 | 表2 | ||
甲醛超标对家人的危害很大,装修新房时尽量简装修降低复合板材的使用度,根据甲醛的基本性质和合理除甲醛方法治理甲醛,只有室内甲醛低于国家标准才能够入住。
(1)甲醛由
(2)装修材料中的甲醛,由于具有
(3)甲醛对儿童、老人等影响最大,即使检测部门检测已达标的房间,儿童进入后也会发生轻微气喘,其原因
(4)利用活性炭捕捉甲醛分子是利用了活性炭的
(5)下列有关甲醛的说法正确的是______。
| A.甲醛不会对成年人造成任何伤害 |
| B.减少甲醛的危害,最重要的是要控制污染源,减少接触甲醛的机会 |
| C.每天开窗通风,并恒温在25℃,能够使甲醛很快释放完毕 |
| D.房间内栽培绿萝、吊兰等绿植,既美化环境,又可以吸收甲醛 |
您最近一年使用:0次
解题方法
3 . “物质的性质决定用途”是化学观念之一,下列物质的用途主要是由其化学性质决定的是
| A.氦气——填充探空气球 | B.金刚石——刻划玻璃 |
| C.熟石灰——改良酸性土壤 | D.硝酸铵——制作冰袋 |
您最近一年使用:0次
名校
解题方法
4 . 下列物质中只含有分子的是
| A.硫酸铜溶液 | B.镁铝合金 | C.医用酒精 | D.石墨 |
您最近一年使用:0次
解题方法
5 . 锂离子动力电池入选2023全球十大工程成就。
①图1中微观粒子c的名称是________ 。
②图2中“x”与图1中微观粒子________ (填“a”或“b”)的数量相等。
③锂元素的相对原子质量为________ 。
(2)锂离子动力电池负极材料以石墨为主,石墨、金刚石都是由_____ 组成的单质。
只含一种元素的物质________ (填“一定”或“不一定”)属于单质。
(3)2023年同济大学科研团队首次成功合成了环形纯碳分子(如图3所示),其化学式为________ 。
(4)锂离子动力电池充电过程中,主要是电能转化为____ 能。

①图1中微观粒子c的名称是
②图2中“x”与图1中微观粒子
③锂元素的相对原子质量为
(2)锂离子动力电池负极材料以石墨为主,石墨、金刚石都是由
只含一种元素的物质
(3)2023年同济大学科研团队首次成功合成了环形纯碳分子(如图3所示),其化学式为
(4)锂离子动力电池充电过程中,主要是电能转化为
您最近一年使用:0次
解题方法
6 . 学校安装的直饮水机工作原理如图所示,下列说法不正确的是

| A.活性炭可吸附色素与异味 |
| B.滤膜允许水分子通过 |
| C.紫外光照射的作用是消毒 |
| D.所得直饮水是纯净物 |
您最近一年使用:0次
7 . 五育并举,劳育先行。下列劳动项目涉及的化学原理及物质的性质不相符的是
| 选项 | 劳动项目 | 化学原理 | 物质性质 |
| A | 燃气灶做饭,锅底变黑,通过增大空气通风口来调节 | 增大空气(或氧气)通入量使甲烷充分燃烧 | 甲烷具有可燃性,氧气可支持燃烧 |
| B | 野外自制净水器中加入活性炭 | 活性炭可吸附色素和异味 | 活性炭具有吸附性 |
| C | 洗涤餐具时加入少量洗洁精 | 洗洁精可将油污分散成无数细小的液滴随水流冲走 | 洗洁精具有乳化性 |
| D | 用CO冶炼金属 | CO可以和金属氧化物反应得到金属单质 | CO具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列物质性质与用途相对应的是
| A.熟石灰能和酸发生中和反应,可用于配制农药波尔多液 |
| B.钛合金与人体具有较好的相容性,可用于航空业制造 |
| C.浓硫酸具有吸水性,可用作干燥剂 |
| D.金刚石是天然存在的最硬的物质,可以用来作装饰品 |
您最近一年使用:0次
名校
解题方法
9 . 下列选项中,符合化学学科核心素养的是
| A.创新与实践:用铁丝代替红磷测定空气中氧气的体积分数 |
| B.变化与守恒:化学反应前后,原子种类、质量与元素种类、质量均不变 |
| C.宏观与微观:金刚石和石墨中碳原子排列方式不同,所以它们的化学性质不同 |
| D.结构与性质:二氧化碳分子与一氧化碳分子由同种原子构成,所以它们的化学性质相同 |
您最近一年使用:0次
2024-05-09更新
|
85次组卷
|
2卷引用:福建省福州市第十九中学2023-2024学年九年级下学期期中考试化学试卷
10 . 和溶液与人类的生产、生活关系紧密。请回答下列问题:____________________ 。
(2)将硬水通过图1所示的阳离子交换柱后可变为软水(图中阴离子未画出),交换后的水仍然呈电中性。
①1个Ca2+可交换出__ 个Na+。
②阳离子交换柱长时间使用后,Na+变少,因失去软化硬水的功能而失效,利用生活中常见物质检验阳离子交换柱已失效的方法是____________________________________ 。
(3)20℃时打开汽水瓶盖,有大量气泡冒出。汽水瓶盖打开前后,CO2的溶解度由图2中的a点变化到__ (填“b”、“c”、“d”或“e”)点。
(4)已知KNO3和NaCl在不同温度时的溶解度如下表.
①20℃时,NaCl的溶解度为____ g。
②图3中表示KNO3溶解度曲线的是__ (填“甲”或“乙”)。
③KNO3溶液中混有少量NaCl时,可用________ (填“降温结晶”或“蒸发结晶”)的方法提纯KNO3。
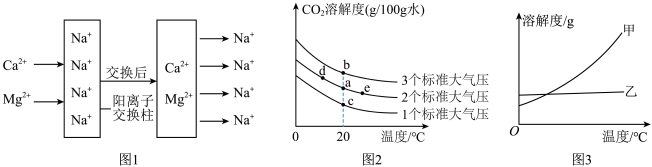
(2)将硬水通过图1所示的阳离子交换柱后可变为软水(图中阴离子未画出),交换后的水仍然呈电中性。
①1个Ca2+可交换出
②阳离子交换柱长时间使用后,Na+变少,因失去软化硬水的功能而失效,利用生活中常见物质检验阳离子交换柱已失效的方法是
(3)20℃时打开汽水瓶盖,有大量气泡冒出。汽水瓶盖打开前后,CO2的溶解度由图2中的a点变化到
(4)已知KNO3和NaCl在不同温度时的溶解度如下表.
温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | |
②图3中表示KNO3溶解度曲线的是
③KNO3溶液中混有少量NaCl时,可用
您最近一年使用:0次