解题方法
1 . 钨(W)是一种重要的战略资源。如图是一种生产钨的工业流程:
(1)操作1中粉碎白钨矿的作用是_______ 。
(2)操作3中发生的反应为2NH3•H2O+H2WO4=(NH4)2SO4+2X,X的化学式为_______ 。
(3)写出加入过量盐酸时发生的一个复分解反应的化学方程式:______ 。
(4)滤液中一定含有的微粒是______ 。
(5)钨铁合金以钨和铁作为主要成分,是一种被广泛应用的金属材料。在托盘天平的两边各放一个等质量的烧杯,在一边烧杯中放入ag锌粒,另一边烧杯中放入ag钨铁合金,然后分别加入等质量和等质量分数的足量稀硫酸。待充分反应后,天平仍然保持平衡。则钨铁合金中铁和钨的质量比为:_______ 。

(1)操作1中粉碎白钨矿的作用是
(2)操作3中发生的反应为2NH3•H2O+H2WO4=(NH4)2SO4+2X,X的化学式为
(3)写出加入过量盐酸时发生的一个复分解反应的化学方程式:
(4)滤液中一定含有的微粒是
(5)钨铁合金以钨和铁作为主要成分,是一种被广泛应用的金属材料。在托盘天平的两边各放一个等质量的烧杯,在一边烧杯中放入ag锌粒,另一边烧杯中放入ag钨铁合金,然后分别加入等质量和等质量分数的足量稀硫酸。待充分反应后,天平仍然保持平衡。则钨铁合金中铁和钨的质量比为:
您最近一年使用:0次
解题方法
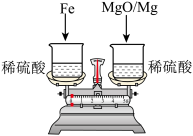
2 . 在托盘天平的两盘上各放一只烧杯,分别盛有等质量、等质量分数的足量的稀硫酸,向左边烧杯中加入56 g铁,向右边烧杯中加入58 g镁和氧化镁的混合物,充分反应后天平保持平衡,则参加反应的铁与氧化镁中氧元素的质量比为______ 。
您最近一年使用:0次
解题方法
3 . 将盛有等质量、等溶质质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的镁和铁,待反应停止后,请判断:
(1)若天平仍保持平衡,烧杯中一定没有剩余的物质是_______ 。
(2)若天平失去平衡,则指针一定偏向放_______ 的一边。
(1)若天平仍保持平衡,烧杯中一定没有剩余的物质是
(2)若天平失去平衡,则指针一定偏向放
您最近一年使用:0次
名校
解题方法
4 . 如图,托盘上各放一只等质量的烧杯,分别盛有等质量、等质量分数的稀硫酸,天平平衡,再向烧杯中分别加入等质量的铁粉和锌粉。
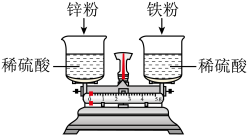
(1)反应一段时间后,右边烧杯中溶液的颜色为______ 色。
(2)写出左边烧杯中反应的化学方程式_______ 。
(3)反应初始,观察到天平指针向______ (填“左”或“右”)偏转,由此可验证两种金属的活动性强弱。
(4)反应结束后,两烧杯中的金属完全消失。下列分析正确的是_____ (填序号)。
①为使天平再次平衡,可将游码右移
②右边烧杯中对应溶液的溶质至少一种
③将两烧杯中的所有物质倒入同一废液缸中,此时废液缸中溶液的pH<7

(1)反应一段时间后,右边烧杯中溶液的颜色为
(2)写出左边烧杯中反应的化学方程式
(3)反应初始,观察到天平指针向
(4)反应结束后,两烧杯中的金属完全消失。下列分析正确的是
①为使天平再次平衡,可将游码右移
②右边烧杯中对应溶液的溶质至少一种
③将两烧杯中的所有物质倒入同一废液缸中,此时废液缸中溶液的pH<7
您最近一年使用:0次
名校
解题方法
5 . 金属材料应用广泛,以下是有关金属的工艺及利用。
(1)《天工开物》中记载“凡红铜(纯铜)升黄(黄铜)而后熔化造器”,由此可知黄铜的熔点比纯铜______ (填“高”或“低”)。
(2)古代铁制品“烤蓝”是防止铁制品锈蚀的措施之一。现今将油漆均匀的涂抹在铁制品外表也能起到防锈的作用,其防锈原理是______ 。
(3)湿法冶金:为从含有硝酸银和硝酸镁的废液中回收银,向废液中加入一定量铁粉与铜粉,充分反应后过滤,得到滤渣和滤液。下列说法正确的是______。
(4)定量计算:质量守恒定律的发现使得化学科学由定性研究走向定量研究。在托盘天平两端分别放质量相同且盛有等质量等溶质质量分数的稀硫酸的烧杯,再向两个烧杯中分别加入等质量的锌粒和铜铝合金,充分反应后酸都有剩余,天平保持平衡,则铜铝合金中铜、铝的质量比为______ 。
(1)《天工开物》中记载“凡红铜(纯铜)升黄(黄铜)而后熔化造器”,由此可知黄铜的熔点比纯铜
(2)古代铁制品“烤蓝”是防止铁制品锈蚀的措施之一。现今将油漆均匀的涂抹在铁制品外表也能起到防锈的作用,其防锈原理是
(3)湿法冶金:为从含有硝酸银和硝酸镁的废液中回收银,向废液中加入一定量铁粉与铜粉,充分反应后过滤,得到滤渣和滤液。下列说法正确的是______。
| A.若向滤渣中加入稀盐酸,没有气泡生成,则滤渣中只有Ag |
| B.若滤液为有色溶液,则滤液中至少有2种金属阳离子 |
| C.向滤液中滴加稀盐酸,若产生白色沉淀,则滤液中一定有镁离子、银离子、铁离子,也可能有铜离子 |
| D.所得滤液质量一定比原溶液的质量小 |
(4)定量计算:质量守恒定律的发现使得化学科学由定性研究走向定量研究。在托盘天平两端分别放质量相同且盛有等质量等溶质质量分数的稀硫酸的烧杯,再向两个烧杯中分别加入等质量的锌粒和铜铝合金,充分反应后酸都有剩余,天平保持平衡,则铜铝合金中铜、铝的质量比为
您最近一年使用:0次
23-24九年级上·全国·单元测试
解题方法
6 . 科学思维是在化学学习中基于事实与逻辑进行独立思考和判断,主要包括比较、分类,归纳科学方法。经过半学期化学学习,小金同学归纳了下列有关化学知识。请你帮他完善下列空白:
(1)空气中含有的能使澄清石灰水变浑浊的气体是________ 。
(2)量取16mL液体,应选用___ ,若量取过程中俯视刻度线,则会使所量液体体积____ (填“小于”、“等于”或“大于”)16mL。
A. 10mL量筒 B. 20mL量筒 C. 50mL量筒 D. 胶头滴管
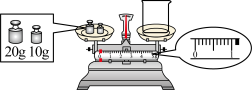
(3)小金用托盘天平称量烧杯的质量,天平平衡后的状态如图所示,她称取的烧杯实际质量为______ g。
(1)空气中含有的能使澄清石灰水变浑浊的气体是
(2)量取16mL液体,应选用
A. 10mL量筒 B. 20mL量筒 C. 50mL量筒 D. 胶头滴管
(3)小金用托盘天平称量烧杯的质量,天平平衡后的状态如图所示,她称取的烧杯实际质量为

您最近一年使用:0次
7 . 金属在生产、生活和社会发展中的应用较为广泛。
(1)考古工作者在三星堆遗址新发现6座三星堆文化“祭祀坑”,发掘并出土了巨型青铜面具。
①青铜与纯铜相比,其硬度更________ (填“大”或“小”),青铜中的铜以________ (填“单质”或“化合物”)形式存在。
②人类最早进入青铜器时代,继而进入铁器时代,而人类利用铝的历史仅100多年,这个先后顺序跟下列因素有关的是________ (填序号)
A.金属的活动性顺序
B.金属的导电、导热性
C.金属的延展性
D.地壳中金属元素的含量
(2)在天平两边的烧杯中分别盛有同质量、同溶质质量分数的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁和铁,充分反应后,若天平平衡,则反应物中一定有剩余的物质________ 。
(3)有一包白色固体粉末可能由 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。
由以上实验可推断:
这包白色固体中肯定存在________ ,肯定不存在________ ;写出②中出现白色浑浊的化学方程式________ 。
(1)考古工作者在三星堆遗址新发现6座三星堆文化“祭祀坑”,发掘并出土了巨型青铜面具。
①青铜与纯铜相比,其硬度更
②人类最早进入青铜器时代,继而进入铁器时代,而人类利用铝的历史仅100多年,这个先后顺序跟下列因素有关的是
A.金属的活动性顺序
B.金属的导电、导热性
C.金属的延展性
D.地壳中金属元素的含量
(2)在天平两边的烧杯中分别盛有同质量、同溶质质量分数的稀硫酸,天平平衡,再向两烧杯中分别加入相同质量的镁和铁,充分反应后,若天平平衡,则反应物中一定有剩余的物质
(3)有一包白色固体粉末可能由
 、
、 、
、 、
、 、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:
、NaCl中的一种或几种组成。为了确定其组成,小东做了以下实验:①取少量白色粉末于研钵中,加入少量的熟石灰粉末混合,研磨,没有闻到氨味;
②另取少量白色粉末加入到适量的水中,出现白色浑浊,静置后,上层清液无色;
③小心倒掉上层清液,向沉淀中加入稀硝酸,白色沉淀完全溶解,并有无色无味的气体产生。
由以上实验可推断:
这包白色固体中肯定存在
您最近一年使用:0次
解题方法
8 . 在天平两端各放一个盛有足量稀盐酸的小烧杯,调至天平平衡。分别将一定质量的镁、铝放入两个烧杯中,待金属耗尽后,天平仍保持平衡。写出该过程发生反应的化学方程式______ (一个即可),加入镁和铝的质量比是______ 。
您最近一年使用:0次
2023-05-22更新
|
70次组卷
|
3卷引用:2023年河南省南阳市镇平县中考二模化学试题
解题方法
9 . 用化学用语填空
(1)①2个铁离子______ ;
②胃酸的主要成分______ 。
(2)在托盘天平的两个托盘上各放一个盛有等质量、等质量分数稀盐酸的烧杯,此时天平平衡。向两烧杯中分别加入等量铁和锌。
①若酸是足量的,从反应开始时到反应结束,观察到天平的指针______ 。
②当两烧杯中的金属都反应完后,若将游码移到0.9刻度处天平重新平衡,则左盘加入的物质是______ 。
③若反应结束天平平衡,则金属的反应情况为______ (写一种情况即可)。
(1)①2个铁离子
②胃酸的主要成分
(2)在托盘天平的两个托盘上各放一个盛有等质量、等质量分数稀盐酸的烧杯,此时天平平衡。向两烧杯中分别加入等量铁和锌。
①若酸是足量的,从反应开始时到反应结束,观察到天平的指针
②当两烧杯中的金属都反应完后,若将游码移到0.9刻度处天平重新平衡,则左盘加入的物质是
③若反应结束天平平衡,则金属的反应情况为
您最近一年使用:0次
10 . 填空。
(1)用化学用语填空。
①天然气的主要成分____ 。
②3Fe2+表示____ 。
(2)溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。

①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______ 。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是______ (填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______ 。(结果精确到0.1%)
(3)在托盘天平的两个托盘上各放一个盛有等质量、等质量分数稀盐酸的烧杯,此时天平平衡。向两烧杯中分别加入等量铁和锌。
①若酸是足量的,从反应开始时到反应结束,观察到天平的指针__________ 。
②若反应结束天平平衡,则金属的反应情况为__________________ (写一种情况即可)。
(1)用化学用语填空。
①天然气的主要成分
②3Fe2+表示
(2)溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。

①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为
(3)在托盘天平的两个托盘上各放一个盛有等质量、等质量分数稀盐酸的烧杯,此时天平平衡。向两烧杯中分别加入等量铁和锌。
①若酸是足量的,从反应开始时到反应结束,观察到天平的指针
②若反应结束天平平衡,则金属的反应情况为
您最近一年使用:0次



