解题方法
1 . 下列是部分化学知识的归纳,其中完全正确的一组是
| A.物质的分类 | B.资源的利用和保护 |
| ①氧化物中含有氧元素 ②混合物中一定含有多种元素 | ①保护空气要减少有害气体和烟尘的排放 ②爱护水资源要节约用水和防止水体污染 ③保护金属资源只能通过防止金属腐蚀实现 |
| C.“低碳经济”的措施 | D.用“化学”眼光分析 |
| ①改造或淘汰高能耗、高污染产业 ②研制和开发新能源替代传统能源 ③教科书循环使用 | ①洗涤剂去油污是因为起乳化作用 ②湿衣服晾干是因为分子之间有间隔 ③用适量的熟石灰改良酸性土壤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 人类的生产生活离不开金属材料。
(1)某兴趣小组探究Fe、Cu、Ag、R四种金属活动性顺序(R在化合物中化合价为+2价),进行了如下实验:___________ 。
②一段时间后,将烧杯中铁丝替换为R进行实验,如图B所示。若甲中出现气泡,乙中无明显现象,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为___________ ,写出R与稀硫酸反应的化学方程式___________ 。
(2)地球上的矿物是不可再生资源,下列对金属资源的保护措施可行的是___________。
(1)某兴趣小组探究Fe、Cu、Ag、R四种金属活动性顺序(R在化合物中化合价为+2价),进行了如下实验:
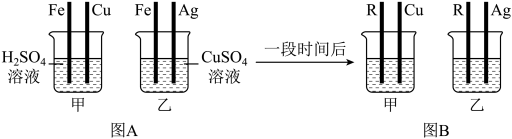
②一段时间后,将烧杯中铁丝替换为R进行实验,如图B所示。若甲中出现气泡,乙中无明显现象,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为
(2)地球上的矿物是不可再生资源,下列对金属资源的保护措施可行的是___________。
| A.合理开采金属矿物 | B.禁止使用金属制品 | C.回收废弃旧金属 |
您最近一年使用:0次
解题方法
3 . 请回答下列问题。
(1)请写出一种防止铁生锈的措施。
(2)铝具有很好的抗腐蚀性能,原因是______ 。
(3)请写出一种保护金属资源的途径。
(1)请写出一种防止铁生锈的措施。
(2)铝具有很好的抗腐蚀性能,原因是
(3)请写出一种保护金属资源的途径。
您最近一年使用:0次
解题方法
4 . 阅读科普短文,回答下列问题。
钛(化学式为Ti)外观似不锈钢,熔点达1672℃。我国钛资源较丰富,仅四川攀枝花地区发现的钛储量,就接近国外探明钛储量的总和。钛机械性能强,可塑性好,易于加工,密度小且强度高,常用于制造性能优异的轻质合金。
但钛和钛合金的刚性差,切削物体时易磨损。
钛和钛合金有优异的耐腐蚀性。在常温下,钛不能与浓度小于5%的盐酸反应,若温度升高或盐酸浓度升高,钛也能和盐酸反应。钛和钛合金对海水很稳定,将钛或钛合金放入海水中数年,取出后,仍光亮如初,远优于不锈钢。
工业上常通过以下工艺流程(如下图)冶炼金属钛。___________ (填“金属”或“合成”)材料。下列产品的制造中不适合使用钛和钛合金的是___________ (填字母)。
A.厨房刀具 B.船舶 C.眼镜框架
(2)下列措施中,能有效保护钛金属资源的是___________(填字母)。
(3)钛铁矿的主要成分为钛酸亚铁,钛酸亚铁的化学式可用 表示,其中钛元素的化合价为+4价,则该化学式中的x=
表示,其中钛元素的化合价为+4价,则该化学式中的x=___________ 。
(4)请将“反应1”的化学方程式补充完整,
___________ 。“反应2”的基本反应类型为___________ 。
(5)上述冶炼过程得到的金属钛中常混有少量铁。为了得到纯净的金属钛,可以在常温下,通过加入足量的___________ 将铁除去,且金属钛的质量不会改变。
钛(化学式为Ti)外观似不锈钢,熔点达1672℃。我国钛资源较丰富,仅四川攀枝花地区发现的钛储量,就接近国外探明钛储量的总和。钛机械性能强,可塑性好,易于加工,密度小且强度高,常用于制造性能优异的轻质合金。
但钛和钛合金的刚性差,切削物体时易磨损。
钛和钛合金有优异的耐腐蚀性。在常温下,钛不能与浓度小于5%的盐酸反应,若温度升高或盐酸浓度升高,钛也能和盐酸反应。钛和钛合金对海水很稳定,将钛或钛合金放入海水中数年,取出后,仍光亮如初,远优于不锈钢。
工业上常通过以下工艺流程(如下图)冶炼金属钛。
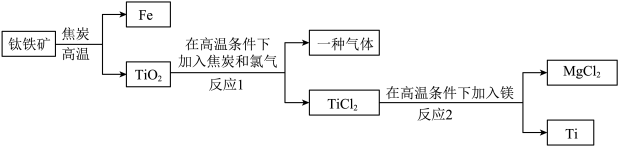
A.厨房刀具 B.船舶 C.眼镜框架
(2)下列措施中,能有效保护钛金属资源的是___________(填字母)。
| A.回收利用废旧金属制品中的钛 | B.任意开采钛金属矿石 |
(3)钛铁矿的主要成分为钛酸亚铁,钛酸亚铁的化学式可用
 表示,其中钛元素的化合价为+4价,则该化学式中的x=
表示,其中钛元素的化合价为+4价,则该化学式中的x=(4)请将“反应1”的化学方程式补充完整,

(5)上述冶炼过程得到的金属钛中常混有少量铁。为了得到纯净的金属钛,可以在常温下,通过加入足量的
您最近一年使用:0次
2024-04-13更新
|
79次组卷
|
4卷引用:2024年黑龙江省哈尔滨市南岗区九年级中考一模物理 化学试卷 -初中化学
2024年黑龙江省哈尔滨市南岗区九年级中考一模物理 化学试卷 -初中化学2024年黑龙江省哈尔滨市南岗区九年级一模化学试题(已下线)化学(哈尔滨卷)-【试题猜想】2024年中考考前最后一卷(已下线)03 押辽宁卷第11题 科普阅读题-备战2024年中考化学临考题号押题(辽宁卷)
解题方法
5 . 下列关于金属的说法正确的是
| A.铝只有在加热的条件下才能与氧气反应 |
| B.工业炼铁的主要产物是生铁 |
| C.不锈钢是纯铁,抗腐蚀能力强 |
| D.回收冶炼废弃金属浪费燃料和资源 |
您最近一年使用:0次
2024-04-12更新
|
179次组卷
|
3卷引用:2024年辽宁省中考百校联合模拟化学试题(一)
解题方法
6 . 我国高铁创造的中国速度令人瞩目。兴趣小组同学开展了高铁建设中的项目学习之旅。
项目一:金属材料的选择
(1)高铁铁轨多使用铁合金而不用纯铁,是因为铁合金的硬度比纯铁______ (填“大”或“小”)。
项目二:金属材料的制取
(2)实验室模拟工业炼铁的装置如图1所示,要检验气体产物,试剂X应为______ 。
(3)图2中,能证明铁生锈需要氧气的实验是______ (填序号)。
项目四:为列车蚀刻车牌
(4)用砂纸清除铁片表面杂质后,用镊子夹取铁片放入熔化的石蜡中形成保护膜,冷却后用笔刻画图案,最后用 溶液完成蚀刻。该过程中发生反应的化学方程式为
溶液完成蚀刻。该过程中发生反应的化学方程式为______ 。
项目五:我国金属资源的现状和保护
(5)我国科学家用竹子做原料,研发出的竹缠绕复合材料已正式投入到高铁车厢的建造中、使用竹缠绕复合材料代替金属材料的优点有______ (写一条)。
项目一:金属材料的选择
(1)高铁铁轨多使用铁合金而不用纯铁,是因为铁合金的硬度比纯铁
项目二:金属材料的制取
(2)实验室模拟工业炼铁的装置如图1所示,要检验气体产物,试剂X应为
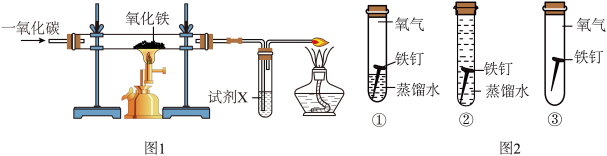
(3)图2中,能证明铁生锈需要氧气的实验是
项目四:为列车蚀刻车牌
(4)用砂纸清除铁片表面杂质后,用镊子夹取铁片放入熔化的石蜡中形成保护膜,冷却后用笔刻画图案,最后用
 溶液完成蚀刻。该过程中发生反应的化学方程式为
溶液完成蚀刻。该过程中发生反应的化学方程式为项目五:我国金属资源的现状和保护
(5)我国科学家用竹子做原料,研发出的竹缠绕复合材料已正式投入到高铁车厢的建造中、使用竹缠绕复合材料代替金属材料的优点有
您最近一年使用:0次
2024-04-10更新
|
45次组卷
|
2卷引用:2024年陕西省咸阳市秦都区咸阳方圆学校模拟预测化学试题
解题方法
7 . 在进行“垃圾的分类与回收利用”的跨学科实践活动时,兴趣小组对金属垃圾(主要成分是铁、铜、氧化铁和二氧化硅)的处理及综合利用的部分工艺如图所示。请回答下列问题:______ 。由此流程可推知SiO2的性质有______ (填字母)。
A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应
(2)步骤③发生反应的基本反应类型是______________ 。
(3)请写出步骤②所发生反应的化学方程式:____________________ 。
(4)倡导金属垃圾回收利用的意义是____________________________ 。
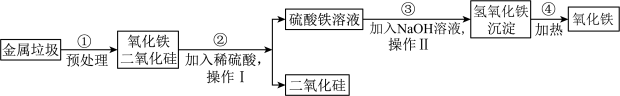
A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应
(2)步骤③发生反应的基本反应类型是
(3)请写出步骤②所发生反应的化学方程式:
(4)倡导金属垃圾回收利用的意义是
您最近一年使用:0次
名校
解题方法
8 . 下列关于资源和能源的叙述正确的是
| A.空气中稀有气体的质量分数约为0.94% |
| B.我国的金属矿物储量丰富,其中铜、铝、锰等储量居世界前列 |
| C.地球上水资源丰富,淡水约占全球水储量的96.5% |
| D.作为高能燃料,液氢已经应用于航天等领域 |
您最近一年使用:0次
9 . 龙是中华民族的图腾,是祥瑞与威仪的象征。纪录片《如果国宝会说话》中曾经介绍过唐代国宝“鎏金铁芯铜龙”,该国宝以铁铸造内芯,铁上包铜,外层鎏金,整个龙身飞扬舒展,反映出唐代高超的铸造工艺。某兴趣小组的学生们了解“鎏金铁芯铜龙”的历史渊源、艺术特色及主要材质后,对国宝展开了讨论。
【国宝选材】
(1)“鎏金铁芯铜龙”选用铁、铜和金三种不同的金属为材料,下列对于金属性质的描述能作为选材依据的是__________。
(2)金属材料的性能与用途息息相关,请用“—”进行连线。
【铸造工艺】
“鎏金铁芯铜龙”的铸造工艺体现出唐代工匠对金属材料的性质及性能的思考及运用,某兴趣小组同学针对国宝提出了几个问题并设计实验进行验证。
(3)问题一:为何是“铁铸内芯”,而不是“铁制外层”?
根据学过的铁的性质可知,铁在空气中易与__________ 发生反应,导致生锈,因此“铁铸内芯”。
(4)问题二:如何实现“铁上包铜”?
西汉古籍《淮南万毕术》中有“曾青得铁则化为铜,外化而内不化”这样的记载,中国劳动人民意识到铜盐溶液里的铜能被铁置换,从而实现“铁上包铜”。为了模拟此过程,某兴趣小组将打磨光亮的铁钉放入CuSO4溶液中,实验中除观察到铁钉表面有红色固体析出,溶液变为浅绿色外,还看到出现小气泡。小组同学对“出现小气泡”这一异常现象展开探究。
查阅资料:CuSO4溶液呈酸性,铁与酸性溶液反应会产生氢气;溶液中氢离子浓度越大,酸性就越强,pH越小;FeSO4溶液会与氧气发生反应从而产生氢离子。
探究一:探究CuSO4溶液酸性强弱的影响因素
小组同学利用打磨光亮的铁钉与不同的CuSO4溶液进行如表实验。并记录了现象。
①由实验bd推知:温度相同时,CuSO4溶液酸性强弱与溶液的浓度有关;由实验__________ 推知:浓度相同时,CuSO4溶液酸性强弱与温度有关。
探究二:探究铁与CuSO4溶液反应过程中的酸性强弱变化及其原因
将打磨光亮的铁钉放入30mL5%冷的CuSO4溶液中,插入pH传感器检测溶液pH变化(如图1),同时插入氧气传感器检测密闭容器内氧气含量的变化(如图2)。___________ (填“增强”或“减弱”),其原因是________ 。请再设计一个对比实验继续进行验证:用__________ 配制30mL5%的CuSO4溶液,放入光亮的铁钉,用pH传感器测密闭容器中溶液的pH。
③小组同学又配制了30mL5%的CuSO4溶液,放入光亮的铁钉,用pH传感器测密闭容器中溶液pH变化(如图3),分析图3,依据__________ 可判断铁与硫酸铜溶液的反应已经停止。
④有细心的同学发现,同样用30mL5%的CuSO4溶液做实验,图1和图3曲线的起点pH不同,原因可能是_________ ,请设计实验进行验证_________ 。
⑤依据上述探究实验,利用铁钉和硫酸铜溶液验证质量守恒定律时装置需要___________ 。
⑥在铁制模型镀铜前要用酸清除铁表面的氧化膜,请写出盐酸去除氧化膜的化学方程式__________ ,但不能长时间用酸浸泡铁制模型的原因是__________ 。
【国宝防护】
(5)鎏金除具有装饰作用外,还可以起到保护器物的作用。防止金属腐蚀是保护金属资源的一个重要方法,除此,还有哪些保护金属资源的方法:__________ (写出一条即可)。
【国宝选材】
(1)“鎏金铁芯铜龙”选用铁、铜和金三种不同的金属为材料,下列对于金属性质的描述能作为选材依据的是__________。
| A.金具有金色光泽,可以作为表层用于装饰 |
| B.金比铁的硬度小,易变形 |
| C.铁的硬度最大,能够保持龙飞扬的姿态,不易变形 |
| D.铜的延展性比铁更好,易于铸造 |
(2)金属材料的性能与用途息息相关,请用“—”进行连线。
| 合金性能 | 合金用途 |
| 不锈钢具有较强的抗腐蚀性 | 做保险丝 |
| 铅锑合金熔点低 | 做人体植入物,如假肢等 |
| 硬铝强度和硬度大 | 做医疗器械、炊具、容器、反应釜 |
| 钛合金无毒、质轻、生物相容性好 | 用于飞机、火箭、轮船等制造业 |
【铸造工艺】
“鎏金铁芯铜龙”的铸造工艺体现出唐代工匠对金属材料的性质及性能的思考及运用,某兴趣小组同学针对国宝提出了几个问题并设计实验进行验证。
(3)问题一:为何是“铁铸内芯”,而不是“铁制外层”?
根据学过的铁的性质可知,铁在空气中易与
(4)问题二:如何实现“铁上包铜”?
西汉古籍《淮南万毕术》中有“曾青得铁则化为铜,外化而内不化”这样的记载,中国劳动人民意识到铜盐溶液里的铜能被铁置换,从而实现“铁上包铜”。为了模拟此过程,某兴趣小组将打磨光亮的铁钉放入CuSO4溶液中,实验中除观察到铁钉表面有红色固体析出,溶液变为浅绿色外,还看到出现小气泡。小组同学对“出现小气泡”这一异常现象展开探究。
查阅资料:CuSO4溶液呈酸性,铁与酸性溶液反应会产生氢气;溶液中氢离子浓度越大,酸性就越强,pH越小;FeSO4溶液会与氧气发生反应从而产生氢离子。
探究一:探究CuSO4溶液酸性强弱的影响因素
小组同学利用打磨光亮的铁钉与不同的CuSO4溶液进行如表实验。并记录了现象。
| 实验 | 不同的CuSO4溶液 | 出现浅绿色溶液速度 | 有无红色固体生成 | 有无气泡 |
| a | 3%CuSO4冷溶液 | 96s | 有 | 无 |
| b | 3%CuSO4热溶液 | 77s | 有 | 无 |
| c | 5%CuSO4冷溶液 | 48s | 有 | 无 |
| d | 5%CuSO4热溶液 | 23s | 有 | 有 |
探究二:探究铁与CuSO4溶液反应过程中的酸性强弱变化及其原因
将打磨光亮的铁钉放入30mL5%冷的CuSO4溶液中,插入pH传感器检测溶液pH变化(如图1),同时插入氧气传感器检测密闭容器内氧气含量的变化(如图2)。
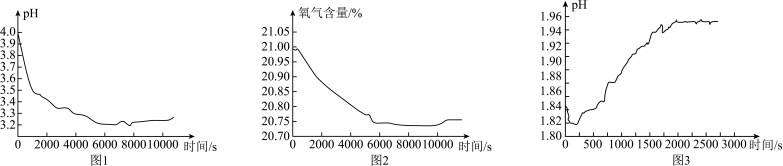
③小组同学又配制了30mL5%的CuSO4溶液,放入光亮的铁钉,用pH传感器测密闭容器中溶液pH变化(如图3),分析图3,依据
④有细心的同学发现,同样用30mL5%的CuSO4溶液做实验,图1和图3曲线的起点pH不同,原因可能是
⑤依据上述探究实验,利用铁钉和硫酸铜溶液验证质量守恒定律时装置需要
⑥在铁制模型镀铜前要用酸清除铁表面的氧化膜,请写出盐酸去除氧化膜的化学方程式
【国宝防护】
(5)鎏金除具有装饰作用外,还可以起到保护器物的作用。防止金属腐蚀是保护金属资源的一个重要方法,除此,还有哪些保护金属资源的方法:

您最近一年使用:0次
解题方法
10 . 下列做法中,不利于保护金属资源的是
| A.用塑钢代替不锈钢 | B.防止金属腐蚀 |
| C.过度开采金属矿物 | D.回收易拉罐 |
您最近一年使用:0次



