1 . 常温下向一定量的稀盐酸中逐滴加入氢氧化钠溶液至过量,绘制溶液中水的质量、生成水的质量随氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是

| A.乙表示生成水的质量 |
| B.加入b克氢氧化钠溶液时,恰好完全反应 |
| C.加入a克氢氧化钠溶液时,所得溶液中溶质为氯化氢 |
| D.加入b克氢氧化钠溶液时,溶液中氯化钠的质量分数最大 |
您最近一年使用:0次
2024-06-14更新
|
88次组卷
|
4卷引用:2024年江苏省盐城市两校联考中考二模化学试题
2024年江苏省盐城市两校联考中考二模化学试题2024年江苏省盐城市两校联考中考二模综合I物理、化学合卷-初中化学(已下线)专题09 酸碱盐和化肥-【好题汇编】2024年中考化学二模试题分类汇编(江苏专用)(已下线)专题12 酸和碱-【好题汇编】2024年中考化学二模试题分类汇编(全国通用)
解题方法
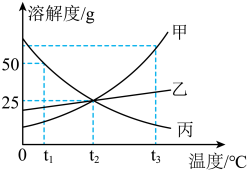
2 . 如图是甲、乙、丙三种物质的溶解度曲线。 ℃三种物质的饱和溶液升温
℃三种物质的饱和溶液升温 ℃,溶质质量分数由小到大的关系是
℃,溶质质量分数由小到大的关系是________ 。
(2)将 ℃时25g丙的饱和溶液降温到
℃时25g丙的饱和溶液降温到 ℃时,若使该溶液变成饱和溶液,需加入丙质量是
℃时,若使该溶液变成饱和溶液,需加入丙质量是________ g。
(3)现有含少量甲的乙固体,若要通过结晶法进行提纯乙,(甲和乙不发生化学反应),现有下列实验步骤可供选择:
①取一定量的水将固体溶解 ②趁热过滤
③用少量水洗涤晶体并烘干 ④加热蒸发至大部分晶体析出
合理的操作顺序为________ (填顺序编号)。
(4) ℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定量的水(析出晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小关系为
℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定量的水(析出晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小关系为________ 。
 ℃三种物质的饱和溶液升温
℃三种物质的饱和溶液升温 ℃,溶质质量分数由小到大的关系是
℃,溶质质量分数由小到大的关系是(2)将
 ℃时25g丙的饱和溶液降温到
℃时25g丙的饱和溶液降温到 ℃时,若使该溶液变成饱和溶液,需加入丙质量是
℃时,若使该溶液变成饱和溶液,需加入丙质量是(3)现有含少量甲的乙固体,若要通过结晶法进行提纯乙,(甲和乙不发生化学反应),现有下列实验步骤可供选择:
①取一定量的水将固体溶解 ②趁热过滤
③用少量水洗涤晶体并烘干 ④加热蒸发至大部分晶体析出
合理的操作顺序为
(4)
 ℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定量的水(析出晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小关系为
℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定量的水(析出晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小关系为
您最近一年使用:0次
3 . 水和溶液与人类的生活息息相关。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以___________ 悬浮于水中的杂质,使之从水中沉降出来。明矾的化学式可用KAl(SO4)x·12H2O来表示,其中x=___________ 。
(2)我国科学家屠呦呦因为对青蒿素的研究取得巨大成就而荣获了诺贝尔奖。她用乙醚代替水成功提取出青蒿素,说明研究青蒿素在不同的___________ (填“溶质”或“溶剂”)中的溶解性很有价值。为了提高药物在水中或油中的溶解性,对其进行了分子结构修饰,说明了物质的___________ 决定物质的性质。
(3)如图为甲、乙两种不含结晶水的固体物质的溶解度曲线。___________ 乙溶液(填“>”或“<”或“=”)。
②将t2℃时等质量的甲、乙两种物质的饱和溶液,分别降温到t1℃,所得溶液中溶质的质量:甲溶液___________ 乙溶液(填“>”或“<”或“=”)。
(4)20℃时,NaCl的溶解度为36g。20℃时,将一定量NaCl溶液平均分为三份,进行如图所示的实验。据此分析,y=___________ ,每一份NaCl溶液中水的质量为___________ g。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以
(2)我国科学家屠呦呦因为对青蒿素的研究取得巨大成就而荣获了诺贝尔奖。她用乙醚代替水成功提取出青蒿素,说明研究青蒿素在不同的
(3)如图为甲、乙两种不含结晶水的固体物质的溶解度曲线。
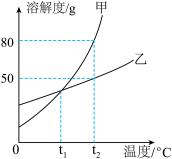
②将t2℃时等质量的甲、乙两种物质的饱和溶液,分别降温到t1℃,所得溶液中溶质的质量:甲溶液
(4)20℃时,NaCl的溶解度为36g。20℃时,将一定量NaCl溶液平均分为三份,进行如图所示的实验。据此分析,y=

您最近一年使用:0次
4 . 我国著名化学家侯德榜先生创立的联合制碱法,极大促进了世界制碱技术的发展。
(1) 和NaCl溶解度曲线如图所示。
和NaCl溶解度曲线如图所示。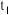 ℃时,174g
℃时,174g 饱和溶液中,溶质与溶剂的质量比为
饱和溶液中,溶质与溶剂的质量比为_____ (填最简整数比)。
②将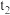 ℃时等质量的
℃时等质量的 饱和溶液和NaCl饱和溶液分别降温至
饱和溶液和NaCl饱和溶液分别降温至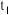 ℃,下列有关说法不正确的是
℃,下列有关说法不正确的是_____ (填字母)。
A.所得溶液的质量: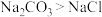
B.所得溶液中溶剂的质量: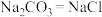
C.所得溶液的溶质质量分数: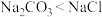
D.析出固体的质量: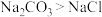
(2) 溶液可用于清洗油污。化学小组对影响
溶液可用于清洗油污。化学小组对影响 溶液去油污效果的因素进行探究。分别用不同温度、不同溶质质量分数的
溶液去油污效果的因素进行探究。分别用不同温度、不同溶质质量分数的 溶液进行实验,数据如下表。
溶液进行实验,数据如下表。
经实验测定,清洗油污的效果是:⑥号>③号,③号>①号,则⑤号_____ (填“>”或“<”)①号。
在家中用苏打清洗油污时,为增强清洗效果,请提出一点合理建议:_____ 。
(1)
 和NaCl溶解度曲线如图所示。
和NaCl溶解度曲线如图所示。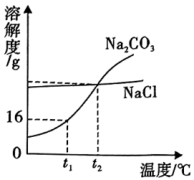
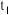 ℃时,174g
℃时,174g 饱和溶液中,溶质与溶剂的质量比为
饱和溶液中,溶质与溶剂的质量比为②将
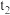 ℃时等质量的
℃时等质量的 饱和溶液和NaCl饱和溶液分别降温至
饱和溶液和NaCl饱和溶液分别降温至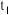 ℃,下列有关说法不正确的是
℃,下列有关说法不正确的是A.所得溶液的质量:
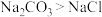
B.所得溶液中溶剂的质量:
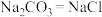
C.所得溶液的溶质质量分数:
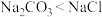
D.析出固体的质量:
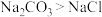
(2)
 溶液可用于清洗油污。化学小组对影响
溶液可用于清洗油污。化学小组对影响 溶液去油污效果的因素进行探究。分别用不同温度、不同溶质质量分数的
溶液去油污效果的因素进行探究。分别用不同温度、不同溶质质量分数的 溶液进行实验,数据如下表。
溶液进行实验,数据如下表。| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% |
| 溶液温度/℃ | 20 | 40 | 60 | 20 | 40 | 60 |
在家中用苏打清洗油污时,为增强清洗效果,请提出一点合理建议:
您最近一年使用:0次
5 . 我国是世界上最早开发和利用海洋的国家之一,海洋资源的合理开发和综合利用对人类有重要意义。
(1)海水淡化:用膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池(海水中体积较大的盐的离子和其他分子不能通过),从而得到淡水。下列说法中,不合理的是______(填字母)。
(2)海水晒盐:海水晒盐能得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线。_____ g。
②t℃时,MgSO4的溶解度大于KCl的溶解度,则t的取值范围是______ 。
③t3℃时,将等质量的MgCl2、KCl和MgSO4三种物质的饱和溶液降温到t2℃,所得溶液的质量由大到小的顺序为______ 。
(3)海水制镁:以海水晒盐后的母液来制取镁的流程如下:______ 。
(1)海水淡化:用膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池(海水中体积较大的盐的离子和其他分子不能通过),从而得到淡水。下列说法中,不合理的是______(填字母)。

| A.膜分离法的原理与滤纸过滤原理类似 |
| B.膜分离法较传统蒸馏法更节约能源 |
| C.加压后右侧海水的溶质质量增大 |
| D.加压后右侧海水的溶质质量分数增大 |
(2)海水晒盐:海水晒盐能得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线。

②t℃时,MgSO4的溶解度大于KCl的溶解度,则t的取值范围是
③t3℃时,将等质量的MgCl2、KCl和MgSO4三种物质的饱和溶液降温到t2℃,所得溶液的质量由大到小的顺序为
(3)海水制镁:以海水晒盐后的母液来制取镁的流程如下:

您最近一年使用:0次
6 . “盐穴储气”是一种地下储能技术,进气时采集盐水(含有NaCl和 ),注水时排天然气,原理如图1所示。NaCl和
),注水时排天然气,原理如图1所示。NaCl和 的溶解度曲线如图2。
的溶解度曲线如图2。
(2)将 ℃时
℃时 的饱和溶液升温至
的饱和溶液升温至 ℃,溶液的溶质质量分数
℃,溶液的溶质质量分数______ (填“变大”、“变小”或“不变”)。
(3) ℃时,取等质量的NaCl和
℃时,取等质量的NaCl和 固体,分别配成饱和溶液,所需水的质量NaCl
固体,分别配成饱和溶液,所需水的质量NaCl______ (填“>”、“<”或“=”) 。
。
(4)如图3所示,将装有NaOH固体的小试管放入盛有X的饱和溶液的烧杯中,然后向试管中滴入少量的水,发现烧杯中立即出现浑浊,则X为______ (填“NaCl”或“ ”),滴入水前X饱和溶液的温度一定
”),滴入水前X饱和溶液的温度一定______ (填字母)。
A.小于 ℃ B.大于或等于
℃ B.大于或等于 ℃ C.小于
℃ C.小于 ℃
℃
 ),注水时排天然气,原理如图1所示。NaCl和
),注水时排天然气,原理如图1所示。NaCl和 的溶解度曲线如图2。
的溶解度曲线如图2。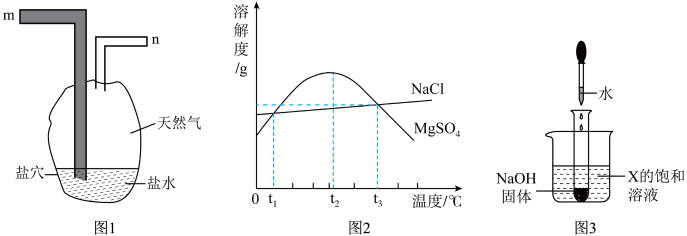
| A.天然气是可再生能源 | B.天然气难溶于盐水 |
| C.从m端进气可采集盐水 | D.从n端进水可排天然气 |
(2)将
 ℃时
℃时 的饱和溶液升温至
的饱和溶液升温至 ℃,溶液的溶质质量分数
℃,溶液的溶质质量分数(3)
 ℃时,取等质量的NaCl和
℃时,取等质量的NaCl和 固体,分别配成饱和溶液,所需水的质量NaCl
固体,分别配成饱和溶液,所需水的质量NaCl 。
。(4)如图3所示,将装有NaOH固体的小试管放入盛有X的饱和溶液的烧杯中,然后向试管中滴入少量的水,发现烧杯中立即出现浑浊,则X为
 ”),滴入水前X饱和溶液的温度一定
”),滴入水前X饱和溶液的温度一定A.小于
 ℃ B.大于或等于
℃ B.大于或等于 ℃ C.小于
℃ C.小于 ℃
℃
您最近一年使用:0次
7 . 溶解度曲线反映了溶解度随温度的变化规律。如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线图,下列说法正确的是

A. ℃时,甲、乙两种物质的溶液中溶质的质量分数相等 ℃时,甲、乙两种物质的溶液中溶质的质量分数相等 |
B. ℃时,100g甲的饱和溶液中甲的质量为25g ℃时,100g甲的饱和溶液中甲的质量为25g |
| C.将丙的饱和溶液转化为不饱和溶液可采用升温的方法 |
D.将 ℃时等质量的甲、乙、丙三种物质的饱和溶液降温到 ℃时等质量的甲、乙、丙三种物质的饱和溶液降温到 ℃,析出晶体最多的是甲 ℃,析出晶体最多的是甲 |
您最近一年使用:0次
真题
解题方法
8 . 如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是

| A.t1℃时,甲和丙的饱和溶液中所含溶质的质量相等 |
| B.乙溶液中混有少量甲时可采用降温结晶的方法提纯乙 |
| C.t2℃时,将25g甲物质加入到50g水中充分溶解后可以形成75g溶液 |
| D.将t2℃时甲、乙、丙三种物质的饱和溶液分别降温到t1℃后,所得溶液溶质质量分数由大到小的关系是乙>甲=丙 |
您最近一年使用:0次
9 . 向50g一定溶质质量分数的硫酸铜溶液中逐滴加入氢氧化钡溶液,用数字化传感器测得溶液的电导率与氢氧化钡溶液质量的关系如图所示(溶液中离子浓度越高,电导率越高),下列分析正确的是

| A.结合图甲,硫酸铜溶液中含有的阳离子为Cu2+ |
| B.反应过程中可观察到有沉淀生成,颜色为白色 |
| C.图乙中D点时,向溶液中滴加酚酞,溶液会变红 |
| D.图乙中,B→C→D过程中烧杯中溶质质量逐渐增大 |
您最近一年使用:0次
解题方法
10 . 我国航天员王亚平利用乙酸钠溶液演示太空“冰雪”实验。已知不同温度时,乙酸钠固体的溶解度曲线如下图所示。下列说法正确的是

| A.a点溶液溶质的质量分数40% |
| B.从a点到b点,溶液由饱和溶液变不饱和溶液 |
| C.10℃的乙酸钠溶液升温到40℃,溶质的质量分数增大 |
| D.40℃时,将80g乙酸钠固体加入到100g水中,所得溶液的质量为180g |
您最近一年使用:0次



