2022八年级上·浙江·专题练习
1 . 小海做自然界中“冬季排碱”模拟实验,他首先配制了40℃的碳酸钠热饱和溶液,然后冷却至4℃,其操作过程如图:

(1)在向甲烧杯中添加碳酸钠粉末过程中,充分搅拌,若观察到___________ 现象,则甲溶液已饱和。
(2)乙丙溶液中溶质的质量分别为a、b,则a、b的大小关系为___________ 。
(3)用图2装置回收丙烧杯中的固体,当蒸发皿中出现大量固体,仅剩少许液体时,该如何操作___________ 。

(1)在向甲烧杯中添加碳酸钠粉末过程中,充分搅拌,若观察到
(2)乙丙溶液中溶质的质量分别为a、b,则a、b的大小关系为
(3)用图2装置回收丙烧杯中的固体,当蒸发皿中出现大量固体,仅剩少许液体时,该如何操作
您最近一年使用:0次
2 . 如图是粗盐提纯的相关实验操作,以下说法不正确的是( )


| A.正确实验操作步骤为①②③④ |
| B.步骤②溶解应该在烧杯中进行 |
| C.步骤②③④中玻璃棒的作用不完全相同 |
| D.步骤④当水分全部蒸发之后再熄灭酒精灯 |
您最近一年使用:0次
2021九年级下·浙江·专题练习
3 . 下列图示实验操作中,正确的是( )
A. 点燃酒精灯 点燃酒精灯 | B. 稀释浓硫酸 稀释浓硫酸 |
C. 过滤液体 过滤液体 | D. 加热蒸发 加热蒸发 |
您最近一年使用:0次
4 . 下列混合物可以用降温结晶法分离的是( )
| A.分离泥沙和食盐的混合物 |
| B.在混有少量食盐的硝酸钾中分离出固体硝酸钾 |
| C.分离乙醇和水的混合物 |
| D.从食盐溶液中把食盐分离出来 |
您最近一年使用:0次
2021八年级上·浙江·专题练习
5 . 观察下列实验装置图,按要求作答:

(1)填写仪器名称:X________ ,Y________ 。
(2)为下列实验挑选合适的装置(填序号)。
①从水中提取较纯净的水使用装置________ ;
②从食盐溶液中分离出食盐使用装置________ ;
③为除去黄河水中的泥沙应使用装置________ ;
(3)图C中有一处错误,请指出_________ ,蒸馏烧瓶中放几块碎瓷片的作用是__________ 。

(1)填写仪器名称:X
(2)为下列实验挑选合适的装置(填序号)。
①从水中提取较纯净的水使用装置
②从食盐溶液中分离出食盐使用装置
③为除去黄河水中的泥沙应使用装置
(3)图C中有一处错误,请指出
您最近一年使用:0次
2021八年级上·浙江·专题练习
6 . 下列实验操作中,玻璃棒的作用与其它三个不同的是( )
A. 溶解 溶解 | B. 稀释 稀释 |
C. 过滤 过滤 | D. 蒸发 蒸发 |
您最近一年使用:0次
2021八年级上·浙江·专题练习
7 . 以下混合物的分离方法中,不正确的是( )
| 选项 | 混合物 | 分离方法 |
| A | 色拉油和水 | 加热溶解、过滤 |
| B | 氯化钠中混有少量泥沙 | 溶解、过滤、蒸发结晶 |
| C | 酒精和水 | 蒸馏 |
| D | 食盐和水 | 蒸发结晶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021八年级上·浙江·专题练习
8 . 分离混合物常用的方法有:(1)过滤;(2)蒸发;(3)蒸馏;(4)冷却热饱和溶液;(5)沉淀法。选择合理的方法分离下列混合物(填序号)。
A.食盐和砂___________ ; B.酒精和水___________ ;
C.从海水中获取食盐___________ D含少量氯化钠的硝酸钾___________
A.食盐和砂
C.从海水中获取食盐
您最近一年使用:0次
2021八年级下·浙江·专题练习
9 . 通过下列实验操作不能达到相应目的是( )
A. 配制蔗糖溶液 配制蔗糖溶液 | B.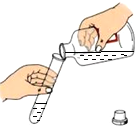 取用液体药品 取用液体药品 |
C.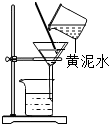 获取纯净水 获取纯净水 | D.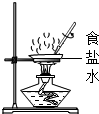 获取氯化钠晶体 获取氯化钠晶体 |
您最近一年使用:0次
2021八年级·浙江·专题练习
10 . 小金用铜粉、浓 和
和 反应制备硫酸铜晶体(
反应制备硫酸铜晶体( ),探究硫酸铜晶体产率的影响因素,实验步骤如下。
),探究硫酸铜晶体产率的影响因素,实验步骤如下。
步骤一:称取3.0g铜粉于容器中,并加入一定质量某浓度的稀 溶液;
溶液;
步骤二:再加入3.3克一定浓度的浓硝酸,40℃水浴加热五分钟。
步骤三:调节溶液的pH=4.0,然后过滤、蒸发结晶,并用无水酒精洗涤、干燥制得硫酸铜晶体。
步骤四:改变加入浓硝酸的质量,重复上述实验1-3步操作。测得硫酸铜晶体的质量,计算产率如表。
请回答下列问题:

(1)在过滤和蒸发、结晶实验操作中,图乙中不需要 用到实验器材的有___________ ;
(2)结合上图表格的实验数据,得出的结论是___________ ;
(3)实验过程中产生少量 气体有毒,需要用
气体有毒,需要用 溶液吸收,同时鼓入一定量氧气,生成硝酸钠和水,其化学方程式
溶液吸收,同时鼓入一定量氧气,生成硝酸钠和水,其化学方程式___________ ;
(4)结晶用无水酒精洗涤而不用水洗涤的原因___________ 。
 和
和 反应制备硫酸铜晶体(
反应制备硫酸铜晶体( ),探究硫酸铜晶体产率的影响因素,实验步骤如下。
),探究硫酸铜晶体产率的影响因素,实验步骤如下。步骤一:称取3.0g铜粉于容器中,并加入一定质量某浓度的稀
 溶液;
溶液;步骤二:再加入3.3克一定浓度的浓硝酸,40℃水浴加热五分钟。
步骤三:调节溶液的pH=4.0,然后过滤、蒸发结晶,并用无水酒精洗涤、干燥制得硫酸铜晶体。
步骤四:改变加入浓硝酸的质量,重复上述实验1-3步操作。测得硫酸铜晶体的质量,计算产率如表。
请回答下列问题:
| 浓硝酸的质量/g | 3.3 | 4.5 | 5.6 | 6.8 | 8.0 | 9.2 | 10.4 | 11.6 | 12.81 | 14.0 | 15.2 |
| 硫酸铜晶体的产率% | 25.2 | 36.1 | 54.4 | 71.2 | 83.8 | 81.2 | 69.3 | 63.7 | 60.8 | 58.4 | 57.6 |

(1)在过滤和蒸发、结晶实验操作中,图乙中
(2)结合上图表格的实验数据,得出的结论是
(3)实验过程中产生少量
 气体有毒,需要用
气体有毒,需要用 溶液吸收,同时鼓入一定量氧气,生成硝酸钠和水,其化学方程式
溶液吸收,同时鼓入一定量氧气,生成硝酸钠和水,其化学方程式(4)结晶用无水酒精洗涤而不用水洗涤的原因
您最近一年使用:0次



