10-11高二上·湖北黄冈·期中
1 . 下列说法完全正确的是
| A.放热反应均是自发反应 |
| B.ΔS 为正值的反应均是自发反应 |
| C.物质的量增加的反应,ΔS为正值 |
| D.如果ΔH和ΔS 均为正值,当温度升高时,反应可能自发进行 |
您最近一年使用:0次
2016-12-09更新
|
489次组卷
|
4卷引用:2010年湖北省黄冈中学高二上学期期中考试试题化学
(已下线)2010年湖北省黄冈中学高二上学期期中考试试题化学(已下线)2011-2012年安徽芜湖一中高二下学期期中考试理科化学试卷2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷吉林省通化市第十四中学2018-2019学年高二上学期期末考试化学试题
2 . 有关化学反应的说法中,正确的是
| A.非自发反应在任何条件下都不能实现 | B.自发反应 都是熵增大的反应 都是熵增大的反应 |
| C.能自发进行的吸热反应一定是熵增大的反应 | D.自发反应都是放热反应 |
您最近一年使用:0次
3 . 下列叙述正确的是
| A.生成物能量一定低于反应物总能量 |
| B.吸热反应和熵减的反应都具有自发进行的倾向 |
| C.正、逆反应速率都改变,化学平衡一定发生移动 |
D.同温同压下,H2(g)+Cl2(g) 2HCl(g)在光照和点燃条件下的ΔH相同 2HCl(g)在光照和点燃条件下的ΔH相同 |
您最近一年使用:0次
4 . 如何解决好碳排放问题是关系到人类可持续发展的重大课题之一。目前,采用较多的方法是对二氧化碳进行捕集封存和富集再利用。下列与二氧化碳有关的叙述正确的是
| A.CO2是形成酸雨的主要物质 |
| B.CO2导致温室效应,是一种大气污染物 |
C.CO2(g)+C(s) 2CO(g) H>0,高温有利于该反应自发进行 2CO(g) H>0,高温有利于该反应自发进行 |
| D.实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳 |
您最近一年使用:0次
2016-12-09更新
|
123次组卷
|
3卷引用:2016届湖北武汉华中师大一附中等八校高三上联考一理化学卷
5 . 下列对化学反应的说法正确的是
| A.化学反应过程中,分子的种类一定发生改变 |
| B.已知2A(g)+B(g)⇌C(g)+D(s)△H<0,则该反应一定能自发进行 |
| C.有化学键发生断裂,就有化学反应的发生 |
| D.放热反应的反应速率一定比吸热反应的反应速率大 |
您最近一年使用:0次
10-11高二上·湖北孝感·期中
6 . 一定温度下,对可逆反应A(g)+2B(g) 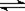 3C(g)的下列叙述中,能说明反应已达到平衡的是(A、B为无色气体,C为有色气体)
3C(g)的下列叙述中,能说明反应已达到平衡的是(A、B为无色气体,C为有色气体)
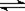 3C(g)的下列叙述中,能说明反应已达到平衡的是(A、B为无色气体,C为有色气体)
3C(g)的下列叙述中,能说明反应已达到平衡的是(A、B为无色气体,C为有色气体)| A.混合气体的物质的量不再变化 |
| B.单位时间内消耗amolA,同时生成3amolC |
| C.容器内的压强不再变化 |
| D.容器内气体颜色不再变化 |
您最近一年使用:0次
10-11高二上·湖北·期中
7 . 在0.lmol/L的HA溶液中存在如下电离平衡: HA A-+H+,对于该溶液,下列叙述正确的是
A-+H+,对于该溶液,下列叙述正确的是
 A-+H+,对于该溶液,下列叙述正确的是
A-+H+,对于该溶液,下列叙述正确的是| A.滴加少量0.lmol/L HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减少 |
| B.加水,溶液中所有离子浓度均减小 |
| C.加入少量NaA固体,平衡向逆反应方向移动, 溶液中c(OH-)增大 |
| D.加入少量NaOH固体,平衡向正反应方向移动, 溶液中c(H+)增大 |
您最近一年使用:0次
11-12高二下·浙江金华·期中
8 . 如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+ 2B(g)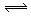 C(g)
C(g) +2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
+2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
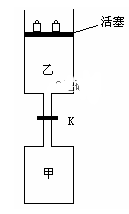
(1)乙中B的转化率为______________ ;
(2)甲中D和乙中C的物质的量比较:__________ (填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为________ (用含V的代数式表示,连通管中气体体积忽略不计)。
 C(g)
C(g) +2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
+2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
(1)乙中B的转化率为
(2)甲中D和乙中C的物质的量比较:
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为
您最近一年使用:0次
9 . 下列说法中,不正确的是
| A.如果反应是在恒温恒压条件下进行的,此时的反应热与焓变相等 |
| B.某吸热反应能自发进行,因此该反应是熵增反应 |
| C.白铁(镀锌)制品镀层受损后,铁制品比受损前更容易生锈 |
| D.一个化学反应的△H仅与反应的起始状态和反应的最终状态有关,与反应途径无关 |
您最近一年使用:0次
10 . 下列说法正确的是
| A.能自发进行的化学反应,一定是△H<0、△S>0 |
| B.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| C.焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 |
| D.钢铁发生电化学腐蚀时,负极的电极反应式为 Fe–3e- = Fe3+ |
您最近一年使用:0次



