名校
1 . 常温下, 在碱性条件下能将
在碱性条件下能将 还原成银(第五周期IB族)。肼还可以用作燃料电池的燃料。一种肼燃料电池的工作原理如图所示,电池工作过程中会有少量
还原成银(第五周期IB族)。肼还可以用作燃料电池的燃料。一种肼燃料电池的工作原理如图所示,电池工作过程中会有少量 在电极表面发生自分解反应生成
在电极表面发生自分解反应生成 、
、 、
、 逸出。下列关于
逸出。下列关于 的说法正确的是
的说法正确的是
 在碱性条件下能将
在碱性条件下能将 还原成银(第五周期IB族)。肼还可以用作燃料电池的燃料。一种肼燃料电池的工作原理如图所示,电池工作过程中会有少量
还原成银(第五周期IB族)。肼还可以用作燃料电池的燃料。一种肼燃料电池的工作原理如图所示,电池工作过程中会有少量 在电极表面发生自分解反应生成
在电极表面发生自分解反应生成 、
、 、
、 逸出。下列关于
逸出。下列关于 的说法正确的是
的说法正确的是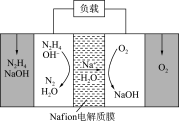
A. 中六个原子共平面 中六个原子共平面 |
| B.电池工作时,负极区消耗的NaOH与正极区生成的NaOH物质的量相等 |
C. 还原成Ag得到的电子基态时填充在4s轨道上 还原成Ag得到的电子基态时填充在4s轨道上 |
D.肼使 转变为 转变为 的反应中,肼作氧化剂 的反应中,肼作氧化剂 |
您最近一年使用:0次
2024-01-05更新
|
126次组卷
|
4卷引用:山西省运城市新绛县第二中学2023-2024学年高三上学期1月月考理综试题
山西省运城市新绛县第二中学2023-2024学年高三上学期1月月考理综试题甘肃省酒泉育英中学等多校2023-2024学年高三上学期12月一轮复习联考(四)化学试题甘肃省张掖市高台县第一中学2023-2024学年高三下学期模拟考化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
解题方法
2 . “乌铜走银”是我国非物质文化遗产之一、匠人以铜为胎,将氧化变黑的银丝( )嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
)嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是

 )嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
)嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
| A.揉搓工序中电子从铜器经汗液流向银丝 |
| B.铜作为原电池的负极发生了吸氧腐蚀 |
| C.铜和银均不活泼,在任何条件下都不能形成原电池 |
| D.用铁丝代替银丝,铜器不会变黑 |
您最近一年使用:0次
2023-12-24更新
|
761次组卷
|
3卷引用:山西省忻州市名校2023-2024学年高三上学期联合质量检测化学试卷
山西省忻州市名校2023-2024学年高三上学期联合质量检测化学试卷广东省部分名校2023-2024学年高三上学期联合质量检测化学试题(已下线)寒假收官卷01-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
解题方法
3 . 氨气是一种重要的化工原料,工业合成氨反应为: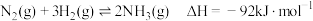 ,将上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有
,将上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有 的稀的A溶液为电解质溶液,下列说法
的稀的A溶液为电解质溶液,下列说法错误 的是

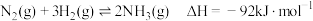 ,将上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有
,将上述合成氨反应设计成燃料电池,工作原理如图所示,其中溶有 的稀的A溶液为电解质溶液,下列说法
的稀的A溶液为电解质溶液,下列说法
| A.a电极为正极,发生还原反应 |
B.A溶液中所含溶质为 ,可用蒸发结晶的方法分离出A ,可用蒸发结晶的方法分离出A |
C.a电极发生的反应为: |
| D.导线中电流方向为a→b |
您最近一年使用:0次
2023-11-16更新
|
661次组卷
|
3卷引用:山西省晋城市第一中学校2023-2024学年高二上学期第五次调研考试化学试题
名校
4 . 银铝电池具有能量密度高的优点,其工作原理如图所示,电池放电时的反应为2Al+3Ag2O+2NaOH+3H2O=2Na[Al(OH)4]+6Ag。
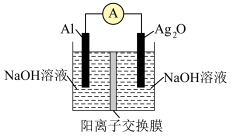
下列说法错误的是

下列说法错误的是
| A.Al为电源负极 | B.正极反应为Ag2O+2e-+H2O=2Ag+2OH- |
| C.放电时负极区pH增大 | D.放电时Na+通过交换膜向右侧移动 |
您最近一年使用:0次
2023-11-10更新
|
687次组卷
|
4卷引用:山西省晋城市第一中学校2023-2024学年高二上学期第五次调研考试化学试题
名校
5 . 室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应: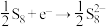 ,
,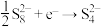 ,
,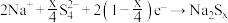
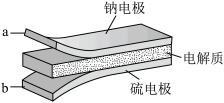
下列叙述错误的是
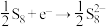 ,
,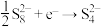 ,
,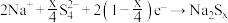

下列叙述错误的是
| A.炭化纤维素纸的作用是增强硫电极导电性能 |
B.放电时负极反应为: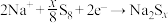 |
C.充电时 从硫电极向钠电极迁移 从硫电极向钠电极迁移 |
D.放电时外电路电子流动的方向是 |
您最近一年使用:0次
2023-09-02更新
|
307次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三上学期第四次调研化学试题
名校
6 . 图示为发表于《科学进展》的一种能够捕捉CO2的电化学装置,下列说法正确的是
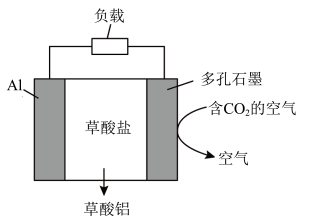

| A.Al电极是阴极 |
B.正极的电极反应为2CO2+2e-= |
| C.每生成1mol的草酸铝,外电路中转移3mol电子 |
D.在捕捉二氧化碳的过程中, 不断移向石墨电极附近 不断移向石墨电极附近 |
您最近一年使用:0次
2023-08-08更新
|
275次组卷
|
3卷引用:山西省三重教育联盟2023-2024学年高三上学期9月联考化学试题
名校
7 . 硼化钒( )-空气电池是目前储电能力最高的电池,电池示意图如图所示(已知:阴离子交换膜只允许阴离子通过)。该电池工作时反应为:
)-空气电池是目前储电能力最高的电池,电池示意图如图所示(已知:阴离子交换膜只允许阴离子通过)。该电池工作时反应为: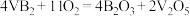 。下列说法正确的是
。下列说法正确的是
 )-空气电池是目前储电能力最高的电池,电池示意图如图所示(已知:阴离子交换膜只允许阴离子通过)。该电池工作时反应为:
)-空气电池是目前储电能力最高的电池,电池示意图如图所示(已知:阴离子交换膜只允许阴离子通过)。该电池工作时反应为: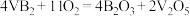 。下列说法正确的是
。下列说法正确的是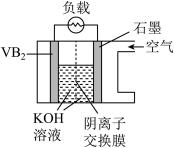
A. 电极为电池正极 电极为电池正极 |
B.电流由石墨电极经导线流向 电极 电极 |
C.当外电路转移1mol电子时,1mol 从 从 电极移向石墨电极 电极移向石墨电极 |
| D.电路中有2mol电子转移时,消耗氧气的体积为11.2L |
您最近一年使用:0次
2023-07-16更新
|
226次组卷
|
6卷引用:山西省怀仁市第一中学校、大地学校高中部2023-2024学年高二上学期第一次月考化学试题
山西省怀仁市第一中学校、大地学校高中部2023-2024学年高二上学期第一次月考化学试题河南省开封市五校2022-2023学年高一下学期期末联考化学试题甘肃省天祝藏族自治县第一中学2023-2024学年高二上学期9月月考化学试题河南省平顶山市叶县高级中学2023-2024学年高二上学期10月月考化学试题河南省郑州市宇华实验学校2023-2024学年高一下学期4月期中考试化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
名校
解题方法
8 . 我国科研工作者设计了一种多功能的质子陶瓷燃料电池膜反应器(如图所示),在单一的膜反应器中实现了乙烯一电能的联产和温室气体 的降解。下列说法正确的是
的降解。下列说法正确的是

| A.电极a为正极,发生氧化反应 |
B. 由电极a移向电极b 由电极a移向电极b |
C.电极b发生的电极反应为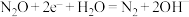 |
D.每生成11.2L ,降解的 ,降解的 的物质的量为0.5 mol 的物质的量为0.5 mol |
您最近一年使用:0次
2023-07-16更新
|
186次组卷
|
4卷引用:山西省应县第一中学校2022-2023学年高二下学期7月期末考试化学试题
解题方法
9 . 常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生,下列说法错误的是
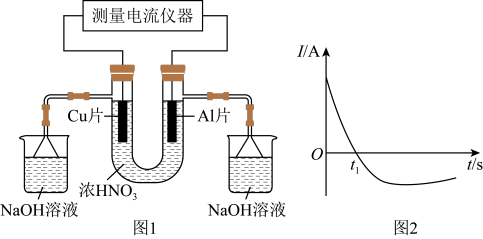
已知:①U形管中盛有足量的浓硝酸;
②电流强度(I)的正负表示电流的方向,正值表示电流方向与规定方向相同,负值表示电流方向与规定的正方向相反。

已知:①U形管中盛有足量的浓硝酸;
②电流强度(I)的正负表示电流的方向,正值表示电流方向与规定方向相同,负值表示电流方向与规定的正方向相反。
| A.O~t1s时,负极为Al片,t1s之后Cu片作负极 |
| B.t1s后电流反转是因为Al片在浓硝酸中完全钝化,氧化膜阻碍了Al继续反应 |
C.t1s前电解质溶液中的 向Cu片移动 向Cu片移动 |
| D.O~t1s时正极的电极反应式与t1s后正极的电极反应式相同 |
您最近一年使用:0次
2023-07-09更新
|
267次组卷
|
2卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
10 . 某化学兴趣小组探究原电池的工作原理,下列设计与工作原理判断正确的是
| 选项 | 电极材料 | 电解质溶液 | 电极反应类型 | 电子移动方向 | 阳离子移动方向 |
| A | Mg、Al | 稀硫酸 | 铝电极:氧化反应 | Al→Mg | Al→Mg |
| B | 石墨、Cu | 浓硝酸 | 铜电极:氧化反应 | Cu→石墨 | 石墨→Cu |
| C | Al、石墨 | 稀盐酸 | 石墨电极:还原反应 | Al→石墨 | Al→石墨 |
| D | Mg、Al | 氢氧化钠溶液 | 铝电极:还原反应 | Mg→Al | Al→Mg |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-09更新
|
431次组卷
|
3卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题



