1 . 银锌电池工作时的总反应式为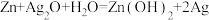 。以该电池为电源,使用惰性电极电解
。以该电池为电源,使用惰性电极电解 溶液,下列说法正确的是
溶液,下列说法正确的是
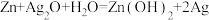 。以该电池为电源,使用惰性电极电解
。以该电池为电源,使用惰性电极电解 溶液,下列说法正确的是
溶液,下列说法正确的是A.电池的正极反应式为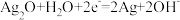 |
B.电池正极生成 时,负极消耗 时,负极消耗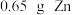 |
C.电解池中阳被生成标准状况下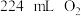 时,阴极生成 时,阴极生成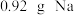 |
| D.电解池中阴、阳两极均生成气体,理论上同温、同压下二者的体积比为2:1 |
您最近一年使用:0次
名校
解题方法
2 . 金属(M)–空气电池结构如图(电池总反应方程式可表示为4M+nO2+2nH2O=4M(OH)n),未来有望被应用于新能源汽车和各种移动设备。下列说法正确的是
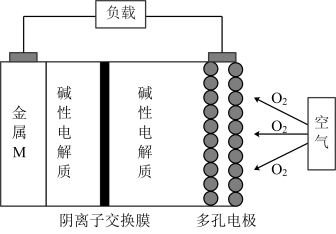

| A.金属(M)–空气电池的正极反应式为O2+2H2O+4e-=4OH- |
| B.若为Mg–空气电池,则每消耗1 mol Mg转移2 mol电子 |
| C.该类电池工作时,碱性电解质中的OH-离子通过阴离子交换膜移向多孔电极 |
| D.Na–空气电池的“理论比能量”(单位质量的电极材料理论上能释放出的最大电能)比Al–空气电池的高 |
您最近一年使用:0次
名校
解题方法
3 . 任意自发的反应在一定条件下均能设计成为原电池,例如配位反应:Cu2+(aq)+4NH3·H2O(aq)=[Cu(NH3)4]2++4H2O可以设计成原电池,该原电池的装置图如图。下列说法错误的是
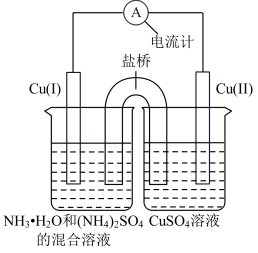

| A.电池工作时,Cu(Ⅱ)电极为原电池的正极 |
| B.电池工作时,氯化钾盐桥中的氯离子向右池移动 |
| C.Cu(Ⅰ)电极上发生的电极反应为:Cu-2e-+4NH3·H2O=[Cu(NH3)4]2++4H2O |
| D.电池工作时,右池中c(Cu2+)增大 |
您最近一年使用:0次
名校
解题方法
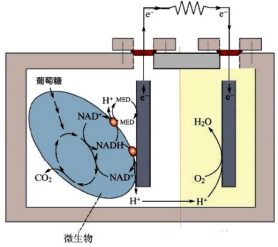
4 . 微生物燃料电池是一种高效、经济的发电装置。一种双室微生物燃料电池的装置如图所示,其中负极反应为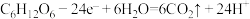 。下列说法错误的是
。下列说法错误的是
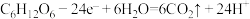 。下列说法错误的是
。下列说法错误的是
| A.该装置可实现化学能转化为电能 |
| B.上图所示装置中,左侧区域为负极区,右侧区域为正极区 |
| C.放电时,正极生成的气体和负极消耗气体的物质的量之比为1:1 |
| D.放电一段时间后,正极区酸性增强 |
您最近一年使用:0次
2021-07-10更新
|
236次组卷
|
2卷引用:山东省滨州市2020-2021学年度第二学期期末考试高一化学试题



